
����Ŀ����������(NaClO2)����ǿ�����ԣ������ֽ⣬����Ư����ʳƷ�������ȡ�
���������Ƶ��Ʊ�
�������Ƶ�Ϊԭ���Ʊ��������ƵĹ����������£�
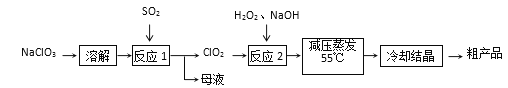
��1���������Ӧ1����Ӧ���ʵĴ�ʩ��__________________�����һ�����ɣ���ĸҺ�����ʵ���Ҫ�ɷ���___________(�ѧʽ)��
��2��ÿ��1mol SO2�μӷ�Ӧ�������Ͽ�����ClO2�����ʵ���Ϊ________mol��
��3�� ����Ӧ2���Ļ�ѧ����ʽΪ_____________________________________��
��4����ȡ����ѹ����������������ѹ��������ԭ����____________________��
��5������Ӧ2����ʹ��H2O2�������������ʵ�ԭ����____________________��
���������Ƶ�Ӧ��
��6��������������ˮ��������ˮ�п��ܲ��������������ƣ����Լ�������������ȥ�������������Σ����������������������Ʒ�Ӧ�⣬��������������____________��
��7��ʵ���ҿ����������ƺ������������������·�Ӧ�Ʊ�ClO2���塣д��������Ӧ�����ӷ���ʽΪ____________________________��
���𰸡��ʵ����߷�Ӧ�¶ȣ���������ҺŨ�ȵ� Na2SO4 2 H2O2+2ClO2+2NaOH=2NaClO2+O2��+2H2O ��ѹ�����¶ȹ��ߣ������������ֽ� �����H2O2�ɷֽ�Ϊ������ˮ���������������� Fe2+������ΪFe3+��Fe3+ˮ������Fe(OH)3��Fe(OH)3���н�������ʣ���������ˮ������ ClO2��+ClO3��+2H+=2ClO2��+H2O
��������
NaClO3����ǿ�����ԣ��ܽ���ڷ�Ӧ�������������Ӧ����ClO2��Na2SO4��ClO2�ڷ�Ӧ������˫��ˮ���������Ʒ�Ӧ�����������ƣ�����ѹ�������ᾧ�õ��侧�塣
(1)���������Һ��ķ�Ӧ��Ϊ��߷�Ӧ���ʣ����ʵ����߷�Ӧ�¶ȣ���������ҺŨ�ȣ�����SO2������Һ�ĽӴ�����ȣ�NaClO3�ڷ�Ӧ�������������Ӧ����ClO2��Na2SO4������ĸҺ�����ʵ���Ҫ�ɷ���Na2SO4��
(2)��Ӧ��SԪ�ػ��ϼ���+4�����ߵ�+6�ۣ�ClԪ�ػ��ϼ���+5�۽��͵�+4�ۣ���ÿ��1mol SO2�μӷ�Ӧ�������Ͽ�����ClO2�����ʵ���Ϊ2mol��
(3)�������ղ���NaClO2����Ԫ�صĻ��ϼۿ�֪��Ӧ2��ClO2��˫��ˮ��ԭ����Ӧ�ķ���ʽΪH2O2+2ClO2+2NaOH=2NaClO2+O2��+2H2O��
(4)��ѹ�����ڽϵ��¶��¿ɽ��У���ֹ��ѹ�����¶ȹ��ߣ�����������Ʒֽ⣻
(5)��˫��ˮ����ԭ��������Ϊˮ���������Ҷ����H2O2�ɷֽ�Ϊ������ˮ���������������ʣ�
(6)Fe2+������ΪFe3+��Fe3+ˮ������Fe(OH)3��Fe(OH)3���н�������ʣ���������ˮ�����ʣ�
(7)�������ƺ������������������·�Ӧ�Ʊ�ClO2���壬�ù�����������������Ԫ�ػ��ϼ�����������������Ԫ�ػ��ϼ۽��ͣ�Ϊ����������ԭ��Ӧ����ϵ����غ��Ԫ���غ��֪����ʽΪClO2-+ClO3-+2H+=2ClO2��+H2O��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʵ�������������Ӧ2Fe3����2I��2Fe2����I2��Ƴ���ͼ��ʾ��ԭ��ء������ж�����ȷ����
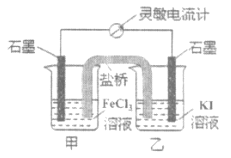
A.��Ӧ��ʼʱ�����е缫��ӦΪ2I����2e����I2
B.��Ӧ��ʼʱ������ʯī�缫��Fe3������ԭ
C.�����ƶ���Ϊ��ʱ����Ӧ�ﵽ��ѧƽ��״̬
D.ƽ��ʱ��������FeCl2���������ָ�벻ƫת
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����º����£���2L�ܱ������м���MgSO4��s����CO��g����������Ӧ��MgSO4��s��+CO��g��MgO��s��+CO2��g��+SO2��g����Ӧ�����вⶨ�IJ������ݼ��±���
��Ӧʱ��/min | n��MgSO4��/mol | n��CO��/mol | n��CO2��/mol |
0 | 2.00 | 2.00 | 0 |
2 | 0.80 | ||
4 | 1.20 |
����˵����ȷ���ǣ�������
A.��Ӧ��0��2min�ڵ�ƽ������Ϊv��SO2��=0.6molL-1min-1
B.��Ӧ��2��4min��������������ܶ�û�б仯
C.�������¶ȣ���Ӧ��ƽ�ⳣ����Ϊ1.00��������ӦΪ���ȷ�Ӧ
D.���������������䣬��ʼʱ�������г���1.00molMgSO4��1.00molCO������ƽ��ʱn��CO2����0.60mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����ijɷ�ΪCu2O��Al2O3��Fe2O3��SiO2����ҵ���øÿ�����ȡͭ�͵����IJ���������ͼ��

��֪����Cu2O��2H+=Cu��Cu2+��H2O��
�ڲ���������������������ʽ����ʱ��Һ��pH���±���ʾ��
������ | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
��ʼ����pH | 5.4 | 4.0 | 2.7 | 5.8 |
������ȫpH | 6.7 | 5.2 | 3.7 | 8.8 |
��1��Ϊ�˼ӿ췴Ӧ������ʣ����Բ�ȡ�Ĵ�ʩ��__(��д1��)��
��2����������A�еijɷ���__��
��3����Ӧ����ɺ���Ԫ�صĴ�����ʽΪ__(�����ӷ���)����������ӳ��õķ���֮һ�ǣ�ȡ�����������ӵ���Һ���Թ��У��μӼ��κ���+3����Ԫ�ص��������Һ�����������.д���÷�Ӧ�����ӷ���ʽ__��
��4������1��Ҫ������__��__��__��ϴ��CuSO4��5H2O�ֲ�Ʒ�����ô���ˮϴ�����ñ�ˮϴ�ӡ�ԭ����__��
��5����NaClO��pH�������ɳ���B����������������Ϣ��������BΪ___���÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ___��
��6����NaOH��pH�������ɳ���C����������������Ϣ����y�ķ�ΧΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��TiO2��TiCl4��Ϊ��Ҫ�Ļ���ԭ�ϣ���֪��
��.TiCl4(g)+O2(g)![]() TiO2(s)+2Cl2(g) ��H=-175.4kJ/mol
TiO2(s)+2Cl2(g) ��H=-175.4kJ/mol
��.2C(s)+O2(g)![]() 2CO(g) ��H=-220.9kJ/mol
2CO(g) ��H=-220.9kJ/mol
��ش��������⣺
��1��TiCl4(g)+2CO(g)![]() TiO2(s)+2C(s)+2Cl2(g)����H=___kJ/mol��
TiO2(s)+2C(s)+2Cl2(g)����H=___kJ/mol��
��2��t��ʱ����10L�����ܱ������г���1molTiCl4��2molO2��������ӦI��4min�ﵽƽ��ʱ���TiO2�����ʵ���Ϊ0.2mol��
�ٷ�Ӧ0~4minĩ��ƽ������v(Cl2)=_�����¶���K=_���÷�����ʾ����O2��ƽ��ת����=__��
�����д�ʩ�����ܼӿ�����Ӧ���ʣ���������O2��ƽ��ת���ʵ���_��
A.�����������
B.�������
C.���������TiO2
D.����O2��Ũ��
E.�����¶�
F.���Ϸ�����������
��t��ʱ����10L�����ܱ������г���3molTiCl4��һ������O2��������ӦI�����������ƽ��ת���ʣ�a%������ʼ�����ʵ���֮�ȣ�TiCl4/O2���Ĺ�ϵ��ͼ1��ʾ���ܱ�ʾO2��ƽ��ת���ʵ�����Ϊ___(����L1������L2��)��M�������Ϊ___(�������������ʾ)��
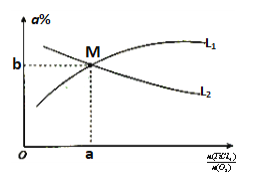
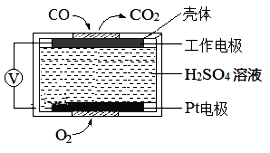
��3��CO���ж����壬�ⶨ������CO�������õķ���֮һ�ǵ绯ѧ������������������CO�������Ĺ���ԭ����ͼ2��ʾ�������缫�ķ�ӦʽΪ___��Ϊ���ٶԻ�����ɵ�Ӱ�죬��CO��H2�����Ʊ��״�(CH3OH)���Լ״�Ϊȼ�ϣ�����Ϊ��������KOH��ҺΪ�������Һ�����Ƴ�ȼ�ϵ�أ��缫����Ϊ���Ե缫�����������Һ��KOH�����ʵ���Ϊ0.8mol������0.5mol�״����뷴Ӧʱ���������Һ�����ʵ���Ҫ�ɷ���___(д��ѧʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Lawrece Liermore����ʵ���ң�LINL���ɹ����ڸ�ѹ�½�![]() ת��Ϊ��������
ת��Ϊ��������![]() �ṹ��ԭ�Ӿ��壬���й���
�ṹ��ԭ�Ӿ��壬���й���![]() ��ԭ�Ӿ���˵������ȷ���ǣ�
��ԭ�Ӿ���˵������ȷ���ǣ�
A. ![]() ��ԭ�Ӿ���ͷ��Ӿ��廥Ϊͬ���칹��
��ԭ�Ӿ���ͷ��Ӿ��廥Ϊͬ���칹��
B. ��һ�������£�![]() ԭ�Ӿ���ת��Ϊ
ԭ�Ӿ���ת��Ϊ![]() ���Ӿ����������仯
���Ӿ����������仯
C. ![]() ��ԭ�Ӿ����
��ԭ�Ӿ����![]() ���Ӿ��������ͬ���������ʺͻ�ѧ����
���Ӿ��������ͬ���������ʺͻ�ѧ����
D. ��![]() ��ԭ�Ӿ����У�ÿһ��Cԭ����Χ���4��Oԭ�ӣ�ÿһ��Oԭ�Ӹ�����Cԭ������
��ԭ�Ӿ����У�ÿһ��Cԭ����Χ���4��Oԭ�ӣ�ÿһ��Oԭ�Ӹ�����Cԭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)NiO(������)����Ľṹ��NaCl��ͬ��Ni2+�����ڽ�O2-�ĺ˼����Ϊa��10-8cm������NiO������ܶ�____________________��(��֪NiO��Ħ������Ϊ74.7gmol-1)
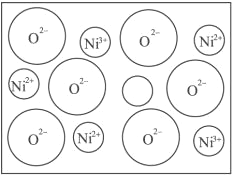
(2)��Ȼ�ĺ;����˹��Ʊ��ľ��嶼���ڸ���ȱ�ݡ����磺��ij��NiO�����оʹ�������ͼ��ʾ��ȱ�ݣ�һ��Ni2+��ȱ����������Ni2+������Ni3+��ȡ�������������Գʵ����ԣ�����������Ni��O�ı�ֵȴ�����˱仯��ij��������Ʒ���ΪNi0.97O���Լ���þ�����Ni3+��Ni2+��������֮��____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
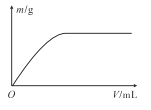
����Ŀ������������Ԫ��X��Y��Z��W��ԭ��������������X��Y��Z��ɵ�һ�ֻ��������Ч��ɱ����״���������ĽṹʽΪ��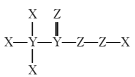 ����W��һ������ˮ��Һ��ͨ��YZ2���壬��������������m��ͨ��YZ2��������V�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
����W��һ������ˮ��Һ��ͨ��YZ2���壬��������������m��ͨ��YZ2��������V�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
A.�⻯����۵�һ���ǣ�Y<Z
B.����������Ӧˮ��������ԣ�Y>W
C.X��Y��Z����Ԫ��ֻ�����һ�ֻ�����
D.��ҵ�ϳ����Ȼ�ԭ��ұ������W
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���������� X ����ij 10 L �ݻ��㶨�����������(�����������������Բ���)���ں㶨�¶���ʹ��ﵽ�ֽ�ƽ�⣺X(s) ![]() 2Y(g)��Z(g)��ʵ���ò�ͬ�¶��µķֽ�ƽ�ⳣ�������±�������˵���в���ȷ���ǣ� ��
2Y(g)��Z(g)��ʵ���ò�ͬ�¶��µķֽ�ƽ�ⳣ�������±�������˵���в���ȷ���ǣ� ��
�¶ȣ� oC�� | 15.0 | 25.0 | 30.0 | 35.0 |
K/(��10��8 mol3��L��3) | 0.205 | 1.64 | 4.68 | 10.8 |
A.�÷�Ӧ�ڸ����¿����Է�
B.��Z���������������ʱ��仯ʱ��ʾ��Ӧ��ƽ��״̬
C.���ں����£�ѹ������������ٴδ�ƽ���n(X)��ԭƽ���
D.35��ʱ����ƽ��ʱ��X�ֽ���0.03 mol
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com