
����Ŀ��ˮ����![]() ����Ҫ�Ļ���ԭ�ϣ��㷺��Ӧ����ҽҩ��ũҩ��Ⱦ�ϵȡ����ڹ�ҵ�ϳ����������������Ʊ�����Ӧԭ��Ϊ
����Ҫ�Ļ���ԭ�ϣ��㷺��Ӧ����ҽҩ��ũҩ��Ⱦ�ϵȡ����ڹ�ҵ�ϳ����������������Ʊ�����Ӧԭ��Ϊ![]() ��ijͬѧ��ʵ����ģ�¹�ҵ�Ʊ������Ʊ�
��ijͬѧ��ʵ����ģ�¹�ҵ�Ʊ������Ʊ�![]() ���ش��������⣺
���ش��������⣺
(1)![]() ��Һ���Ʊ���װ����ͼ��ʾ��
��Һ���Ʊ���װ����ͼ��ʾ��

��ʵ�������ö������̺�Ũ�����Ʊ����������ӷ���ʽΪ_________________��
��ʵ����Ҫ�õ�![]() ��NaOH��Һ�����Ƹ���Һ���貣����������Ͳ���_____��
��NaOH��Һ�����Ƹ���Һ���貣����������Ͳ���_____��
����ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ___________________________��
�������ʵ����Ҫ���������к͵ζ�ԭ���ⶨ��Ӧ����ƿ�л����Һ��NaOH��Ũ�ȡ��������ṩ�Լ������ʵ�鷽����____________________________���ṩ���Լ��У�![]() ��Һ��
��Һ��![]() ��Һ��
��Һ��![]() �����ᡢ��̪��Һ��
�����ᡢ��̪��Һ��
(2)ˮ���µ��Ʊ���װ����ͼ��ʾ��

ʵ�鲽�裺���Ʒ�Ӧ�¶�![]() ����װ����ʡ��
����װ����ʡ��![]() ������Һ©������Һ��������������ƿ�У���ַ�Ӧ������������������ƿ�ڵ���Һ���ռ�
������Һ©������Һ��������������ƿ�У���ַ�Ӧ������������������ƿ�ڵ���Һ���ռ�![]() �������ƿ�С���֪
�������ƿ�С���֪![]() ����Һ©���е���Һ��_________
����Һ©���е���Һ��_________![]() ����
����![]() ��Һ������NaOH��NaClO�����Һ��
��Һ������NaOH��NaClO�����Һ��![]() ��ѡ���������___________��
��ѡ���������___________��
(3)�����ˮ���º����IJⶨ��
��ȡ���![]() ������������
������������![]() ����
����![]() �ζ������У�������Һ��pH������
�ζ������У�������Һ��pH������![]() ����
����![]() ����ˮ���
����ˮ���![]() ��Һ���Ƴ�
��Һ���Ƴ�![]() ����
����![]() ��
��![]() ��Һ�ζ���ʵ��������
��Һ�ζ���ʵ��������![]() ��Һ��ƽ��ֵΪ
��Һ��ƽ��ֵΪ![]() �������ˮ����
�������ˮ����![]() ����������Ϊ_____��
����������Ϊ_____��![]() ��֪��
��֪��![]()
���𰸡�![]()
![]()
![]() �ձ���������
�ձ��������� ![]() ȡһ������ƿ�ڻ����Һ������������
ȡһ������ƿ�ڻ����Һ������������![]() ��Һ�μ�
��Һ�μ�![]() �η�̪��Һ����
�η�̪��Һ����![]() ������ζ����ظ���������
������ζ����ظ���������![]() ��
�� ![]() ��NaClO�����Һ ���NaClO��Һװ����ƿ�У���Ӧ���ɵ�ˮ���»ᱻNaClO����
��NaClO�����Һ ���NaClO��Һװ����ƿ�У���Ӧ���ɵ�ˮ���»ᱻNaClO���� ![]()
��������
![]() �ٶ������̺�Ũ���ᷴӦ�����Ȼ��̡�������ˮ���ݴ˽��
�ٶ������̺�Ũ���ᷴӦ�����Ȼ��̡�������ˮ���ݴ˽��
������![]() ��NaOH��Һʱ��ʹ����Ͳ��ȡˮ�������ʹ���ձ��ܽ��������ƣ��ò��������裬�ݴ˽��
��NaOH��Һʱ��ʹ����Ͳ��ȡˮ�������ʹ���ձ��ܽ��������ƣ��ò��������裬�ݴ˽��
����ƿ�з���![]() ��Ӧ���ɴ������ơ��Ȼ��ƺ�ˮ���ݴ˽��
��Ӧ���ɴ������ơ��Ȼ��ƺ�ˮ���ݴ˽��
�ܻ����Һ���д������ƣ�ˮ��ʼ��ԣ�����������������ȥ����������ӣ��ʲⶨ����������ҺŨ�ȵ�ʵ�鷽��Ϊ��ȡһ������ƿ�ڻ����Һ������������![]() ��Һ�μ�
��Һ�μ�![]() �η�̪��Һ����
�η�̪��Һ����![]() ������ζ����ظ���������
������ζ����ظ���������![]() �Σ��ݴ˽��
�Σ��ݴ˽��
![]() ������ȡˮ����
������ȡˮ����![]() �ķ�Ӧԭ��Ϊ��
�ķ�Ӧԭ��Ϊ��![]() ����Ϸ�Ӧ����ͷ�Ӧ������жϣ���Һ©���е���Һ��NaOH��NaClO�����Һ����Ϊˮ����
����Ϸ�Ӧ����ͷ�Ӧ������жϣ���Һ©���е���Һ��NaOH��NaClO�����Һ����Ϊˮ����![]() ���л�ԭ�ԣ��ױ����������������������������Һװ����ƿ�У���Ӧ���ɵ�ˮ���»ᱻ���������������ݴ˽��
���л�ԭ�ԣ��ױ����������������������������Һװ����ƿ�У���Ӧ���ɵ�ˮ���»ᱻ���������������ݴ˽��
![]() ��Ϸ�Ӧ������ϵ����õ������ˮ����
��Ϸ�Ӧ������ϵ����õ������ˮ����![]() ������������
������������
![]() �������̺�Ũ���ᷴӦ�����ӷ���ʽΪ
�������̺�Ũ���ᷴӦ�����ӷ���ʽΪ![]()
![]()
![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]()
![]()
![]() ��
��
������![]() ��NaOH��Һʱ��ʹ����Ͳ��ȡˮ�������ʹ���ձ��ܽ��������ƣ��ò��������裬�����Ƹ���Һ���貣����������Ͳ����ձ������������ʴ�Ϊ���ձ�����������
��NaOH��Һʱ��ʹ����Ͳ��ȡˮ�������ʹ���ձ��ܽ��������ƣ��ò��������裬�����Ƹ���Һ���貣����������Ͳ����ձ������������ʴ�Ϊ���ձ�����������
����ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
�ܻ����Һ���д������ƣ�ˮ��ʼ��ԣ�����������������ȥ����������ӣ��ʲⶨ����������ҺŨ�ȵ�ʵ�鷽��Ϊ��ȡһ������ƿ�ڻ����Һ������������![]() ��Һ�μ�
��Һ�μ�![]() �η�̪��Һ����
�η�̪��Һ����![]() ������ζ����ظ���������
������ζ����ظ���������![]() �Σ��ʴ�Ϊ��ȡһ������ƿ�ڻ����Һ������������
�Σ��ʴ�Ϊ��ȡһ������ƿ�ڻ����Һ������������![]() ��Һ�μ�
��Һ�μ�![]() �η�̪��Һ����
�η�̪��Һ����![]() ������ζ����ظ���������
������ζ����ظ���������![]() �Σ�
�Σ�
![]() ������ȡˮ����
������ȡˮ����![]() �ķ�Ӧԭ��Ϊ��
�ķ�Ӧԭ��Ϊ��![]() ����Ϸ�Ӧ����ͷ�Ӧ������жϣ���Һ©���е���Һ��NaOH��NaClO�����Һ����Ϊˮ����
����Ϸ�Ӧ����ͷ�Ӧ������жϣ���Һ©���е���Һ��NaOH��NaClO�����Һ����Ϊˮ����![]() ���л�ԭ�ԣ��ױ����������������������������Һװ����ƿ�У���Ӧ���ɵ�ˮ���»ᱻ���������������ʴ�Ϊ��NaOH��NaClO�����Һ�����NaClO��Һװ����ƿ�У���Ӧ���ɵ�ˮ���»ᱻNaClO������
���л�ԭ�ԣ��ױ����������������������������Һװ����ƿ�У���Ӧ���ɵ�ˮ���»ᱻ���������������ʴ�Ϊ��NaOH��NaClO�����Һ�����NaClO��Һװ����ƿ�У���Ӧ���ɵ�ˮ���»ᱻNaClO������
![]() ��Ϸ�Ӧ������ϵ����õ������ˮ����
��Ϸ�Ӧ������ϵ����õ������ˮ����![]() ������������
������������ 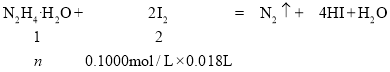 ��
��
![]()
![]() ��250mL��Һ�к��е�ˮ�������ʵ���
��250mL��Һ�к��е�ˮ�������ʵ���![]() ��ˮ����
��ˮ����![]() ����������
����������![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ���ǣ� ��
A.��CuƬ��������ⱥ��ʳ��ˮ��2Cl����2H2O![]() Cl2����H2����2OH��
Cl2����H2����2OH��
B.������ͭƬ���缫���AgNO3��Һ��Cu��2Ag��![]() 2Ag��Cu2��
2Ag��Cu2��
C.��ʯī���缫���FeCl3��Һ��2Cl����2H2O![]() Cl2����H2����2OH��
Cl2����H2����2OH��
D.��ʯī���缫���CuBr2��Һ��2Cu2����2H2O![]() 2Cu��O2����4H��
2Cu��O2����4H��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����֪SO2(g)+ 1/2 O2(g) ![]() SO3(g) ��H = ��98.30kJ��mol���ֽ�4molSO2��һ����O2��Ϻ��ַ�Ӧ�����ų�314.56kJ����ʱ��SO2��ת����Ϊ_________________��
SO3(g) ��H = ��98.30kJ��mol���ֽ�4molSO2��һ����O2��Ϻ��ַ�Ӧ�����ų�314.56kJ����ʱ��SO2��ת����Ϊ_________________��
��2����˹�����������Ϳ�ѧ�о����к���Ҫ�����塣��Щ��Ӧ�ķ�Ӧ����Ȼ��ֱ�Ӳ�ã�����ͨ����ӵķ����ⶨ���ָ�������3���Ȼ�ѧ��Ӧ����ʽ��
Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) ��H�� �D24.8kJ��mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) ��H�� �D47.2kJ��mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ��H�� +640.5kJ��mol
д��CO���廹ԭFeO����õ�Fe�����CO2������Ȼ�ѧ��Ӧ����ʽ��_____________________________
��3����һ�������£�CH4 ��CO��ȼ�յ��Ȼ�ѧ����ʽ�ֱ�Ϊ��
CH4 ( g ) + 2O2 ( g ) = 2H2O ( l ) + CO2 ( g ) ��H = ��890 kJ/mol
2CO ( g ) + O2 ( g ) = 2CO2 ( g ) ��H = ��566 kJ/mol
һ������CH4��CO�Ļ��������ȫȼ��ʱ���ų�������Ϊ262.9 kJ�����ɵ�CO2�ù����ı���ʯ��ˮ��ȫ���գ��ɵõ�50 g��ɫ����������������CH4 ��CO�������_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ѳ������л���Ӧ���ܼ���ʵ�����Ʊ������ѵķ�Ӧ����Ҫʵ��װ�����£�2CH3CH2CH2CH2OH![]() ��CH3CH2CH2CH2��2O+H2O����Ӧ��Ͳ��������������±���
��CH3CH2CH2CH2��2O+H2O����Ӧ��Ͳ��������������±���
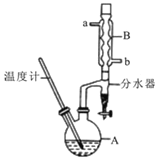

�ٽ�6 mLŨ�����37 g����������һ��˳�����ӵ�A�У����Ӽ�����ʯ��
�ڼ���A�з�ӦҺ��Ѹ��������135�棬ά�ַ�Ӧһ��ʱ�䡣
�۷����ᴿ����A��Һ����ȴ���仺������ʢ��70 mLˮ���¶ȷ�Һ©���У���ҡ���ã���Һ�ôֲ��
�ֲܴ���������40 mLˮ��20 mL NaOH��Һ��40 mLˮϴ�ӣ���Һ�����Լ3g��ˮ�Ȼ��ƿ���������һ��ʱ�����ȥ�Ȼ��ơ�
�ݽ������������Ĵֲ�����������ռ���֣��ô���������11g����ش�
��1���������Ũ�����������������˳��Ϊ��Ӧ�ȼ� ��
��2������Aǰ�����ȴ� ���a����b��������B��ͨ��ˮ��
��3������۵�Ŀ���dz���ϴȥ ����ҡ���ã��ֲ���Ӧ ����ϡ����¡����ڵ�����
��4��������У���������ʱӦ�ռ� ����ѡ����ĸ�����ҵ���֡�
A��100�� B��117�� C��135�� D��142��
��5����Ӧ�����л�۲쵽��ˮ�����ռ���Һ�����ʣ��ҷ�Ϊ�������㣬���ŷ�Ӧ�Ľ��У���ˮ����Һ��������������ʱ���ϲ�Һ�������֧���Զ�����A����ˮ�����ϲ�Һ�����Ҫ�ɷ�Ϊ ���²�Һ�����Ҫ�ɷ�Ϊ ��
��6����ʵ���У������ѵIJ���Ϊ ����ȷ��1%����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�Ȼ���![]() ��һ����Ҫ��±�ػ�����ڻ����������й㷺Ӧ�á��й�һ�Ȼ���IJ�����Ϣ���£�
��һ����Ҫ��±�ػ�����ڻ����������й㷺Ӧ�á��й�һ�Ȼ���IJ�����Ϣ���£�

ijС�������ʵ���Ʊ�һ�Ȼ��Ⲣ�ⶨ�䴿�ȣ�װ����ͼ��ʾ��

����ͼ��ʾװ�ý���ʵ�飬��Dװ���в�������ɫҺ�塢������ʧʱֹͣ��Ӧ��
��ش��������⣺
(1)ʢװ�ⵥ�ʵ�����������_____________��Eװ��������_____________��
(2)![]() װ�����Լ�������______________________________��
װ�����Լ�������______________________________��
(3)д��A�з�Ӧ�����ӷ���ʽ______________________��
(4)������Ӧ��Dװ�õ�������������ˮԡ�У���Ŀ����__________________��
(5)�ֲ�Ʒ�л��еⵥ�ʣ��ᴿ��Ʒ��ѡ������װ���е�_____________![]() ����ĸ
����ĸ![]() ��
��

(6)�ⶨ��Ʒ���ȡ�ȡ![]() �ò�Ʒ����ƿ�����������KI��Һ����ַ�Ӧ����
�ò�Ʒ����ƿ�����������KI��Һ����ַ�Ӧ����![]() ��Һ�ζ�
��Һ�ζ�![]() �йط�Ӧ��
�йط�Ӧ��![]() ��
��![]() ������ƽ��ʵ�����������£�
������ƽ��ʵ�����������£�
![]()
�ò�Ʒ����Ϊ___________![]() �ú�a��c�Ĵ���ʽ��ʾ
�ú�a��c�Ĵ���ʽ��ʾ![]() ������Ʒ�л�������
������Ʒ�л�������![]() ����ý��_______________
����ý��_______________![]() ����ƫ������ƫ����������Ӱ����
����ƫ������ƫ����������Ӱ����![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й���100mL 0.1 mol/L![]() ����100mL 0.1 mol/L
����100mL 0.1 mol/L![]() ������Һ����������ȷ����
������Һ����������ȷ����
A.��Һ��ˮ�������![]() ��������>��B.��Һ�������ӵ����ʵ���Ũ��֮��:��>��
��������>��B.��Һ�������ӵ����ʵ���Ũ��֮��:��>��
C.����Һ��:![]() D.����Һ��:
D.����Һ��:![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������![]() ���л��ϳɵij��û�ԭ����һ���Ʊ������ǽ�����
���л��ϳɵij��û�ԭ����һ���Ʊ������ǽ�����![]() �����ռ���Һ��ϡ����ȣ����ɴ������ƺ�
�����ռ���Һ��ϡ����ȣ����ɴ������ƺ�![]() ��
��![]() ��һ����ɫ���ж��Ŀ�ȼ�����塣ʵ��װ����ͼ��ʾ��
��һ����ɫ���ж��Ŀ�ȼ�����塣ʵ��װ����ͼ��ʾ��
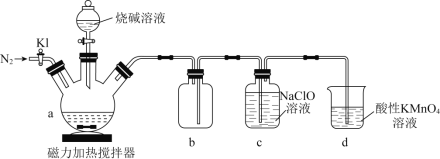
�ش��������⣺
(1)��a�м�����ס�����̿��ĩ����![]() ��ͨ��
��ͨ��![]() һ��ʱ�䣬�ر�
һ��ʱ�䣬�ر�![]() ���������Ƚ��������μ��ռ���Һ��
���������Ƚ��������μ��ռ���Һ��
�ٻ���̿��ĩ��Ϊ���ķ�ɢ����ԭ����_______��b������______________��
��![]() �з�Ӧ�Ļ�ѧ����ʽΪ_______________________________��
�з�Ӧ�Ļ�ѧ����ʽΪ_______________________________��
(2)��Ӧ������![]() ������ͨ��
������ͨ��![]() ��Ŀ����______________________________��d��������__________________��
��Ŀ����______________________________��d��������__________________��
(3)![]() ������
������![]() ��NaCl����������ܽ��
��NaCl����������ܽ��![]() ���£�
���£�
|
| |
NaCl | 37 | 39 |
| 100 | 667 |
��ַ�Ӧ��c�л��Һ����Ũ�����д��������������þ�����Ҫ�ɷֵĻ�ѧʽΪ_____________��Ȼ��________________��______________�����ˡ�ϴ�ӡ�����õ���![]() �Ĵֲ�Ʒ��
�Ĵֲ�Ʒ��
(4)��Ʒ���Ȳⶨ��
ȡ��Ʒm�����![]() ��Һ��ȡ25mL����ƿ�У��ữ�����
��Һ��ȡ25mL����ƿ�У��ữ�����![]() ��ˮ���ڰ�����ַ�Ӧ���Ե�����Һ��ָʾ������
��ˮ���ڰ�����ַ�Ӧ���Ե�����Һ��ָʾ������![]() ��Һ�ζ����յ㣬ƽ������VmL����ط�Ӧ����ʽΪ��
��Һ�ζ����յ㣬ƽ������VmL����ط�Ӧ����ʽΪ��![]() ��
��![]() ����Ʒ���ȱ���ʽΪ________________��
����Ʒ���ȱ���ʽΪ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڷ�Ӧ��������˵����ȷ����
A.Zn(s)+CuSO4(aq)![]() ZnSO4(aq)+Cu(s) ��H=216 kJ/mol��E��Ӧ��<E������
ZnSO4(aq)+Cu(s) ��H=216 kJ/mol��E��Ӧ��<E������
B.CaCO3(s)![]() CaO(s)+CO2(g) ��H=+178.2 kJ/mol��E��Ӧ��<E������
CaO(s)+CO2(g) ��H=+178.2 kJ/mol��E��Ӧ��<E������
C.HCl(g)![]()
![]() H2(g)+
H2(g)+![]() Cl2(g) ��H=+92.3 kJ/mol��1 mol HCl���ܱ������зֽ��ų�92.3 kJ������
Cl2(g) ��H=+92.3 kJ/mol��1 mol HCl���ܱ������зֽ��ų�92.3 kJ������
D.H+(aq)+OH(aq)![]() H2O(l) ��H=57.3 kJ/mol����1 mol NaOH���ռ���Һ�뺬0.5 mol H2SO4��ŨH2SO4��Ϻ�ų�57.3 kJ������
H2O(l) ��H=57.3 kJ/mol����1 mol NaOH���ռ���Һ�뺬0.5 mol H2SO4��ŨH2SO4��Ϻ�ų�57.3 kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾ��װ�ý���ʵ��(�г�������ȥ)������a��b��c�зֱ�ʢ���Լ�1��2��3,�ܴﵽʵ��Ŀ�ĵ���
ѡ�� | �Լ�1 | �Լ�2 | �Լ�3 | ʵ��Ŀ�� | װ�� |
A | Ũ���� | MnO2 | ����NaCl��Һ | �Ʊ�������Cl2 |
|
B | Ũ HNO3 | CuƬ | KI--������Һ | ��֤NO2�������� | |
C | ϡ���� | ��ҺX | �Μ[ʯ��ˮ | ��֤X���Ƿ���CO32- | |
D | ϡ���� | FeS | ����KMnO4��Һ | ��֤H2S���л�ԭ�� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com