
在下述条件下,一定能大量共存的离子组是
A.无色透明的水溶液中:K+、Ba2+、I-、MnO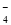
B.含有大量NO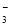 的水溶液中:NH
的水溶液中:NH 、Fe2+、SO
、Fe2+、SO 、H+
、H+
C.C(HCO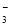 )=0.1 mol·L-1的溶液中:Na+、K+、CO
)=0.1 mol·L-1的溶液中:Na+、K+、CO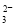 、Br-
、Br-
D.强碱性溶液中:ClO-、S2-、HSO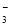 、Na+
、Na+
科目:高中化学 来源:2015届辽宁省抚顺市六校联合体高二下学期期末考试化学试卷(解析版) 题型:选择题
有五瓶溶液分别是①10mL 0.6moL·L-1NaOH水溶液 ②20mL 10.50moL·L-1H2SO4水溶液 ③30mL0.40moL·L-1HCl水溶液 ④40mL0.30moL·L-1CH3COOH水 溶液 ⑤50mL0.20moL·L-1蔗糖水溶液。以上各瓶溶液所含微粒总数的大小顺序是( )
A.①>②>③>④>⑤ B.②>①>③>④>⑤
C.②>③>④>①>⑤ D.⑤>④>③>②>①
查看答案和解析>>
科目:高中化学 来源:2015届福建省福州八市高二下学期期中考试化学试卷(解析版) 题型:选择题
做葡萄糖被新制Cu(OH)2氧化的实验时,有以下步骤:①加入0.5 mL葡萄糖溶液;②加入2%CuSO4溶液4到5滴;③加入10% NaOH溶液2 mL;④加热至沸腾。其正确的操作顺序是( )
A.①②③④ B.②③①④ C.③②①④ D.①③②④
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三上学期第一次检测考试化学试卷(解析版) 题型:选择题
用FeCl3溶液腐蚀印刷电路板上的铜,所得溶液中加入铁粉。对加入铁粉充分反应后的溶液分析合理的是
A.若无固体剩余,则溶液中一定有Fe3+
B.若有固体存在,则溶液中一定有Fe2+
C.若溶液中有Cu2+,则一定没有固体析出
D.若溶液中有Fe2+,则一定有Cu析出
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三上学期第一次检测考试化学试卷(解析版) 题型:选择题
高铁酸钾是一种高效绿色水处理剂,其工业制备的反应原理为
2Fe(OH)3 + 3KClO + 4KOH == 2K2FeO4 + 3KCl + 5H2O,下列说法正确的是
A.制备高铁酸钾用ClO-作还原剂
B.制备高铁酸钾时1 mol Fe(OH)3得到3 mol 电子
C.高铁酸钾中铁的化合价为+7
D.用高铁酸钾处理水时,其还原产物能水解产生具有强吸附能力的胶体
查看答案和解析>>
科目:高中化学 来源:2015届湖南省益阳市高三第一次模拟考试化学试卷(解析版)) 题型:实验题
(8分) 某透明澄清溶液可能含有Na+、Fe3+、Ba2+、CO32-、SO32-、SO42-、Cl-、I-等离子中的几种,为鉴别这些离子,分别取三份少量溶液,按照以下顺序进行三个实验:
实验①:加CCl4,再滴加少量氯水,振荡后,CCl4后层变为紫色;
实验②:加盐酸后,生成无色无味气体,该气体能使饱和石灰水溶液变浑浊;
实验③:加BaCl2溶液产生白色沉淀,过滤出沉淀,在沉淀中加入足量盐酸,沉淀不能完全溶解。
(1)分析上述3个实验,用离子符号写出每一个实验得出的结论,可不必完全填满。
实验①:含有 ;不含 ;
实验②:含有 ;不含 ;
实验③:含有 ;
(2)通过上述实验,不能确定是否存在的离子是 。
查看答案和解析>>
科目:高中化学 来源:2015届湖南省益阳市高三第一次模拟考试化学试卷(解析版)) 题型:选择题
下列解释事实的方程式不正确的是( )
A.测0.1 mol/L的氨水的pH为11: NH3·H2O  NH4+ +OH-
NH4+ +OH-
B.将Na块放入水中,产生气体:2Na+2H2O= 2OH-+2Na++H2↑
C.Al片溶于NaOH溶液中,产生气体:2Al+2OH-+2H2O = 2AlO2-+3H2↑
D.用CuCl2溶液做导电性实验,灯泡发光:CuCl2 Cu2+ +2Cl-
Cu2+ +2Cl-
查看答案和解析>>
科目:高中化学 来源:2015届湖南省高三第一次月考化学试卷(解析版) 题型:实验题
(12分) (1)高锰酸钾保存在棕色试剂瓶,下列试剂保存不需要棕色试剂瓶的是_______。
A.浓硝酸 B.硝酸银 C.氯水 D.纯碱
(2)下列实验中仪器的下端不能插入液面以下的是 (填字母编号)。
A 蒸馏时用的温度计 B 制备乙烯时用的温度计
C 用水吸收氨气的导管口 D 用碱液吸收多余氯气的导管口
E.制备H2的简易装置中加入稀硫酸用的长颈漏斗
F.制备Fe(OH )2时,向FeSO4溶液中滴入NaOH溶液用的胶头滴管
(3)下列有关实验的叙述,正确的是 (填字母编号)。
A 用98%的浓硫酸配制100g10%的稀硫酸溶液时,除使用量筒外还需用到容量瓶
B 测定溶液的pH时,可用洁净、干燥的玻璃棒蘸取溶液,滴在pH试纸上,再与标准比色卡比较
C 不能用分液漏斗将乙醇和水的混合液体分离
D 用浓氨水洗涤做过银镜反应的试管
E.用广泛pH试纸测得氯水的pH为2
F.用碱式滴定管量取20.00mL0.1000mol/L的高锰酸钾溶液
G.用托盘天平称取10.50g干燥的NaCl固体
H.配制一定物质的量浓度的溶液,定容时俯视容量瓶的刻度线,会使所配溶液的浓度偏低
I.用瓷坩埚高温熔融NaOH和Na2CO3的固体混合物
(4)“磨砂”是增加玻璃仪器密封性的一种处理工艺。在仪器A.试管 B.分液漏斗 C.带滴管的试剂瓶(滴瓶) D.集气瓶 E.酸式滴定管 F.碱式滴定管中,没有用到“磨砂”工艺处理的有________。
(填字母编号)。
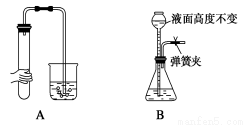
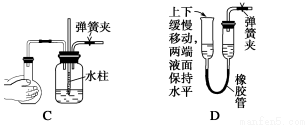
(5))下列各图所示装置的气密性检查中,一定漏气的是 (填字母编号)。
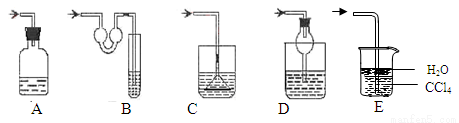
(6)下图各种尾气吸收装置中,适合于吸收NH3气体,而且能防止倒吸的有_____________。
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:填空题
【选修2:化学与技术】(15分)
空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:

(1)步骤④的离子反应方程式为 。
(2)溴微溶于水,步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,它们的相对密度相差较大。分离出液溴的实验室方法为 。
(3)步骤⑥如果在实验室中进行,需用到的玻璃仪器有 。
(4)工业生产不直接蒸馏含溴的海水得到液溴,而要经过“空气吹出、SO2吸收、氯化”,原因是 。
(5)苦卤水还可以用于制取金属镁,用化学方程式表示从苦卤水制取金属镁的反应原理 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com