

请填写以下各空白:
(1)单质A的化学式为_____________。
(2)根据氧化还原反应理论判断:
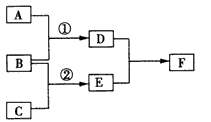
①丙和丁能否在一定条件下相互反应生成D________。(填可能、不可能、无法判断)判断的理由是________,若可能反应则反应的化学方程式为________。(不必写反应条件,若不可能反应则此空不必填写)
②丁和D能否在一定条件下相互反应生成丙________,(填可能、不可能、无法判断)判断的理由是________,若可能反应则反应的化学方程式为________________。
科目:高中化学 来源:湖南省长郡中学2012届高三第二次月考化学试题(人教版) 题型:022
A为单质,B、C、D、E为与A含有相同元素的化合物,它们之间有如下转化关系:
(1)若五种物质的焰色反应均为黄色,其中C、D、E的水溶液均显碱性,且等浓度时碱性C>D>E,B可做供氧剂.
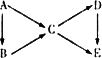
①B的电子式________,C中含有的化学键类型为________(填“离子键”、“极性键”或“非极性键”).
②A转化成C的离子方程式为:________
(2)若常温下A、B、C、D均为气体,且D为红棕色气体.
①D物质的化学式:________.写出B-C的化学方程式为________
②将B和CO2气体通入饱和食盐水中有碳酸氢钠晶体析出,反应的离子方程式是:________
查看答案和解析>>
科目:高中化学 来源:2011-2012学年湖南省高三上学期第二次月考化学试卷 题型:填空题
(9分)A为单质,B、C、D、E为与A含有相同元素的化合物,它们之间有如下转化关系:

(1)若五种物质的焰色反应均为黄色,其中C、D、E的水溶液均显碱性,且等浓度时碱性C〉D〉E,B可做供氧剂。
①B的电子式__________,C中含有的化学键类型为__________ (填“离子键”、“极性键”或“非极性键”)。
②A转化成C的离子方程式为: ____________________
(2)若常温下A、B、C、D均为气体,且D为红棕色气体。
①I)物质的化学式:__________.写出B—C的化学方程式为____________________
②将B和CO2气体通入饱和食盐水中有碳酸氢钠晶体析出,反应的离子方程式是:__________
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:推断题
查看答案和解析>>
科目:高中化学 来源:吉林省模拟题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com