
科目: 来源:2017届江苏省联盟大联考高三2月联考化学试卷(解析版) 题型:选择题
常温下,下列各组离子能在指定溶液中大量共存的是
A. 使甲基橙变红色的溶液中:Na+、Fe2+、MnO4-、AlO2+
B. Kw/c(H+)=1×10-12mol/L,的溶液中:NH4+、Ca2+、Cl-、NO3-
C. PH=0的溶液中:Al3+、Ag(NH3)2+、I-、SO42-
D. 加入Mg能放出H2的溶液中:Ca2+、NH4+、ClO-、NO3-
查看答案和解析>>
科目: 来源:2017届江苏省联盟大联考高三2月联考化学试卷(解析版) 题型:选择题
下列实验方案能达到实验目的的是
A. 证明浓度的的改变可导致平衡移动:将少量KCl晶体加入FeCl3+3KSCN Fe(SCN)3+3KCl的平衡体系中
Fe(SCN)3+3KCl的平衡体系中
B. 除去MgCl2溶液中少量的FeCl3:向含有少量FeCl3的MgCl2溶液中加入足量的Mg(OH)2粉末,搅拌一段时间后过滤
C. 检验某溶液中是否含有乙醛:向盛有2mL 10%CuSO4溶液的试管中滴加0.5mL10%NaOH溶液,混合均匀,滴入待检液,加热
D. 证明Fe3+的氧化性大于I2:将KI溶液和FeCl3溶液在试管中混合后,加入CCl4,振荡、静置,下层溶液显紫红色
查看答案和解析>>
科目: 来源:2017届江苏省联盟大联考高三2月联考化学试卷(解析版) 题型:选择题
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
A. 0.1mol/L的Na2CO3溶液中:c(HCO3-)=2c(HCO3-)+c(H+)- c(OH-)
B. 物质的量浓度之比为1:2的NaClO、NaHCO3混合溶液中: c(HClO)+c(ClO-)=2c(HCO3-)+2c(CO32-)+2c(H2CO3)
C. 向3.0L0.1mol/LNaOH溶液中缓慢通入CO2至溶液增重8.8g时,溶液中: c(Na+)>c(CO32-)> c(HCO3-) >c(OH-)>c(H+)
D. 等物质的量的CH3COOH、CH3COONa混合溶液PH=4.75中:c(CH3COO-)+ c(OH-)>c(CH3COOH)+ c(H+)
查看答案和解析>>
科目: 来源:2017届江苏省联盟大联考高三2月联考化学试卷(解析版) 题型:选择题
一定条件下,在三个容积均为2L的恒容密闭容器中发生反应:H2(g)+CO2(g)  HCOOH(g)。下列说法正确的是
HCOOH(g)。下列说法正确的是
容器编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/mol | |
H2 | CO2 | HCOOH | |||
Ⅰ | 150 | 0.4 | 0.4 | 0.2 | 2 |
Ⅱ | 150 | 0.8 | 0.8 | t1 | |
Ⅲ | 0.4 | 0.4 | 0.16 | t2 | |
A. 反应达到平衡时,容器Ⅰ中的平均反应速率为v(H2)=0.1mol/(L·min)
B. 反应达到平衡时,容器Ⅱ所需时间t2<2min
C. 若只改变一个反应条件,容器Ⅲ可能是加入了合适的催化剂
D. 起始时,向容器Ⅱ中充入0.45mol H2、0.20mol CO2 和0.18molHCOOH,则反应向正反应方向进行
查看答案和解析>>
科目: 来源:2017届江苏省联盟大联考高三2月联考化学试卷(解析版) 题型:填空题
工业上以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(MnCO3)。其工业流程如下:
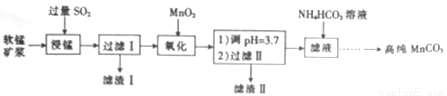
(1)过滤Ⅰ所得滤液中主要存在的两种金属阳离子为____和_____(填离子符号)。
(2)写出氧化过程中MnO2与SO2反应的化学方程式:____________。
(3)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示,为减少MnS2O6的生成,“浸锰”的适宜温度是___________。

(4)向过滤Ⅱ所得的滤液中加入NH4HCO3溶液时温度控制在30-35℃,温度不宜太高的原因是___。
(5)加入NH4HCO3溶液后,生成MnCO3沉淀,同时还有气体生成,写出反应的离子方程式:_______。
(6)生成的MnCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是_________________。
查看答案和解析>>
科目: 来源:2017届江苏省联盟大联考高三2月联考化学试卷(解析版) 题型:推断题
维拉佐酮是临床上使用广泛的抗抑郁药,其关键中间体的合成路线如下:

(1)D中的含氧官能团名称为____________(任写2种)。
(2)B C的反应类型为__________________。
C的反应类型为__________________。
(3)化合物E的结构简式为___________________。
(4)写出同时满足下列条件的B的一种同分异构体的结构简式:______________。
①能发生银镜反应;
②能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应;
③分子中有3种不同化学环境的氢。
(5)已知:RBr RCN
RCN RCOOH。请以甲苯和乙醇为原料制备
RCOOH。请以甲苯和乙醇为原料制备 ,写出相应的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干):____________________________。
,写出相应的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干):____________________________。
查看答案和解析>>
科目: 来源:2017届江苏省联盟大联考高三2月联考化学试卷(解析版) 题型:简答题
K3[Fe(C2O4)3](三草酸合铁酸钾)可用于摄影和蓝色印刷。工业上以H2C2O4(草酸)、FeC2O4(草酸亚铁)、K2C2O4(草酸钾)、双氧水等为原料制备K3[Fe(C2O4)3]的反应原理如下:
氧化:6FeC2O4+3H2O2+6K2C2O4═4K3[Fe(C2O4)3]+2Fe(OH)3
转化:2Fe(OH)3+3K2C2O4+3H2C2O4═2K3[Fe(C2O4)3]+6H2O
(1)制备1mol 三草酸合铁酸钾至少需要H2O2的物质的量为____________。
(2)制备过程中需防止草酸被H2O2氧化,写出草酸被H2O2氧化的化学方程式:______________。
(3)[K3[Fe(C2O4)3·xH2O](三草酸合铁酸钾晶体)是一种光敏材料,为测定该晶体中草酸根的含量和结晶水的含量,某实验小组进行了如下实验:
①称量9.820g三草酸合铁酸钾晶体,配制成250mL溶液.
②取所配溶液25.00mL于锥形瓶中,滴加KMnO4溶液至C2O42-全部转化成CO2时,恰好消耗24.00mL 0.1000mol/L KMnO4溶液。
计算该晶体的化学式,并写出计算过程______________。
查看答案和解析>>
科目: 来源:2017届江苏省联盟大联考高三2月联考化学试卷(解析版) 题型:填空题
某化学兴趣小组以菱铁矿(主要成分为FeCO3,含有SiO2、Al2O3等少量杂质)为原料制备氯化铁晶体(FeCl3·6H2O)的实验过程如下:

(1)酸溶及后续过程中均需保持算过量,其目的除了提高铁元素的浸出率之外,还有___________。
(2)操作Ⅰ名称是_______________。
(3)滴加H2O2溶液氧化时,发生主要反应的离子方程式为_________________。
(4)在氧化过程中,如何检验铁元素全部以Fe3+形式存在:_______________________。
(5)加入过量NaOH溶液的目的是__________________。
(6)请补充完整由过滤后得到的固体制备FeCl3·6H2O的实验方案:向过滤后所得固体______,用水洗涤固体2-3次,低温干燥,得到FeCl3·6H2O。
查看答案和解析>>
科目: 来源:2017届江苏省联盟大联考高三2月联考化学试卷(解析版) 题型:简答题
碘及其化合物在生活中应用广泛。含有碘离子的溶液需回收处理。
(1)“硫碘循环”法是分解水制备氢气的研究热点,涉及下列两个反应:
反应Ⅰ:SO2(g)+I2(aq)+2H2O(l)=2HI(aq)+H2SO4(aq) △H1
反应Ⅱ:HI(aq)=1/2H2(g)+1/2I2(aq) △H2
①反应:SO2(g)+2H2O(1)=H2SO4(aq)+H2(g)的△H=_________(用△H1、△H2表示)。
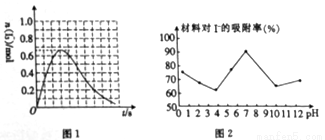
②反应I发生时,溶液中存在如下平衡:I2(aq)+I-(aq)  I3-(aq),其反应速率极快且平衡常数大。现将1mol SO2缓缓通入含1mol I2的水溶液中至恰好完全反应。溶液中I3-的物质的量[n(I3-)]随反应时间(t)的变化曲线如图1所示。开始阶段。N(I3-)逐渐增大的原因是_______________。
I3-(aq),其反应速率极快且平衡常数大。现将1mol SO2缓缓通入含1mol I2的水溶液中至恰好完全反应。溶液中I3-的物质的量[n(I3-)]随反应时间(t)的变化曲线如图1所示。开始阶段。N(I3-)逐渐增大的原因是_______________。
(2)用海带提取碘时,需用氯气将碘离子氧化成单质。酸性条件下,若氯气过量就能将碘单质进一步氧化成碘酸根离子,写出氯气与碘单质反应的离子方程式:____________。
(3)科研小组用新型材料Ag/TiO2对溶液中碘离子进行吸附研究。如图2是不同PH条件下,碘离子吸附效果的变化曲线。据此推断Ag/TiO2材料最适合吸附____(填“酸性”“中性”或“碱性”)溶液中的I-。
(4)氯化银复合吸附剂也可有效吸附碘离子。氯化银复合吸附剂对碘离子的吸附反应为I-(aq)+AgCl(s)
 AgI(s)+Cl-(aq),反应达到平衡后溶液中c(I-)=________[用c(Cl-)、Kap(AgCl)和Kaq(AgI)表示]。该方法去除碘离子的原理是________________。
AgI(s)+Cl-(aq),反应达到平衡后溶液中c(I-)=________[用c(Cl-)、Kap(AgCl)和Kaq(AgI)表示]。该方法去除碘离子的原理是________________。
查看答案和解析>>
科目: 来源:2017届江苏省联盟大联考高三2月联考化学试卷(解析版) 题型:填空题
[物质结构与性质]已知:将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色,继续加入乙醇,析出深蓝色的晶体[Cu(NH3)4]SO4·H2O。硫酸铜溶液中滴入氨基乙酸钠(H2NCH2COONa)可得到如图1所示配合物A。
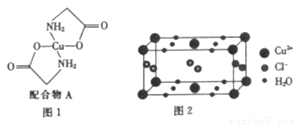
(1)Cu2+基态核外电子排布式为____________。
(2)N、O、S第一电离能由大到小的顺序为_________________。
(3)写出一种与NH3分子互为等电子体的阳离子:_________________。
(4)配合物A中碳原子的轨道杂化类型为_______________。
(5)1mol 氨基乙酸钠(H2NCH2COONa)含有σ键的数目为________。
(6)某含有结晶水的铜的氯化物的晶胞结构如图2所示,该金属氯化物的化学式是_____。(Cl-球的位置:4个在晶面上,2个在晶胞内)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com