
科目: 来源:2016-2017学年四川省成都市北湖校区高二3月月考化学试卷(解析版) 题型:选择题
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g) 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和下图表示:
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和下图表示:
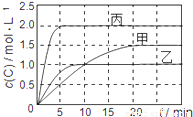
容器 | 甲 | 乙 | 丙 |
容积 | 1L | 1L | 2L |
温度 | T1 | T2 | T2 |
反应物 起始量 | 1molA 2molB | 1molA 2molB | 4molA 8molB |
下列说法正确的是 ( )
A. 由图可知:T1<T2,且该反应为吸热反应
B. T1时该反应的平衡常数K=7.2
C. 前10min甲、乙、丙三个容器中A的平均反应速率:v(A)乙<v(A)甲<v(A)丙
D. 平衡时A的质量m:m乙<m甲<m丙
查看答案和解析>>
科目: 来源:2016-2017学年四川省成都市北湖校区高二3月月考化学试卷(解析版) 题型:填空题
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增加。相关信息如下表所示,根据推断回答下列问题:(答题时A、B、C、D、E、F用所对应的元素符号表示)
A | A原子核外电子有6种不同的运动状态 |
B | B元素的第一电离能比同周期相邻两个元素都大 |
C | C原子在同周期原子中半径最大(稀有气体除外),其单质焰色为黄色 |
D | D原子最外层电子数等于电子层数 |
E | E的基态原子最外层电子排布式为3s23p2 |
F | F与C位于不同周期,F原子核外最外层电子数与C相同,其余各层电子均充满 |
(1)F基态原子核外价电子排布式是________________
(2)A、B、E三种元素电负性由大到小排列顺序为__________________
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如右图所示,其原子的杂化类型为________________

(4)煤燃烧产生的烟气中有B的氧化物,会引起严重的环境问题,因此,常用AH4催化还原以消除污染,已知:
AH4(g)+2 BO2(g)= B2(g)+AO2(g)+2H2O (g) △H1=-867kJ/mol
2BO2(g)  B2O4(g) △H2=-56.9 kJ/mol
B2O4(g) △H2=-56.9 kJ/mol
写出AH4和B2O4反应的热化学方程式__________________
(5)D单质为面心立方晶体,其晶胞边长a=0.405nm,用NA表示阿伏伽德罗常数,列式表示D单质的密度______g·cm-3(不必计算出结果)。
(6)继A60后,科学家又合成了E60、B60, E60分子中每个E原子只跟相邻的3个原子形成共价键,且每个E原子最外层都满足8电子稳定结构,则E60分子中π键的数目为_______________
(7)F的单质和过氧化氢在稀硫酸中可反应,有人将这个反应设计成原电池,请写出该原电池正极反应方程式_______________
(8)某学生所做的有关F元素的实验流程如下图:
F单质 棕色的烟
棕色的烟 绿色溶液
绿色溶液 蓝色沉淀
蓝色沉淀 蓝色溶液
蓝色溶液 黑色沉淀
黑色沉淀
请书写第⑤步反应的离子方程式:___________________
查看答案和解析>>
科目: 来源:2016-2017学年四川省成都市北湖校区高二3月月考化学试卷(解析版) 题型:填空题
Ⅰ.沉淀的生成、溶解和转化在无机物制备和提纯以及科研等领域有广泛应用。
(1)已知25℃时,Ksp(BaSO4)=1×10-10,将BaSO4的悬浊液过滤,滤液中c(Ba2+)=_______mol·L-1。取100 mL滤液与100 mL 2 mol·L-1的Na2SO4溶液混合,混合液中c(Ba2+)=___________ mol·L-1。
(2)长期使用的锅炉需要定期除水垢,否则会降低燃料的利用率。水垢中含有的CaSO4,可先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去。
①CaSO4转化为CaCO3的离子方程式为:_____________________________________________________
②请分析CaSO4转化为CaCO3的原理:______________________________________________________
Ⅱ.在25 ℃时,HSCN、HClO、H2CO3的电离常数如下表:
HClO | HSCN | H2CO3 |
K=3.2×10-8 | K=0.13 | K1=4.2×10-7 K2=5.6×10-11 |
(1)1 mol·L-1的KSCN溶液中,所有离子的浓度由大到小的顺序为_________________________________
(2)向Na2CO3溶液中加入过量HClO溶液,反应的化学方程式为_______________________________
(3)25 ℃时,为证明HClO为弱酸,某学习小组的同学设计了以下三种实验方案。下列三种方案中,你认为能够达到实验目的的是______________________(填下列各项中序号)。
a.用pH计测量0.1mol·L-1NaClO溶液的pH,若测得pH>7,可证明HClO为弱酸
b.用pH试纸测量0.01 mol·L-1 HClO溶液的pH,若测得pH>2,可证明HClO为弱酸
c.用仪器测量浓度均为0.1 mol·L-1的HClO溶液和盐酸的导电性,若测得HClO溶液的导电性弱于盐酸,可证明HClO为弱酸
查看答案和解析>>
科目: 来源:2016-2017学年四川省成都市北湖校区高二3月月考化学试卷(解析版) 题型:实验题
Ⅰ.某校化学课外活动小组进行测定果汁中维生素C(分子式是C6H8O6)含量实验,下面是他们的实验过程及分析报告,请根据此报告填写有关空白。
(1)实验目的:测定××牌软包装鲜橙汁维生素C含量。
(2)实验原理:C6H8O6+I2→C6H6O6+2H++2I-
(3)实验用品和试剂:
①仪器和用品(自选,略)
②试剂:浓度为7.50×10-3mol?L-1的标准碘(水)溶液,指示剂,蒸馏水等。
(4)实验过程:
①洗涤仪器,检查是否漏液,用标准液润洗后装好标准液待用。在此步操作中,用标准液润洗的仪器是______________________。
②打开橙汁包,目测:颜色―橙黄色,澄清度―好,将酸式滴定管用橙汁润洗2~3遍,移取20.00mL橙汁入锥形瓶,向瓶中加入2滴指示剂,该指示剂的名称是___________________________。
③用左手操作滴定管,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色变化。滴定至终点时的现象是
___________________________________________________________________。
(5)数据记录和处理:(设计出表格,将三次滴定所得数据都填入表格中),若经数据处理,滴定中消耗标准碘溶液体积平均值为20.00mL,则此橙汁中维生素C的含量是__________________mg·L-1。
(6)记录测定结果时,滴定前仰视刻度线,滴定到达终点时又俯视刻度线,将导致滴定结果
_________________。(填“偏高”“偏低”或“无影响”)。
Ⅱ.某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的开关K时,观察到电流计的指针发生了偏转。

请回答下列问题:
(1)甲池为__________(填“原电池”“电解池”),A电极的电极反应式为_________________________
(2)丙池中F电极为_____________(填“正极”“负极”“阴极”或“阳极”),该池的总反应方程式为
____________________________________________________________
(3)当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为_________mL(标准状况)。
(4)一段时间后,断开开关K。下列物质能使乙池恢复到反应前浓度的是_________(填选项字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
查看答案和解析>>
科目: 来源:2016-2017学年四川省成都市北湖校区高二3月月考化学试卷(解析版) 题型:填空题
肼(N2H4)是一种高能燃料,在工业生产中用途广泛。
(1)肼(N2H4)也可与NO2发生反应,产物均不污染环境。请写出反应方程式:____________________。
(2)肼性质与氨气相似,易溶于水,可发生如下电离过程:
N2H4 + H2O  N2H5+ + OH- I N2H5+ +H2O
N2H5+ + OH- I N2H5+ +H2O  N2H62+ + OH- II
N2H62+ + OH- II
① 常温下,某浓度N2H6Cl2溶液的pH为4,则该溶液中由水电离产生的c(H+)为__________。
② 已知在相同条件下过程I的进行程度大于N2H5+的水解程度。常温下,若0.2 mol/L N2H4溶液与0.1 mol/L HCl溶液等体积混合,则此时溶液呈_________性,溶液中N2H5+、Cl-、OH-、H+、N2H4浓度由大到小的顺序为___________________。

(3)肼和氧气在不同温度和催化剂条件下生成不同产物(如图):
温度较低时主要发生反应a:N2H4(g)+O2(g) N2(g)+2H2O(g)
N2(g)+2H2O(g)
温度较高时主要发生反应b:N2H4(g)+2O2(g) 2NO(g)+2H2O(g)
2NO(g)+2H2O(g)
①若反应b在1000℃时的平衡常数为K1,1100℃时的平衡常数为K2,则K1__________K2。(填“>”、“<”或“=”)
②某温度下,容积固定的密闭容器中,下列描述可说明反应a达到平衡的是_______________。
A.v(N2)=v(N2H4)
B.c(N2H4):c(O2):c(N2)=1:1:1
C.混合气体的密度不再改变
D.体系的压强不再发生变化
E.混合气体的平均相对分子质量不再发生变化
③1000℃,反应b达到平衡时,下列措施能使容器中 变大的是_______。
变大的是_______。
A.恒容条件下充入He B.增大容器体积 C.恒容条件下下充入N2H4 D.使用催化剂
查看答案和解析>>
科目: 来源:海南省、文昌中学2017届高三下学期联考化学试卷 题型:选择题
下列法不正确的是
A. 氯化钠可用于配制生理盐水 B. 硅单质可用于制造光电池
C. 碘盐中的碘元素以单质存在 D. 氧化铝是优良的耐高温材料
查看答案和解析>>
科目: 来源:海南省、文昌中学2017届高三下学期联考化学试卷 题型:选择题
生物法(加入脱硫细菌)净化含硫废气时发生如下反应:CH3COOH +SO42-=2HCO3-+H2S。下列有关说法正确的是
A. CH3COOH是氧化剂 B. SO42-被氧化
C. H2S的酸性弱于H2CO3 D. 该反应属于复分解反应
查看答案和解析>>
科目: 来源:海南省、文昌中学2017届高三下学期联考化学试卷 题型:选择题
下列反应的生成物不受反应物的用量或浓度或反应条件影响的是
A. SO2与NaOH溶液反应 B. Na与O2的反应
C. Cu在S蒸气中燃烧 D. Fe粉加入HNO3中
查看答案和解析>>
科目: 来源:海南省、文昌中学2017届高三下学期联考化学试卷 题型:选择题
分子式为C4H10O,且不能与钠反应生成H2的结构有(不含立体异构)
A. 2种 B. 3种 C. 4种 D. 5种
查看答案和解析>>
科目: 来源:海南省、文昌中学2017届高三下学期联考化学试卷 题型:选择题
下列有关CuSO4溶液的叙述中正确的是
A. 该溶液呈电中性
B. 它与H2S反应的离子方程式为:Cu2++S2-=CuS↓
C. 用惰性电极电解该溶液时,阳极产生铜单质
D. 在溶液中:c (Cu2+) +c (H+)=c(SO42-) +c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com