
科目: 来源: 题型:
可确认发生了化学平衡移动的是
A. 化学反应速率发生了改变
B. 有气态物质参加的可逆反应达到平衡后,改变了压强
C. 由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变
D. 可逆反应达到平衡后,使用催化剂
查看答案和解析>>
科目: 来源: 题型:
下列反应中,熵减小的是
A.(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) B.2N2O5(g)=4NO2(g)+O2(g)
C.MgCO3(s)=MgO(s)+CO2(g) D.2CO(g)=2C(s)+O2(g)
查看答案和解析>>
科目: 来源: 题型:
已知反应X+Y=M+N为放热反应,对该反应的下列说法中正确的
A. X的能量一定高于M
B. Y的能量一定高于N
C. X和Y的总能量一定高于M和N的总能量
D. 因该反应为放热反应,故不必加热就可发生
查看答案和解析>>
科目: 来源: 题型:
⑴ 向 2.0mL 浓度为 0.1mol / L 的 KCl 、KI 混合溶液中滴加1~2 滴0.01mol / L AgNO3 溶液,振荡,沉淀呈黄色,说明AgCl 的 Ksp 比AgI 的 Ksp (填“小”或“大”)。
⑵ 医药级二水合氯化钙(CaCl2?2H2O)样品中Cl-含量的测定方法是:a. 称取0.7500g样品,溶解,在250mL容量瓶中定容;b. 量取25.00mL待测溶液于锥形瓶中;c. 用0.05000mol / L AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值是20.39mL 。
① 上述测定过程中需用溶液润洗的仪器是 ,如果在测定前没有润洗该仪器,测定结果(质量分数)会
(选填“偏大”、“偏小”或“无影响”)。
② 计算上述样品中CaCl2?2H2O的质量分数。
查看答案和解析>>
科目: 来源: 题型:
如图所示装置,通电 5min 后,第 ③ 极增重2.16 g ,同时在 A 池中收集到224 mL气体(标准状况下)。
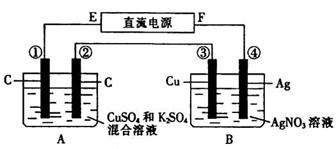
请回答下列问题:
⑴ E为 极;
⑵ 第 ② 极上产生的气体是 ,物质的量为 ;
⑶ 写出第 ① 极上发生反应的电极反应式: ;
⑷ 设A池中原混合液的体积为200mL ,则通电前A池中原混合液中Cu2+的物质的量浓度为 。
查看答案和解析>>
科目: 来源: 题型:
⑴ 在一定温度下,有下列反应发生:
Fe2O3 (s) + 3CO (g) ![]() 2Fe (s) + 3CO2 (g)
2Fe (s) + 3CO2 (g)
① 该反应的平衡常数表达式 K = 。
② 该温度下,在 2L 盛有 Fe2O3 粉末的密闭容器中通入 CO 气体,10min 后,生成了单质铁 11.2g 。则 10min 内 CO 的平均反应速率是 。
③ 请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
a. ;
b. 。
⑵ 在配制 FeCl3 溶液时,加入少许浓盐酸,其目的是:
;
不断加热 FeCl3 溶液,蒸干其水分并灼烧固体,最后得到的物质是 。
⑶ 已知:Fe2O3 (s) + ![]() C(s) =
C(s) = ![]() CO2 (g) + 2Fe(s)
CO2 (g) + 2Fe(s)
△H=+234.1kJ/mol
C (s) + O2 (g) = CO2 (g) △H=-393.5 kJ / mol
则 2Fe (s) + ![]() O2 (g) = Fe2O3 (s)的△H 是 。
O2 (g) = Fe2O3 (s)的△H 是 。
⑷ Fe (OH)2 在空气中短时间内可被氧化为 Fe (OH)3 ,发生的反应为:4Fe(OH)2+O2+2H2O = 4Fe(OH)3 ,下列说法中错误的是
(填字母)。
A. 该反应是能自发进行的反应
B. 该反应是熵增加的反应
C. 该反应是化合反应
D. 该反应是氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
反应 A (g) + B (g) ![]() C (g) + D (g) 过程中的能量变化如下图所示,请回答下列问题:
C (g) + D (g) 过程中的能量变化如下图所示,请回答下列问题:
⑴ 该反应是 (选填“吸热”、“放热”)反应;
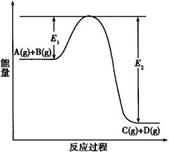 ⑵ 当反应达到平衡时,升高温度,A 的转化率 (选填“增大”、“减小”或“不变”),原因是:
⑵ 当反应达到平衡时,升高温度,A 的转化率 (选填“增大”、“减小”或“不变”),原因是:
;
⑶ 反应体系中加入催化剂对反应热是否有影响?原因是:
;
⑷ 在反应体系中加入催化剂,
反应速率增大,E1 和E2 的变化是:E1 ,E2 (选填“增
大”、“减小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
根据右表提供的数据,判断在等浓度的NaClO 、NaHCO3 混合溶液中,各种离子浓度关系正确的是
A. c (HCO3-)c (ClO-)c (OH-)
B. c (ClO-)c (HCO3-)c (H+)
C. c (HClO)+c (ClO-) = c (HCO3-)+c (H2CO3)
D. c (H+)+c (Na+) = c (HCO3-)+c (ClO-)+c (OH-)
查看答案和解析>>
科目: 来源: 题型:
已知:I2 (aq) + I- (aq) ![]() I3-(aq) 。某I2 、KI混合溶液中,I3-的物质的量浓度c (I3-) 与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是
I3-(aq) 。某I2 、KI混合溶液中,I3-的物质的量浓度c (I3-) 与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是
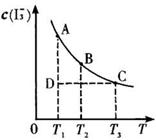
A.反应I2 (aq) + I- (aq) ![]() I3-(aq) 的△H>0
I3-(aq) 的△H>0
B. 若温度为T1、T2 ,反应的平衡常数分别为K1 、K2 ,则K1<K2
C. 若反应进行到状态D时,一定有υ正>υ逆
D. 状态A与状态B相比,状态A的c (I2) 大
查看答案和解析>>
科目: 来源: 题型:
对于常温下 pH 为 1 的硝酸溶液,下列叙述错误的是
A. 该溶液 1mL 稀释至 100mL 后,pH 等于3
B. 向该溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和
C. 该溶液中水电离出的 c(H+) 是 pH 为 3 的硝酸中水电离出的 c(H+)的100 倍
D. 该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为1012
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com