
科目: 来源: 题型:
(9分)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
实验编号 | HA | NaOH | 混合溶液的pH |
甲 | c(HA)=0.2 mol/L | c(NaOH)=0.2 mol/L | pH=a |
乙 | c(HA)=c1 mol/L | c(NaOH)=0.2 mol/L | pH=7 |
丙 | c(HA)=0.1 mol/L | c(NaOH)=0.1 mol/L | pH=9 |
丁 | pH=2 | pH=12 | pH=b |
请回答:
⑴不考虑其它组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸 。
⑵c1 (填<、>或=)0.2mol/L。乙组实验中HA和NaOH溶液混合前,HA溶液中c(A-)与NaOH溶液中c(Na+)的关系是 (从下面选项中选择填空)。
A.前者大 B.后者大 C.二者相等 D.无法判断
⑶从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是
,其中,c(A-)= mol/L(不能做近似计算,回答准确值,结果不一定要化简)。
⑷丁组实验中,HA和NaOH溶液混合前c(HA) (填<、>或=)c(NaOH),b (填<、>或=)7。
查看答案和解析>>
科目: 来源: 题型:
(9分)已知:

一种烃A(分子式符合CnH2n,n代表C原子数)通过臭氧化并经锌和水处理得到B和C。化合物B含碳69.8%,含氢11.6%,B无银镜反应,催化加氢生成D。D在浓硫酸存在下加热,可得到能使溴水褪色且只有一种结构的物质E。反应图示如下:
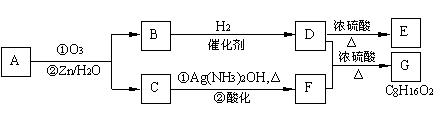
回答下列问题:
⑴B的相对分子质量是 ;B→D的反应类型为 。
⑵D+F→G的化学方程式是: 。
⑶A的结构简式为 。
⑷E发生加聚反应所得高分子的结构简式为 。
查看答案和解析>>
科目: 来源: 题型:
(8分)A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(其它产物已略去)

试回答:
⑴若X是强氧化性单质,则A不可能是 。
a.S b.N2 c.Na d.Mg e.Al
⑵若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀。则B与X反应的化学方程式为 。
⑶若A、B、C均为含有金属元素的无机化合物,无论X是强酸还是强碱,A溶液与C溶液反应都能生成B,则反应的离子方程式为 。
⑷若A、B、C均为含有同种元素的共价化合物,且A的水溶液的pH>7,则A的水溶液的溶质的电离方程式为 。
查看答案和解析>>
科目: 来源: 题型:
(8分)已知:L、M、Q、R、T五种短周期元素,有如下信息:
元素代号 | L | M | Q | R | T |
原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
最高正价或最低负价 | +2 | +3 | +2 | +6、-2 | -2 |
根据上述信息回答下列问题:
⑴M元素在周期表的位置为 周期 族。
⑵L离子的结构示意图是 ,L元素与T元素形成的化合物的化学键为 (填“离子键”、“共价键”)。
⑶T元素形成的含有18电子的无机共价化合物的化学式为 。
⑷L、M、Q三种元素中,金属性最强的是 。写出能说明R与T元素非金属性强弱的一个化学方程式 。
查看答案和解析>>
科目: 来源: 题型:
将固体A置于密闭容器中,在一定温度下发生下列反应:
①A(s)![]() B(g)+C(g);②2C(g)
B(g)+C(g);②2C(g)![]() D(g)+E(g)。
D(g)+E(g)。
达到平衡时,c(D)=0.5mol?L-1,c(C)=4mol?L-1,则此温度下反应①的平衡常数为
A.25 B.20 C.16 D.9
查看答案和解析>>
科目: 来源: 题型:
常温下,AgCl、AgBr、AgI的溶度积常数(Ksp)依次为1.8×10-10mol2?L-2、5.0×10-13mol2?L-2、8.3×10-17mol2?L-2。下列有关说法错误的是
A.常温下在水中溶解能力AgCl>AgBr>AgI
B.在AgCl饱和液中加入足量浓NaBr溶液有AgBr沉淀生成
C.在AgBr饱和溶液中加入足量浓NaCl溶液不可能有AgCl沉淀生成
D.在AgI饱和液中加入NaI固体有AgI沉淀析出
查看答案和解析>>
科目: 来源: 题型:
LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠。已知该电池放电时的电极反应式为:正极 FePO4+Li++e-==LiFePO4 ,负极 Li-e-== Li+。下列说法中正确的是
A.充电时FePO4电极应与外接电源的正极相连
B.充电时电池反应为FePO4+Li = LiFePO4
C.放电时电池内部Li+向负极移动
D.放电时,在正极上是Li+得电子被还原
查看答案和解析>>
科目: 来源: 题型:
已知HI分解的热化学方程式为:2HI(g)![]() H2(g)+I2(s);△H = -53.0kJ/mol。下列说法正确的是
H2(g)+I2(s);△H = -53.0kJ/mol。下列说法正确的是
A.1mol HI在密闭容器中分解后可以放出26.5kJ的能量
B.2mol HI(g)的能量大于1mol H2(g) 与1mol I2(s)的能量总和
C.破坏1mol HI的化学键需要吸收26.5kJ的能量
D.若2HI(g)![]() H2(g)+I2(g);△H = -xkJ/mol(x>0),则x>53.0
H2(g)+I2(g);△H = -xkJ/mol(x>0),则x>53.0
查看答案和解析>>
科目: 来源: 题型:
下列各组物质的无色溶液,不用其他试剂即可鉴别的是
①KOH、Na2SO4、AlCl3 ②NaHCO3、Ba(OH)2、H2SO4
③HCl、NaAlO2、NaHSO4 ④Ca(OH)2、Na2CO3、BaCl2
A.①② B.②③ C.①③④ D.①②④
查看答案和解析>>
科目: 来源: 题型:
有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是
A.氧化剂与还原剂的物质的量之比为1:8
B.该过程说明Fe( NO3)2溶液不宜加酸酸化
C.若有l mol NO3-发生氧化反应,则转移8mol e-
D.若把该反应设计为原电池,则负极反应为Fe2+-e-=Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com