
科目: 来源: 题型:
惰性电极电解NaCl溶液或CuSO4溶液都得到三种产物A、B、C,各物质之间的转化关系如下图所示(图中参与反应和生成的水都已略去)。已知甲是短周期元素的单质,它是日常生活中常用的包装材料。
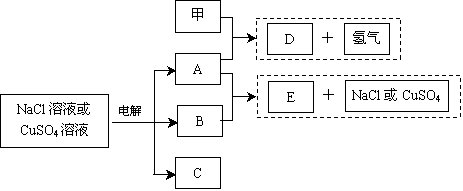
回答下列问题:
⑴若电解的是NaCl溶液:
①甲与A反应的化学方程式是 。
②A与B反应的离子方程式是 。
③若电解100mL0.1 mol·L-1NaCl溶液,阴、阳两极各产生112mL气体(标准状况),则所得溶液的pH为 (忽略反应前后溶液的体积变化及气体溶于水的影响)。
⑵若电解的是CuSO4溶液:
①E的化学式是 ;电解时阳极的电极反应式是 。
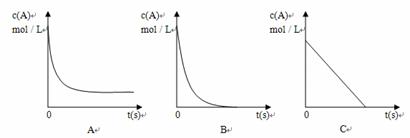
②加热时,A的浓溶液可与B发生反应,A的浓度随时间变化的图像正确是 。
查看答案和解析>>
科目: 来源: 题型:
某校化学小组学生利用下图所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均已略去)

⑴装置B中发生反应的化学方程式是 。
⑵装置E中的现象是 。
⑶停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。将滤液分成两份,分别检验滤液中的金属阳离子。检验Fe3+所用试剂为 ,检验Fe2+所用试剂为 。
![]() ⑷该小组学生利用上述滤液制取FeCl3·6H2O晶体,设计流程如下:
⑷该小组学生利用上述滤液制取FeCl3·6H2O晶体,设计流程如下:
①步骤一中通入足量Cl2发生反应的离子方程式为 。
②步骤二从FeCl3稀溶液中得到FeCl3·6H2O晶体的主要操作如下(均在HCl气氛中进行):
蒸发、浓缩 → 冷却、结晶 → 过滤、洗涤、干燥
在蒸发皿中进行蒸发浓缩操作时,当_________________________时,应停止加热。此过程应保持盐酸过量的原因________________________________________(用离子方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
 铅蓄电池的工作原理为Pb + PbO2 + 4H+ + 2SO42- == 2PbSO4 + 2H2O。如下图所示,A为PbO2电极,B为Pb电极,E、F均为PbSO4电极。先闭合K1足够长时间后断开K1。下列有关说法中不正确的是 ( ) ( )
铅蓄电池的工作原理为Pb + PbO2 + 4H+ + 2SO42- == 2PbSO4 + 2H2O。如下图所示,A为PbO2电极,B为Pb电极,E、F均为PbSO4电极。先闭合K1足够长时间后断开K1。下列有关说法中不正确的是 ( ) ( )
A.1mol Pb和1mol PbO2具有的总能量大于2mol PbSO4具有的总能量
B.若将两U形管中的溶液混合,混合液的质量分数仍为30%
C.两U型管均可单独作为原电池使用,正极分别为A和F
D.若再单独闭合K2,电极A、B的质量会逐渐增加,电极E、F的质量会逐渐减小
查看答案和解析>>
科目: 来源: 题型:
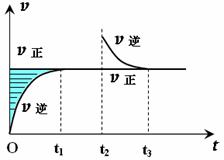 某恒温密闭容器发生可逆反应Z(?)+W(?)
某恒温密闭容器发生可逆反应Z(?)+W(?)![]() X(g)+Y(?) ΔH ,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中不正确的是 ( )
X(g)+Y(?) ΔH ,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中不正确的是 ( )
A.Z和W在该条件下一定不为气态
B.t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均
摩尔质量不可能相等
(※是命题者原创题,难度较大,本选项由于命题者未考 虑周全作了修改,否则无答案。)
C.若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2
时间段与t3时刻后的X浓度相等
D.若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大
查看答案和解析>>
科目: 来源: 题型:
己知:NH3•H2O (aq)与H2SO4 (aq)反应生成1mol正盐的△H= —24.2 kJ·mol-1;强酸、强碱的稀溶液反应的中和热的△H= —57.3 kJ·mol-1。则NH3•H2O在水溶液中电离的△H等于 ( )
A.-69.4 kJ·mol-1 B.-45.2 kJ·mol-1 C.+69.4 kJ·mol-1 D.+45.2 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式书写不正确的是 ( )
A.AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+)=7:2时,
2Al3+ + 7OH- = Al(OH)3↓+ AlO2- + 2H2O
B.Cl2与FeBr2溶液反应,当n(Cl2):n(FeBr2)=1:1时,
2Fe2+ + 4Br- +3Cl2 = 2 Fe3+ + 2Br2 + 6Cl-
C.CuCl2溶液与NaHS溶液反应,当n(CuCl2):n(NaHS)=1:2时
Cu2++2HS-= CuS↓+2H2S↑
D.Fe与稀硝酸反应,当n(Fe):n(HNO3)=1:2时,
3 Fe +2NO3- +8H+ = 3 Fe2+ +2NO↑+4H2O
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z都是短周期元素,X原子的最外层只有1个电子,Y原子的M层电子数只有K层与L层电子数之和的一半,Z原子的L层电子数比Y原子的L层电子数少2,且Y元素可有2种正价,两种正价的差值为2。由X、Y、Z三种元素组成的化合物的化学式可能是 ( )
①X2YZ3 ②XYZ3 ③XYZ4 ④X2YZ4 ⑤X3YZ3 ⑥X3YZ4
A.①②③ B.④⑤⑥ C.②⑤⑥ D.①③⑤
查看答案和解析>>
科目: 来源: 题型:
有下列两种转化途径,某些反应条件和产物已省略,下列有关说法不正确的是
![]()
![]() 途径①
途径①
途径②
A.途径①反应中体现了浓HNO3的强氧化性和酸性
B.途径②的第二步反应在实际生产中可以通过增大O2浓度来降低成本
C.由途径①和②分别制取1 mol H2SO4,理论上各消耗1 mol S,各转移6 mol e-
D.途径②与途径①相比更能体现“绿色化学”的理念是因为途径②比途径①污染相对小且原子利用率高
查看答案和解析>>
科目: 来源: 题型:
在某晶体中,与某一个微粒x距离最近且等距离的另一个微
 粒y所围成的空间构型为正八面体形(如图)。该晶体不是( )
粒y所围成的空间构型为正八面体形(如图)。该晶体不是( )
A.NaCl(x=Na+,y=Cl-)
B.CsCl(x=Cs +,y= Cl +)
C.金属钋(Po)
D.C60晶体
查看答案和解析>>
科目: 来源: 题型:
化学键
Si—O
O=O
Si—Si
键能/kJ·mol-1
X
498.8
176
有关键能数据如表:
晶体硅的燃烧热为989.2kJ·mol-1,则X的值为 ( )
A.423.3 B.460 C.832 D.920
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com