
科目: 来源: 题型:
一定温度下,lmol X和n mol Y在体积为2L的密闭容器中发生如下反应:
X(g)+Y(g)![]() 2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是
2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是
A.用X表示此反应的反应速率是(0.1—0.2a)mol·(L·min)-1
B.向平衡后的体系中加入lmol M,平衡向逆反应方向移动
C.当混合气体的质量不再发生变化时,说明反应达到平衡状态
D.向上述平衡体系中再充入lmol X,v(正)增大,v(逆)减小,平衡正向移动
查看答案和解析>>
科目: 来源: 题型:
今有室温下四种溶液,有关叙述不正确的是
① | ② | ③ | ④ | |
pH | 11 | 11 | 3 | 3 |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
A.分别加水稀释10倍,四种溶液的pH ①>②>④>③
B.①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
C.①、④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D.VaL④与VbL②溶液混合后,若混合后溶液pH=4,则Va ∶Vb= 11∶9
查看答案和解析>>
科目: 来源: 题型:
镁燃料电池以镁合金作为电池的一极,另一极充入过氧化氢,电解质溶液是酸化的氯化钠溶液,放电时总反应:Mg+2H++H2O2= Mg2++2H2O。关于该电池说法正确的是
A.放电时H+在正极反应得电子
B.正极方程式为:H2O2+2e-=2OH-
C.镁合金为电源负极,发生氧化反应
D.放电时正极的pH降低
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是
A.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率
B.含1molBa(OH)2的稀溶液和含1molH2SO4的稀溶液反应释放热量aKJ,则表示该反应中和热的热化学反应方程式为:OH-(aq)+H+(aq)=H2O(l);△H=-aKJ/mol
C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室
D.电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小
查看答案和解析>>
科目: 来源: 题型:
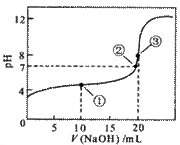 常温下,用0.1mol/L NaOH溶液滴定 20.00mL 0.1 mol/L CH3COOH溶液滴定曲线如右图。下列说法正确的是
常温下,用0.1mol/L NaOH溶液滴定 20.00mL 0.1 mol/L CH3COOH溶液滴定曲线如右图。下列说法正确的是
A. 点①所示溶液中:
c(CH3COO-)+ c(OH-) =c(CH3COOH)+ c(H+)
B. 点②所示溶液中:
c(Na+) =c(CH3COOH)+ c(CH3COO-)
C. 点③所示溶液中:
c(Na+)> c(OH-)> c(CH3COO-)> c(H+)
D. 滴定过程中可能出现:
c(CH3COOH)> c(CH3COO-)> c(H+)> c(Na+)> c(OH-)
查看答案和解析>>
科目: 来源: 题型:
下列说法中正确的是
A.d区元素外层电子排布式为ns1-2
B.电负性越大的元素的原子越容易获得电子
C.第一电离能越小的元素的原子越容易获得电子
D.若BeCl2是共价化合物,则可推知BeF2应为离子化合物
查看答案和解析>>
科目: 来源: 题型:
下列关于金属腐蚀叙述正确的是
A.金属在潮湿空气中腐蚀的实质是:M+nH2O===M(OH)n+![]() H2↑
H2↑
B.金属的化学腐蚀的实质是M-ne-===Mn+,电子直接转移给氧化剂
C.金属的化学腐蚀必须在酸性条件下进行
D.在潮湿的中性环境中,金属的电化学腐蚀主要是析氢腐蚀
查看答案和解析>>
科目: 来源: 题型:
中央电视台报道,一种名叫“排毒基强离子排毒仪”的产品正在市场热销。向排毒盆内倒入了纯净的温水,双脚放入盆中,启动电源开关,加入了适量精盐。过一段时间,盆中开始出现绿色、红褐色的絮状物。下列说法正确的是
A.绿色、红褐色的絮状物就是从脚底排出的体内毒素
B.加一些精盐的目的是起到消炎杀菌的作用
C.此“排毒基强离子排毒仪”一定是用惰性电极制成的
D.绿色、红褐色的絮状物分别是氢氧化亚铁和氢氧化铁
查看答案和解析>>
科目: 来源: 题型:
能促进水的电离,并使溶液中c(H+)>c(OH-)的操作是
①将水加热煮沸②向水中投入一小块金属钠③向水中通CO2④向水中加入NH4C1固体
⑤向水中加入NaHCO3固体⑥向水中加入NaHSO4固体
A.①②⑤ B.①④ C.③④⑥ D.④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com