
1.保护环境已成为当前和未来全球性的重大课题之一,为了消除大气污染,有科学家提出利用太阳能促使燃料循环使用的构想,使一些燃烧产物重新变成燃料,下列物质中有可能合成的燃料是
A.CO2 B.CH3OH C.N2 D.H2O
2.下列物质中,属于电解质的是
A.蔗糖 B.饱和食盐水 C.盐酸 D.KOH
3.用聚光手电筒照射下列分散系,不能观察到丁达尔效应的是
A.KOH溶液 B.Fe(OH)3胶体 C.雾 D.鸡蛋清水溶液
4.下列变化过程需要吸收能量的是
A.2H2+O2===2H2O B.CaO+H2O===Ca(OH)2
C.Cl+Cl―→Cl2 D.H2―→H+H
5.下列物质只含有离子键的是
A.H2O B.CO2 C.Na2O D.NH4Cl
6.生活中的问题常涉及化学知识,下列过程不涉及化学变化的是
A.用食醋除去暖瓶内的水垢
B.用75%的乙醇溶液进行皮肤消毒
C.碘单质遇淀粉变蓝
D.鸡蛋白溶液中加入硫酸铵饱和溶液后析出白色沉淀
7.反应A(g)+3B(g)===2C(g)+D(g),在四种不同的情况下的反应速率分别为:
①v(A)=0.15 mol.(L.s)-1 ②v(B)=0.6 mol.(L.s)-1
③v(C)=0.3 mol.(L.s)-1 ④v(D)=0.3 mol.(L.s)-1
该反应进行最快的是
A.① B.② C.③ D.④
8.2H、13C、15N、18O、34S等常用作环境分析指示物,下列对它们的说法正确的是
A.34S原子核内的中子数为16 B.16O与18O互称同位素
C.13C和15N原子核内的质子数相差2 D.2H的核外电子数比1H多一个
9.下列关于乙醇的说法正确的是
A.难溶于水 B.是一种无色无味液体
C.能发生酯化反应 D.存在官能团叫羧基
10.以下化学方程式中水只作为氧化剂的是
A. B.
B.
C. D.
D.

11.下列对化学用语的理解正确的是

A.结构示意图 :表示碳原子

B.比例模型 :表示二氧化碳分子
 C.电子式 :表示羟基
C.电子式 :表示羟基
D.H++OH-=H2O:表示醋酸和氢氧化钠的反应
12.下列实验操作正确的是
A. |
B.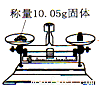 |
C.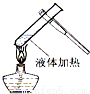 |
D.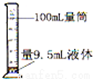 |
13.下列数值都是烃的相对分子质量,其对应的烃一定是烷烃的是
A.44 B.42 C.54 D.128
14.下列区分物质的方法不正确的是
A.用澄清石灰水区别SO2和CO2
B.用酸性KMnO4溶液区分苯和乙烯
C.用新制Cu(OH)2悬浊液区分蔗糖和葡萄糖
D.用加热的方式区别碳酸钠和碳酸氢钠
15. 关于如图所示装置的叙述,不正确的是( )
关于如图所示装置的叙述,不正确的是( )
A.铜片上有气泡产生 B.铜片质量逐渐减少
C.电子从锌片经导线流向铜 D.该装置把化学能转化为电能
16.下列关于SO2的叙述不正确的是
A.SO2的排放是形成酸雨的主要原因
B.SO2能使酸性高锰酸钾褪色是因为SO2具有漂白性。
C.实验室制备少量SO2可以用Na2SO3和浓硫酸加热制备
D.SO2的收集应采用向上排空气法
17.25℃时,PH=13的氨水溶液,下列说法不正确的是
A.溶液中C(OH-)=0.1
B.溶液中C(OH-) >C(H+)
C.该氨水的浓度为0.1
D.溶液中水的离子积为1×10-14
18.为了除去混入CO2中的SO2,最好将混合气体通入下列哪种溶液中
A.饱和小苏打溶液 B. 饱和烧碱溶液
C.饱和纯碱溶液 D.浓硫酸
19.糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质,以下叙述正确的是
A.植物油是高分子化合物
B.淀粉水解的最终产物是葡萄糖
C.葡萄糖能发生水解和氧化反应
D.蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水
20.下列措施不能增大反应速率的是
A.升高温度 B.使用合适的催化剂
C.提高反应物浓度 D. 降低温度
21.下列离子可以大量共存的是:
A.Mg2+ Na+ SO42- OH- B.Ca2+ K+ HCO3- OH-
C.Na+ H+ CH3COO- SO42- D.Ba2+ K+ NO3- Cl-
22.在25 ℃时,101KPa一定量的乙烯完全燃烧产生0.2mol液态水时放出热量akj,下列热化学方程式正确的是
A.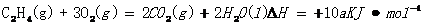
B.
C.
D.
23.下列关于有机物的说法不正确的是:
A.乙烯能使溴的CCl4溶液褪色是因为发生了加长反应
B.苯不能使溴的CCl4溶液褪色,说明苯分子中不存在碳碳双键
C.要除去乙酸乙酯中的少量乙酸可以加入少量乙醇和浓硫酸再加热
D.葡萄糖能与新制的氢氧化铜反应,说明葡萄糖是还原性糖
24.下列关于物质的相互关系正确的是
A. 与
与 互为同素异形体
互为同素异形体
B.金刚石与石墨互为同位素
C.二甲醚与乙醇互为同分异构体
D.乙烷与乙烯互为同系物
25.下列关于性质的比较不正确的是:
A.酸性 H2SO4>H3PO4
B.热稳定性 H2S>H2O
C.碱性 NaOH>Mg(OH)2
D.氧化性F2>O2
26.锂原子比镁原子少1个电子层,最外层电子数也比镁原子少1,在周期表中锂和镁的位置关系存在有“对角线”关系,“对角线”关系的元素性质存在相似性。下列关于锂的判断可能正确的是
A.Li能在空气中燃烧 B.Li2O只有共价键
C.Li2CO3能溶于水 D.LiOH受热不分解
27.某有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为1∶2,下列说法正确的是
A.分子中C、H、O个数之比为1∶2∶3 B.分子中C、H个数之比为1∶2
C.分子中可能含有氧原子 D.此有机物的最简式为CH4
28.下列方程式表达正确的是
A.铁与稀盐酸反应的离子方程式 :
B.Na与水反应的离子方程式:
C.FeCl3中加入统分的离子方程式:
D.醋酸的电离方程式:
29. 用NA表示阿伏伽德罗常数,下列说法不正确的是
A.常温常压下,16gO2 所含的原子数NA
B.标准状况下,2.24L水所含的电子书为10NA
C.2.4g金属镁与足量盐酸反应失去电子数0.2NA
D.1.6g甲烷含有共用电子对数目0.4NA
30.如图是某有机物分子的比例模型,有关该物质的推断不正确的是
 A.该物质可以与碳酸氢钠反应产生气体
A.该物质可以与碳酸氢钠反应产生气体
B.该物质可以发生酯化反应
C.此分子应该为某种氨基酸
D.该物质的分子式C3H6O3
试 卷 Ⅱ
31.(4分) (1)写出下列物质的化学式:①纯碱 ②天然气只要成分
(2)写出Cl2与水反应的化学方程式 。
32.(4分)乙烯是重要的化工原料,工业上常以乙烯为原料合成乙酸乙酯,也可以乙烯为原料来合成聚乙烯(简称PE),合成路线如下。

请回答下列问题:
(1)A的结构简式 。B中所含的官能团结构简式 。
(2) A+B→乙酸乙酯的化学方程式是 。
33.火箭推进器中用肼(N2H4)为燃料和氧化剂NO2,两者反应生成氮气和水蒸气。已知
N2(g) + 2O2(g)== 2NO2 (g) ΔH=+67.7kJ/mol, N2H4(g) + O2(g)== N2 (g) + 2H2O (g) ΔH=-534kJ/mol,
(1)请计算1mol气态肼和NO2完全反应放出的热量是 kJ。
(2)写出肼和NO2反应的热化学方程式: 。
34.(6分)下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
|
a |
|
|
|||||||||||||||
|
|
|
|
|
b |
c |
d |
e |
|
|||||||||
|
f |
g |
|
|
|
h |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1) 写出下列物质的电子式:元素d的最低价的氢化物
(2) 由元素a、d、f组成的化合物存在的化学键是 (A 离子键 B 共价键 C离子键和共价键) (填序号)
(3)由f的最高价氧化物的水化物和h的最高价氧化物的水化物反应的离子方程式是 。
35.如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中伤缺少的一种玻璃仪器是_____________;
(2)烧杯间填满碎纸条的作用是____________________;
(3)若大烧杯上不盖硬纸板,求得的反应热数值__________(填“偏大”“偏小”或“无影响”)。
(4)实验中该用60 mL 0.50 mol.L-1HCl跟50 mL 0.55 mol.L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量_________(填“相等”或“不相等”),所求中和热__________(填“相等”或“不相等”)。
36.(4分) 工业上生产的纯碱常含有少量的NaCl。现将11.77g工业纯碱溶于水中得到溶液,再加入足量稀盐酸,收集到2.24L(标准状况下测定)反应结束溶液的总体积为200mL。
(1)求反应后所得溶液中氯化钠浓度C(NaCl)=  ;
;
(2)求化合物中Na2CO3的质量= 。