
1.形成节约能源和保护生态环境的产业结构是人类与自然和谐发展的重要保证,你认为下列行为中有悖于这一保证的是
A.开发太阳能、水能、风能等新能源,减少使用煤、石油等化石燃料
B.研究采煤、采油新技术,提高产量以满足工业生产的快速发展
C.在农村推广使用沼气
D.减少资源消耗、增加资源的重复使用和资源的循环再生
2.对于温度与反应方向的关系,下列判断不正确的是
A.ΔH<0,ΔS>0,所有温度下反应自发进行
B.ΔH>0,ΔS>0,所有温度下反应自发进行
C.ΔH<0,ΔS<0,低温下反应自发进行
D.ΔH>0,ΔS<0,所有温度下反应不能自发进行
3.下列反应属于吸热反应的是
A.石灰石在高温下的分解反应 B.生石灰和水的反应
C.盐酸与氢氧化钠溶液的反应 D.木炭在氧气中燃烧
4.下列化合物中,在水溶液里和熔融状态下均不能导电的是
A、氯化钠 B、酒精 C、硫酸 D、氢氧化钠
5.下列过程需要通电才能进行的是
①电离 ②电镀 ③电解 ④电化学腐蚀
A.①② B.②③ C.③④ D.全部
6. 原电池的正极和电解池的阴极所发生的反应分别是
A.氧化、还原 B.还原、氧化
C.氧化、氧化 D.还原、还原
7.下列说法正确的是:
A.强电解质的导电能力一定大于弱电解质的导电能力
B.溶于水能导电的化合物都是电解质
C.25℃时,0.1mol/L的盐酸中氢离子浓度大于0.1mol/L的醋酸中氢离子浓度
D.BaSO4属于强电解质,所以其水溶液导电能力很强
8.一定温度下,对于反应N2+O2 2NO在密闭容器中进行,下列措施能增大反应速率的是
2NO在密闭容器中进行,下列措施能增大反应速率的是
A.降低温度 B.恒容充入氮气 C.恒压充入氦气 D.恒容充入氦气
9.下列有关钢铁腐蚀与防护的说法正确的是
A. 钢铁发生析氢腐蚀时,负极反应是Fe-3e-===Fe3+
B. 钢铁发生吸氧腐蚀时,正极反应是2H2O+O2+4e-===4OH-
C. 钢管与电源正极连接时,钢管可被保护
D. 在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀
10.1g碳与适量水蒸气反应生成CO和H2,需吸收10.94KJ热量,此反应的热化学方程式为
A.C + H2O == CO + H2 ; ΔH== +131.3KJ.mol-1
B. C(s)+ H2O(g) == CO(g) + H2(g) ; ΔH== +131.3KJ.mol-1
C. C(s)+ H2O(l) == CO(g) + H2(g) ; ΔH== +131.3KJ.mol-1
D. C(s)+ H2O(g) == CO(g) + H2(g) ; ΔH== +10.94KJ.mol-1
11.下列关于溶液酸碱性的说法中,正确的是
A.c(H+ )很小的溶液一定呈碱性
B.pH=7的溶液一定呈中性
C.c(OH- )=c(H+ )的溶液一定呈中性
D.不能使酚酞溶液变红的溶液一定呈酸性
12.反应N2+3H2 2NH3 ,开始时N2的浓度为3 mol.L-1,
2NH3 ,开始时N2的浓度为3 mol.L-1,
H2的浓度为5mol.L-1,3 min后测得NH3浓度为0.6 mol.L-1,则此时间内,下列反应速率表示正确的是
A.v(NH3)=0.2 mol.L-1.s-1 B.v(N2)=1.0mol.L-1.min-1
C.v(H2)=0.3 mol.L-1.min-1 D.v(H2)=1.67 mol.L-1.min-1
13.下列电离方程式书写正确的是
A.CH3COOH CH3COO-+H+
B.NaHCO3
CH3COO-+H+
B.NaHCO3 Na++H++CO32-
Na++H++CO32-
C.H2CO3 2H++CO32-
D.H2SO4=2H++SO42-
2H++CO32-
D.H2SO4=2H++SO42-
14.100℃时,NaCl溶液中c(H+)=1×10-6 mol/L。下列说法中正确的是
A.该NaCl溶液显酸性 B.该NaCl溶液显碱性
C.该NaCl溶液中KW=c(H+).c(OH-)=1×10-14
D.该NaCl溶液中KW=c(H+).c(OH-)=1×10-12
15.化学反应中的能量变化通常表现为热量的变化,下列图示能表示Ba(OH)2.8H2O与NH4Cl的反应过程中能量变化的是

16.在2A+B = 3C+4D反应中,表示该反应速率最快的是
A.V(A)=0.5 mol.(L.s)-1 B. V(B)=0.3 mol.(L.s)-1
C.V(C)=0.8 mol.(L.s)-1 D.V(D)=1 mol.(L.s)-1
17.微型钮扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2OH--2e-===ZnO+H2O;Ag2O+H2O+2e-===2Ag+2OH根据上述反应式,判断下列叙述中正确的是
A.在使用过程中,电池负极区溶液的碱性增强
B.使用过程中,电子由Ag2O极经外电路流向Zn极
C.Zn是负极,Ag2O是正极
D.Zn电极发生还原反应,Ag2O电极发生氧化反应
18.在一定温度下,向aL密闭容器中加入1molX气体和2molY气体,发生如下反应:X(g) + 2Y(g)  2Z(g) 此反应达到平衡的标志是
2Z(g) 此反应达到平衡的标志是
A.正反应和逆反应的速率都为零
B.容器内各物质的浓度不随时间变化
C.容器内X、Y、Z的浓度之比为1∶2∶2
D.单位时间消耗0.1molX同时生成0.2molZ
19.在密闭容器中发生如下反应:xA(g)+yB(g)  zC(g),达到平衡后测得A的浓度为0.20mol/L。在恒温下增大压强使容器容积缩小为原来的一半,再次达到平衡时,测得A的浓度为0.35mol/L。下列说法不正确的是
zC(g),达到平衡后测得A的浓度为0.20mol/L。在恒温下增大压强使容器容积缩小为原来的一半,再次达到平衡时,测得A的浓度为0.35mol/L。下列说法不正确的是
A、x+y﹥z B、平衡向右移动 C、B的转化率提高 D、C的体积分数降低
20.将c(H+)=10-2mol・L-1的醋酸和盐酸分别稀释100倍,稀释后两种溶液的
c(H+)分别为a和b,则a和b的关系为
A.a>b B.a<b C.a=b D.无法判断
21.某温度下,浓度都为1 mol.L-1的两种气体X2和Y2在密闭容器中反应生成气体Z,经过一段时间后c(X2)为0.4 mol.L-1, c(Y2)为0.8 mol.L-1,c(Z)为0.4 mol.L-1,则反应为
A.X2+2Y2 2XY2 B.2X2+Y2
2XY2 B.2X2+Y2 2X2Y
2X2Y
C.3X2+Y2 2X3Y
D.X2+3Y2
2X3Y
D.X2+3Y2 2XY3
2XY3
22.已知某可逆反应aA(g) +
bB(g)  cC(g) + dD(g)。反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如图。下列叙述正确的是
cC(g) + dD(g)。反应过程中,当其它条件不变时,C的体积分数与温度(T)和压强(P)的关系如图。下列叙述正确的是

A.正反应为吸热反应 B.降低温度,正反应速率增大
C.a + b < c + d D.增大压强,B转化率增大
23.在100mLH2SO4和CuSO4的混合液中,用石墨做电极电解,两极上均收集到2.24L气体(标准状况下),则原混合液中,Cu2+的物质的量浓度为
A.1mol・L-1 B.2mol・L-1 C.3mol・L-1 D.4mol・L-1
24.(6分)一定温度下在某定容容器中发生反应:2A(g) +3B(g) ===2C(g),开始时,A的浓度为3 mol.L -1,B的浓度是5 mol.L-1 ,2 min后,B的浓度减少1.2 mol.L-1 ,则
(1)v(C) = 。
(2)在2min末,A的浓度是 ____________。
25.(15分)下图是一个化学过程的示意图。已知甲池的总反应式为:
2CH3OH+3O2+4KOH 2K2CO3+6H2O
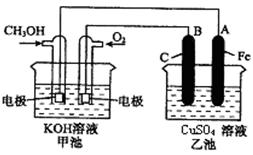
⑴甲池是 装置,通入CH3OH的电极名称是 ,
B电极的名称是 。
⑵通O2一极的电极反应式为 ,
⑶乙池中B极的电极反应式为 。
⑷当乙池中A(Fe)极的质量增加6.4g时,甲池中消耗O2 mL(标况下)
26.(15分)在2 L密闭容器内,800 ℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
|
时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
|
n(NO)(mol) |
0.020 |
0.011 |
0.008 |
0.007 |
0.007 |
0.007 |
(1)写出该反应的平衡常数表达式:K= 。
(2)如图中表示NO2的变化的曲线是 。
(3)能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆 (NO)=2v正 (O2) d.容器内密度保持不变
(4)某同学查阅资料得知,该反应 >
> ;25 ℃时,生成1 mol NO2,热量变化为56.4 kJ。但是该同学由于疏忽,忘记注明“+”、“-”。根据题目信息,该反应的热化学方程式为
。
;25 ℃时,生成1 mol NO2,热量变化为56.4 kJ。但是该同学由于疏忽,忘记注明“+”、“-”。根据题目信息,该反应的热化学方程式为
。
(5)为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
27.(8分)下表是某兴趣小组通过实验获得的相同体积足量稀硫酸与铁反应的实验数据:
|
实验序号 |
金属质量/g |
金属状态 |
c(H2SO4) mol/L |
实验温度/℃ |
金属消失的时间/s |
|
|
1 |
0.10 |
丝 |
0.7 |
20 |
250 |
|
|
2 |
0.10 |
丝 |
1.0 |
20 |
200 |
|
|
3 |
0.10 |
粉末 |
1.0 |
20 |
125 |
|
|
4 |
0.10 |
粉末 |
1.0 |
30 |
50 |
分析上述数据,回答下列问题:
(1)反应的离子方程式: 。
(2)①实验1、2可得出的结论是 ;
②实验2、3可得出的结论是 ;
③实验3、4可得出的结论是 。