
1.下说法错误的是( )
A.二氧化碳是温室气体,但不是大气污染物
B.农村常用明矾净水,是利用了胶体的性质
C.食品添加剂对人体无害,可大量食用
D.氯化钠是常用的防腐剂
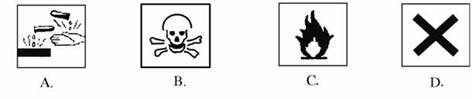
2.盛放浓硫酸的试剂瓶的标签上应印有下列警示标记中的是( )
3. 下列物质所属类别正确的是( )
|
|
氧化物 |
酸 |
碱 |
盐 |
|
A |
CuO |
HCl |
NH3.H2O |
Na2SO4 |
|
B |
CO2 |
CH3COOH |
火碱 |
Cu(OH)2 |
|
C |
H2O |
HBr |
纯碱 |
BaSO3 |
|
D |
MnO2 |
HClO |
生石灰 |
CaCO3 |
4.下列物质中属于非电解质的是( )
A.NaOH B.O2 C.Na2CO3 D.乙醇
5.下列关于(强、弱)电解质和非电解质的叙述中,错误的是( )
A.酸、碱、盐都是电解质
B.蔗糖、酒精是非电解质
C.盐酸是强电解质[]
D.NH3的水溶液能导电,但NH3不是电解质
6.下列叙述与胶体的性质无关的是( )
A.同一支钢笔使用不同品牌墨水时,容易发生堵塞现象
B.当日光从窗隙射入暗室时,可观察到一束光线
C.向氢氧化铁与水形成的某分散系中插入正、负电极,通直流电一段时间后,一极附近颜色变深
D.向氯化铁溶液中加入氢氧化钠溶液,产生红褐色沉淀
7.比较1.0mol N2和1.0mol CO的下列物理量:①质量 ②分子总数 ③原子总数,其中相同的是( )
A. ① B. ①② C. ①②③ D. ②③
8.能正确表示下列化学反应的离子方程式是( )
A.氢氧化钡溶液与硫酸的反应OH- + H+ =H2O
B.澄清的石灰水与稀盐酸反应Ca(OH)2 + 2H+ = Ca2+ + 2H2O
C.铜片插入硝酸银溶液中Cu + Ag+ = Cu2+ + Ag
D.碳酸钙溶于稀盐酸中CaCO3 +2H+=Ca2+ +H2O+CO2↑
9.下列可以大量共存且溶液是无色的离子组是( )
A.H+、Na+、NO3-、Cu2+ B.Ba2+、Mg2+、Cl-、SO42-
C.H+、K+、OH-、NO3- D.NO3-、SO42-、K+、Mg2+
10.NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.23gNa变为Na+ 时失去的电子数为NA
B.18g水所含的电子数为NA
C.8g He所含的分子数为NA
D.16g O2与16g O3所含的分子数均是NA
11.配制一定物质的量浓度的NaOH溶液时,造成实验结果偏高的是( )
A.定容时观察液面仰视 B.定容时观察液面俯视 C.有少量NaOH溶液残留在烧杯中 D.容量瓶中原来有少量蒸馏水
12.今有0.1mol/LNa2SO4溶液300 mL,0.1mol/LMgSO4溶液200 mL和0.1mol/L Al2(SO4)3溶液100 mL,这三种溶液中硫酸根离子浓度之比是 ( )
A 1∶1∶1 B 3∶2∶2 C 3∶2∶3 D 1∶1∶3
13.现有100mLNaCl和Na2SO4的混合溶液。经测定含有0.1mol SO42-,Na+ 的物质的量浓度为5mol/L。则Cl-的物质的量浓度为( )
A 2mol/L B 3mol/L C 4mol/L D 5mol/L
14.已知n mol某气体的质量为a g,则b g该气体在标准状况下的体积(L)为( )
A. 22.4an/b B. 22.4b/an C. 22.4bn/a D. 22.4a/bn
第Ⅱ卷(非选择题共58分)
15.(10分)
(1)分离植物油和水的混合物的方法是(填操作名称) 。
(2)实验室常用加热KClO3和MnO2的混合物的方法制备氧气,写出其化学方程式:
;反应结束后,若要回收催化剂MnO2,需经历的步骤是:溶解→ → →干燥
(3)溶液和胶体的本质区别是 。
16.(10分)用98%的浓硫酸(其密度为1.84 g/cm3)配制100 mL 1.0 mol.L-1的稀硫酸,若实验仪器有:
A.100 mL量筒 B.托盘天平 C.玻璃棒 D.50 mL容量瓶
E.10 mL量筒 F.50 mL烧杯 G.100 mL容量瓶
(1)该浓硫酸的物质的量浓度为 mol/L;需量取浓硫酸的体积为 mL。
(2)实验时选用的仪器有(填序号A-G) ,要完成上述实验,除了上述仪器外,还必需 。
(3)配制过程中,下列情况会使配制结果偏高的是(填序号①-④)
① 定容时俯视刻度线观察液面
② 容量瓶使用时未干燥
③ 定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
④ 浓硫酸稀释后,未冷却就转移至容量瓶中,并立即完成定容
17.(10分)完成下列表格内容
|
实验操作 |
现象 |
离子方程式 |
|
向澄清石灰水中通入少量CO2气体 |
|
|
|
向硫酸溶液中投入少量Mg粉 |
|
|
|
向醋酸溶液中滴加NaOH溶液 |
无明显现象 |
|
18.(12分)用下列物质填空
A.冰水混合物 B.盐酸 C.稀硫酸 D.HCl E.Ba(OH)2
F.纯碱 G. Fe(OH)3胶体 H. CuSO4.5H2O I. C2H5OH J. NH3.H2O
(1)混合物有 ;强电解质有 ;非电解质有
(2)写出F在水中的电离方程式:
(3)写出C、E反应应的离子方程式:
(4)向G中逐滴加入C的现象是
19.(8分)现有标准状况下的CH4气体4.48L。
该气体的物质的量为 mol;该气体的质量为 g;该气体拥有的H原子数为 ;与该气体含有相同H原子数的NH3的物质的量为 mol。
20.现有100mL1.0mol/L的Na2SO4溶液,计算:
(1)所含Na2SO4的物质的量为多少摩尔?
(2)所含Na2SO4的质量为多少克?
若取出上述Na2SO4溶液10mL,加水稀释至100mL后。求:
(3)稀释后的溶液中含Na2SO4的物质的量为多少摩尔?
(4)稀释后的溶液中Na+ 的物质的量浓度为多少?