
1.硅是带来人类文明的重要元素之一,科学家也提出硅是“21世纪的能源”。这主要是由于硅及其化合物对社会发展所起的巨大促进作用。下列关于硅及其化合物的说法中错误的是:
A.水泥、陶瓷、玻璃是三大重要的硅酸盐产品
B.水玻璃是建筑行业经常使用的黏合剂
C.高纯度的硅被用于制作光导纤维
D.水晶、石英的主要成分是SiO2
2.当光束通过鸡蛋清水溶液时,从侧面观察到一条光亮的“通路”,说明鸡蛋清水溶液是:
A.溶液 B.胶体 C.悬浊液 D.乳浊液
3.下列说法不正确的是
A.钠和钾的合金可用于快中子反应堆作热交换剂
B.镁与铜、铝等金属形成的合金大量用于制造火箭、飞机、导弹
C.制作印刷电路板时,可用FeCl3溶液腐蚀Cu
D.氯气有毒,不能用于药物的合成
4.下列贮存化学试剂的方法错误的是:
A.新制的氯水保存在棕色细口瓶中,并放在阴凉处
B.金属钠保存在煤油中
C.FeSO4溶液存放在加少量铁粉的试剂瓶中
D.烧碱溶液置于带玻璃塞的磨口试剂瓶
5.已知:还原性I->Br-。现向含有NaBr和KI的混合溶液中,通入一定量氯气充分反应后,将溶液蒸干并灼烧所得物质,最后剩余的固体可能是:
A.NaCl和KI B.NaCl和I2 C.KCl和NaBr D.KCl和I2
6.下列关于同浓度Na2CO3和NaHCO3溶液性质的说法中,正确的是:
A.常温时在水中的溶解性:NaHCO3>Na2CO3
B.热稳定性:NaHCO3<Na2CO3
C.与酸反应产生气泡的快慢:NaHCO3<Na2CO3
D.Na2CO3不能转化成NaHCO3,而NaHCO3能转化成Na2CO3
7.用MnO2和浓盐酸制取氯气,当4mol氯化氢被氧化时,生成的氯气的体积(标况)是
A.22.4L B. 44.8L C.67.2L D.89.6L
8.下列离子方程式书写正确的是:
A.Fe与FeCl3溶液反应:Fe+ Fe3+= 2 Fe2+
B.碳酸钙溶于稀盐酸:CO32- + 2H+ = H2O + CO2↑
C.FeSO4溶液和NaOH溶液反应: Fe2+ + 2OH- = Fe(OH)2↓
D.氯气溶于水:Cl2 + H2O = 2H+ + ClO- + Cl-
9.以下物质检验的方法、现象和结论,其中错误的是:
A.某盐溶液中加入氯水,再加入KSCN溶液,溶液出现血红色,则原溶液中含有Fe2+
B.某盐加入浓的氢氧化钠溶液并加热,能产生使润湿红色石蕊试纸变蓝的气体,则该盐是铵盐
C.常温下高锰酸钾和浓盐酸反应所产生的气体能使湿润的淀粉碘化钾试纸变蓝,该气体是Cl2
D.用洁净的铂丝蘸取某溶液,置于火焰上灼烧,能观察到火焰呈现黄色,则该溶液中一定含有钠离子,还可能含有钾离子
10.下列有关工业生产的叙述中错误的是:
A.工业上常以海带或其它海产品为原料提取碘
B.炼铁和制玻璃的工业中都要用到石灰石
C.氯气通入石灰乳中制漂白粉
D.电解氯化钠溶液制金属钠
11.设NA代表阿伏加德罗常数的数值,下列说法正确的是:
A.标准状况下,22.4 L水所含分子数目为NA
B.常温常压下,23 g NO2和23 g N2O4所含原子数目均为1.5NA
C.标准状况下,22.4 L氦气(He)与22.4 L氟气(F2)所含原子数均为2NA
D.18g D2O所含电子数目为10NA
12.下列物质中不能用化合的方法制得的是:
①SiO2 ②H2SiO3 ③Na2O2 ④FeCl2 ⑤FeCl3 ⑥CaSiO3
A.② B.②④⑥ C.①③⑤ D.②和④
13.把Fe粉、Cu粉置于FeCl3溶液中,充分反应后加入KSCN不显红色,下列情况不能成立的是:
A.铁不剩余,Cu剩余 B.铜不剩余、铁剩余
C.铁、铜均剩余 D.铁、铜均不剩余
14.现有硫酸钠、石灰石、二氧化硅三种白色固体,只用一种试剂将它们鉴别开来,这种试剂是
A.盐酸 B.氢氧化钠溶液 C.氯化钡溶液 D.碳酸钠溶液
15.下列实验操作中错误的是
A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.蒸发时,应使混合物中的水分完全蒸干后,才能停止加热
D.过滤时,要用蒸馏水浸没沉淀2-3次,以除去可能附着在沉淀上的杂质
16. C-NMR(核磁共振)可以用于含碳化合物的结构分析,
C-NMR(核磁共振)可以用于含碳化合物的结构分析, C表示的碳原子
C表示的碳原子
A.核外有13个电子
B.核内有6个质子,核外有7个电子
C.质量数为13,原子序数为6,核内有7个中子
D.质量数为13,原子序数为6,核内有7个质子
17.下列有关实验室制取气体的反应中,其原理不属于氧化还原反应的是:
A.实验室中用稀盐酸与石灰石反应制取CO2
B.实验室中用高锰酸钾加热分解制取 O2
C.实验室中用浓盐酸与二氧化锰加热制取Cl2
D.实验室中用稀硫酸与锌粒反应制取 H2
18.下列有关氯水的叙述,正确的是:
A.新制氯水只含有氯气和次氯酸分子
B.新制氯水可使紫色石蕊试液先变红后褪色
C.氯水光照时有气泡逸出,该气体的主要成分是氯气
D.氯水放置数天后,其pH增大
19.硫酸镁和硫酸铝溶液等体积混合后,铝离子浓度为0.1mol.L-1,硫酸根离子的浓度为0.3mol.L-1,则混合液中镁离子的浓度为
A.0.15mol.L-1 B.0.3mol.L-1 C.0.45mol.L-1 D.0.2mol.L-1
20.取含有 0.02 mol 的硫酸溶液, 先投入 0.24 g 镁粉, 再滴入 NaOH 溶液,当使溶液中的镁离子全部转化为沉淀时, 需要NaOH 的物质的量为
A.0.01 mol B. 0.02 mol C. 0.03 mol D. 0.04 mol
21.下列各组离子在水溶液中能大量共存的是
A.NH4+、Na+、Cl-、OH- B.Fe3+、H+、Cl-、CH3COO-
C.Fe3+、SCN-、K+、Cl- D.H+、Fe2+、SO42-、Cl-
22.将少量氯水加入KI溶液中振荡,再加入CCl4,振荡,静置后观察到的现象是
A.形成均匀的紫红色溶液 B.有紫色沉淀析出
C.液体分层、上层呈紫红色 D.液体分层、下层呈紫红色
23、下列装置能达到实验目的是:
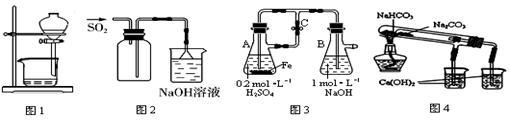
A.图1除去氯化钠溶液中的泥砂
B.图2用于实验室收集SO2
C.图3用于实验室制备Fe(OH)2
D.图4用于比较NaHCO3和Na2CO3热稳定性
24、向Fe和Fe2O3的混合物中加入足量的稀硫酸,充分反应后生成FeSO4溶液,当生成的Fe2+和H2的物质的量之比为5︰2时,则Fe和Fe2O3的物质的量之比为:
A.3︰1 B.1︰2 C.2︰1 D.1∶1
25.某溶液中可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Fe2+和Na+。某同学为了确定其组分,设计并完成了如下实验:
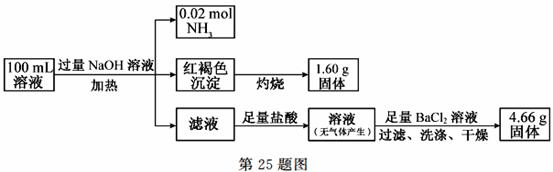
由此可推测原溶液中
A.NH4+、Na+、SO42- 一定存在,CO32- 一定不存在
B.NH4+、SO42- 一定存在, CO32-、Na+ 一定不存在
C.c(Cl-)至少为0.2 mol・L-l
D.c(Fe3+)一定为0.2 mol・L-l
26.(9分)
(1)NaOH的摩尔质量是 ,标准状况下112mLCO2的物质的量是 ,其质量是 ,
(2)质子数为8,中子数为10的核素可表示为 ,该核素的原子结构示意图为 。
(3)一水合氨的电离方程式为 。
(4)用双线桥表示下列反应的电子转移情况:Al2O3 + N2 + 3C = 2AlN + 3CO
27.(6分)下图为某工厂处理含Fe3+、Cu2+、Ag+废水的流程图

据图回答下列问题:
(1)操作①中所有反应的离子方程式为 。
(2)操作②中H2O2的作用可能是 。
(3)操作③中产生的沉淀为 (填化学式)。
(4)操作④中通入的X气体为 (填化学式)
28.(8分)一化学研究性学习小组对某Na2CO3和NaHCO3的混合溶液(以下简称“样品溶液”)的组成进行探究。取20.0 mL样品溶液不断滴入1.0 mol.L-1的稀盐酸,加入盐酸的体积和产生的现象见下表。
|
反应阶段 |
I |
II |
III |
|
盐酸体积x/ mL |
0<x≤10.0 |
10.0<x≤40.0 |
x>40.0 |
|
现 象 |
无气体 |
产生气体 |
无气体 |
|
解释 |
CO32- + H+ =
HCO3- |
|
|
回答下列有关问题:
(1)配制1.0 mol.L-1的稀盐酸250 mL,需要36.5%的浓盐酸 mL(36.5%的浓盐酸的密度约为1.2 g.cm-3);实验配制过程中所用的玻璃仪器除烧杯、玻璃棒和量筒外,还有 。
(2)第II阶段溶液中反应的离子方程式为: 。
样品溶液中c(CO32-)= mol.L-1。
29. (6分)海水中含有大量的氯化镁,从海水中提取镁的生产流程如图所示:
(6分)海水中含有大量的氯化镁,从海水中提取镁的生产流程如图所示:
试回答下列问题:
(1)操作①的名称是 。
操作②包括一系列操作:依次为 、 、过滤。
(2)加入试剂①时所发生反应的离子方程式为 。
(3)如果生成的Mg(OH)2中含有少量Ca(OH)2,可选用 加入除去。
30.(11分)无水FeCl3是一种重要的化学试剂,其熔点306℃沸点315℃,遇潮湿空气即产生大量白雾。某中学化学兴趣小组拟利用中学常见仪器设计实验制备无水FeCl3,实验装置如下图所示。
 请回答下列问题:
(1)制备实验开始时,先检查装置的气密性,检查装置A的气密性的方法是
。
(2)装置A中发生反应的离子方程式为
,其中被还原的物质是
。
请回答下列问题:
(1)制备实验开始时,先检查装置的气密性,检查装置A的气密性的方法是
。
(2)装置A中发生反应的离子方程式为
,其中被还原的物质是
。
(3)写出D装置中可能观察到的现象是 。 (4)装置B和F中的试剂分别是 、 。 (5)甲同学认为F和G可以用一种仪器替代,且加入一种药品即可达到相同效果。这种药品可以是 。 (6)为检验D中的产物是否部分进入到F集气瓶中,可采用进行如下实验:取F中溶液少许,加入适量蒸馏水稀释,然后向溶液中滴加(写名称) ,若观察到(现象) 则说明含有D中的生成物。该反应的离子方程式为 。
31.(4分)4.6g 金属钠投入到100 g 水中,所得溶液的密度为1g.mL-1。
(1)生成的气体在标准状况下的体积为 mL。
(2)列式计算所得溶液的物质的量浓度 。
32.(6分)现有一包铁粉和铜粉混合均匀的粉末样品,为确定其组成,某兴趣小组同学将不同质量的该样品分别与40 mL 1 mol/L的FeCl3溶液反应,实验结果如下表所示(忽略反应前后溶液体积的微小变化)。
|
实验序号 |
① |
② |
③ |
④ |
|
M(粉末样品)/g |
0.90 |
1.80 |
3.60 |
7.20 |
|
M(反应后剩余固体)/g |
0 |
0.64 |
2.48 |
6.08 |
(1)实验①反应后溶液中含有的金属阳离子有 。
(2)原粉末样品中m(Fe)∶m(Cu)= 。