金刚石
石墨
C60
碳纳米管
金刚石
石墨
C60
A.这四种物质都很软,皆可作润滑剂
B.这四种物质内部碳原子的排列方式都相同
C.这四种物质完全燃烧后的产物都是CO2
D.这四种物质的微观结构都是每个碳原子连接3个碳原子
20.某同学欲用实验证明铁、铜、汞、氢的化学活动性顺序,他利用了铁片、铜片、硝酸汞溶液和稀盐酸四种物质,设计了下列实验方案,其中可行的是( )
A.①Cu+HCl ②Fe+Hg(NO3) 2 ③Cu+Hg(NO3)2?
B.①Fe+HCl ②Cu+HCl
③Fe+Hg(NO3) 2?
C.①Fe+HCl ②Fe+Hg(NO3) 2 ③Cu+Hg(NO3) 2 ?
D.①Fe+HCl ②Cu+HCl
③Cu+Hg(NO3) 2?
21.欲将下列物质中所含杂质除去,所选用的试剂或方法正确的是( )
序号
物质
所含杂质
除去杂质的试剂或方法
①
O2
CO2
通过足量NaOH溶液
②
Zn
Cu
加入过量稀盐酸、过滤
③
NaCl
Na2CO3
加入适量稀盐酸、蒸发
④
CO2
CO
点燃混合气体
A.①② B.①③
C.②③ D.③④
第Ⅱ卷 非选择题(共90分)
化学部分
题号
一
二
三
总分
得分
可能用到的相对原子质量:H―1 O―16 S―32 Fe―56
一、填空与简答题(每空1分,共20分)
1.在下表空白处填上相应的化学符号或化学名称。
名称
1个硫酸根离子
+4价的碳元素
化学符号
NaHCO3
FeSO4
试题详情
2.沼气(主要成分甲烷)是当今已开发和使用的最洁净的气体燃料之一,使用沼气是解决农村能源不足及环境卫生问题的重要途径。
(1)写出甲烷完全燃烧的化学方程式
。
(2)沼气中除含有甲烷外,还含有二氧化碳及少量的氢气、氮气、硫化氢、一氧化碳、水蒸气等。沼气略带臭味,你认为臭味可能来自_______________气体。
(3)从安全方面考虑,使用沼气时一定要防止沼气中混入________________。
试题详情
3.河北三鹿集团由于在生产奶粉的过程中非法大量加入化工原料三聚氰胺,导致全国近三十万儿童患尿路结石。三聚氰胺又叫“蛋白精”,化学式为C3N6H6,其中氮元素的质量分数为 。
试题详情
4.请用所学的化学知识简要解释以下问题:?
(1)从分子观点解释:固体碘和碘蒸气遇到淀粉都变蓝色。
?
(2)观察盛水的铁锅,发现与水面接触的一圈最易生锈。
? ?
(3)可溶性钡盐如氯化钡是有毒的。碳酸钡本身难溶于水,但在食用后却会引起中毒,请解释原因(用化学方程式表示)。
? ?
试题详情
5.氨气(NH3)是一种无色有强烈刺激性气味的气体,为了探究氨气的其他性质,王兵同学按从左向右的顺序依次进行了如下实验:
试题详情
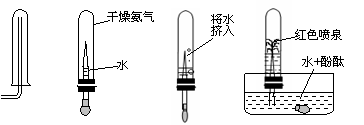
A
B
C
D
(1)通过实验,王兵同学可得出氨气的三点性质,分别是:① ;②
;③
;
(2)在操作A中,导气管要尽量接近试管底部,其目的是 。
试题详情
 6.右图为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线。试回答:
6.右图为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线。试回答:
(1)在温度为10℃时,碳酸钠的溶解度为
;
(2)当温度 时,氯化钠的溶解度大于碳酸钠的溶解度;
(3)生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”。请你解释“冬天捞碱”的原因:
。
试题详情
7.根据所含可溶性钙和镁的化合物多少,可将水分为硬水和软水,区分硬水和软水的方法是
。蒸馏水是典型的软水,请列举蒸馏水在实验室里的一种用途
。
试题详情
二、实验探究题(6分)
8.以下是某化学兴趣小组的同学对氢氧化钠溶液进行探究的过程。他们根据氢氧化钠溶液使无色酚酞试液变红的实验事实,想知道是溶液中的哪一种粒子使酚酞溶液变红了。
(1)猜想与假设:是溶液中的OH―使酚酞溶液变红了。
(2)查阅资料:NaOH溶液中存在着H2O、Na+、OH―等三种粒子。
(3)进行实验:
①在第一支干净的试管中加入2mL蒸馏水,再滴入几滴无色酚酞溶液,溶液几乎不变色,由此得到的结论是 ;
②在第二支干净的试管中加入2mL氯化钠溶液,再滴入几滴酚酞溶液,此时溶液仍然不变色,说明
;
(4)得出结论:原假设
(填“成立”、“不成立”)。
(5)反思与拓展:
在小组讨论时,小明同学认为以上的探究过程还可以进一步改进,使实验步骤更为简单,小明的改进要点是
,原理是
。
若在第三支干净的试管中加入2mL澄清的石灰水(氢氧化钙溶液),再滴入几滴酚酞溶液,出现的现象必定是
。
试题详情
三、计算题(共6分)
9.我市许多县区都盛产石灰石,小李同学为了寻找纯度超过85%的石灰石,便在课余时间对采集的一种样品进行了如下定量实验。
实验
步骤
①称取烧杯的质量
②将适量稀盐酸加入烧杯中并称重
③称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应
④待反应完全后,称重
实验
数据
试题详情
试题详情
试题详情
试题详情
烧杯和其中混合物的质量为107.6 g
试通过分析、计算:
(1)实验过程中生成的二氧化碳的质量是多少?
(2)该石灰石样品的纯度是否符合要求?(假设石灰石样品中的杂质不与稀盐酸反应也不溶于水)
2009年临沂市初中学生学业考试样卷
试题详情
选择题部分
每题2分,共60分。
题号
答案
题号
13
14
15
16
17
18
19
20
答案
B
C
D
C
A
C
C
D
题号
21
答案
B
非选择题部分
化学部分
一、填空与简答题(每空1分,共20分)
1.SO42- C 碳酸氢钠 硫酸亚铁
2.CH4+2O2 CO2+2H2O;硫化氢;空气(或氧气)
CO2+2H2O;硫化氢;空气(或氧气)
3.66.7%
4.(1) 固体碘和碘蒸气都是由相同的分子构成的;(2)该处的铁不仅与水接触,同时也与空气接触;(3)BaCO3+2HCl===BaCl2+CO2↑+H2O
5.(1)氨气(极)易溶于水;氨气的密度比空气小;氨气会和水发生化学反应,反应后的溶液显碱性;(2)收集到的气体更纯。
6.(1)10
g;(2)低于30℃;(3)冬天气温低,碳酸钠因溶解度减小而结晶析出。
7.加入肥皂水,产生泡沫多的是软水,泡沫少的是硬水;配制溶液。
二、实验探究题(6分)
8.H2O不能使酚酞溶液变红;Na+不能使酚酞溶液变红;成立;将实验①省略;实验②中氯化钠溶液不会使酚酞溶液变红,已经说明了H2O不能使酚酞溶液变色;变红色。
三、计算题(6分)
9.(1)根据质量守恒定律得:m(CO2)=(100.0 g+12.0 g)-107.6 g=4.4 g …(2分)
(2)设12.0 g石灰石样品中含CaCO3质量为x
CaCO3+2HCl===CaCl2+CO2↑+H2O …………………………………(1分)
100
44
x
4.4 g
x= =10.0 g ………
………………………………(1分)
=10.0 g ………
………………………………(1分)
 该石灰石样品的纯度为: 100%=83.3%(或83%) …………………(1分)
该石灰石样品的纯度为: 100%=83.3%(或83%) …………………(1分)
因83.3%<85%,所以该石灰石样品的纯度不符合要求。
……………………(1分)

 17.下列实验操作或装置正确的是( )
17.下列实验操作或装置正确的是( )