①
② ③ ④
⑤
⑥
A.②④⑤
B.②④⑥
C.①⑤⑥
D.②③⑤
试题详情
16.下列物质间的转化,不能由一步反应实现的是()
A.NaOH→NaCl B.Fe2O3→Fe(OH)3 C.HCl→CuCl2 D.CO2→CaCO3 试题详情
17.下列生活中的做法,正确的是() A.为了使银耳白净美观,用硫磺加以熏蒸 B.为了防止韭菜在生长过程中遭受病虫害,用剧毒农药进行灌根 C.为了补充维生素,可适量服用维生素制剂 D.为了使包裹粽子的粽叶颜色鲜绿,用硫酸铜溶液浸泡 试题详情
18.某工厂用质量分数为98%的浓硫酸(密度为1.84g/cm3)配制质量分数约为30%的稀硫酸供生产使用。配制时所用的浓硫酸与水的体积比最接近于()
A.1∶3
B.1∶4
C.1∶5
D.1∶6 试题详情
19.下列除杂质所选用试剂正确的是() A.用稀盐酸除去铜粉中的铁粉
B.用适量稀硫酸除去NaCl溶液中的Na2CO3 C.用浓硫酸吸收O2中的CO2气体 D.用稀盐酸除去Fe2O3中的CaCO3 试题详情
20.一定量的木炭在盛有氮气与氧气混合气体的密闭容器中充分燃烧后,生成CO和CO2,且测得反应后混合气体中碳元素的质量分数为24%,则其中氮气的质量分数可能为() A.10%
B.30%
C.50%
D.70% 第Ⅱ卷(非选择题 共60分) 试题详情
二、(本题包括4小题,共20分) 21.(6分)(1)写出下列物质的化学式: ①亚铁离子_____________________;②硫酸铝____________________。 (2)化学反应在从古至今的生产中都起着非常重要的作用。请按要求写出化学方程式: ①古代的湿法炼铜___________________________________________________; ②工业上用赤铁矿炼铁_______________________________________________。 试题详情
22.(4分)我们在初中化学里学过的一些物质,在实际生活中有重要的用途。现有以下4种物质:硝酸钾、稀硫酸、硫酸铜、干冰,请用它们(或其主要成分)的化学式填空。 (1)可用于配制杀菌剂波尔多液
_______________ (2)可用于除去铁锈
_______________ (3)可用于人工降雨
_______________ (4)可作为复合肥使用
_______________ 试题详情
23.(4分)将下列各名词填在与之相对应的空格中(只需填序号)。 ①乳化 ②结晶 ③潮解 ④挥发 (1)氢氧化钠固体露置在空气中,表面变潮湿
(2)打开装有浓盐酸的试剂瓶瓶塞,瓶口出现白雾 (3)将洗洁精洗去餐具上的油污
(4)冷却热的硝酸钾饱和溶液,出现晶体 试题详情
24.(6分)以下是一些常见物质间互相转化的关系图(有些反应条件未注明) 试题详情
(1)将固体A充分加热至不再产生气体,滤液H中所含有的物质有:
____________________________________________(写化学式) (2)固体B的化学式为______________,它在与无色液体E的反应中起____________作用。 (3)如果气体Z是最简单的有机物,它在气体X中燃烧,会因X的量的变化和条件的不同而生成不同的物质。试写出X和Z反应生成固体单质M和无色液体F的化学方程式: ______________________________________________________________。 试题详情
三、(本大题包括2小题,共10分) 25.(3分)中和反应是一类重要的化学反应,广泛应用于化学研究和工农业生产。中和反应过程中会放出热量。以下是在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸(常温下)的反应中,溶液温度变化的数据: 加入盐酸的体积 (V)/mL 2 4 6 8 10 12 14 16 18 20 溶液温度上升 (△t)/℃ 试题详情
试题详情
试题详情
试题详情
试题详情
试题详情
试题详情
试题详情
试题详情
试题详情
试题详情
 (1)试绘出溶液的温度变化(△t)与加入的盐酸体积(V)之间的关系曲线图: (1)试绘出溶液的温度变化(△t)与加入的盐酸体积(V)之间的关系曲线图: 试题详情
(2)请根据曲线变化的趋势,说明溶液温度变化的原因 试题详情
26.(7分)利用中和反应可以测定酸或碱溶液中溶质的质量分数。例如,在一定量的待测酸(或碱)溶液中逐滴加入已知质量分数的碱(或酸)溶液(标准溶液),直到酸、碱正好完全反应,根据消耗标准碱(或酸)溶液的多少即可求算出待测酸(或碱)溶液的质量分数。 右图为某次测定过程中,溶液的pH随所滴加的某标准溶液体积的变化而变化的关系图。 试题详情
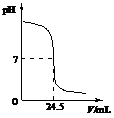 (1)根据右图曲线可以判断实验中是向_______(填“酸”或“碱”,下同) (1)根据右图曲线可以判断实验中是向_______(填“酸”或“碱”,下同)
溶液(待测液)中滴加__________溶液(标准液)。
(2)在这次测定中,为了指示中和反应刚好完全,用酚酞作指示剂,即在
待测溶液中先滴入几滴酚酞试液,若看到_______________________
_____________________________,则证明中和反应正好完成。 试题详情
(3)如果实验中使用的酸是硫酸,碱是氢氧化钠,且待测液和标准液的密度均以1.0g/mL计。若测定中取用待测液25mL,标准液溶质的质量分数为4.5%,根据图中数据,计算待测液溶质的质量分数。 试题详情
四、(本大题包括2小题,共22分) 27.(12分)燃烧是一种发光、发热的剧烈的化学反应。认识燃烧,科学地利用和控制燃烧,使燃烧为人类服务是十分重要的。 (1)物质燃烧一般需要同时满足三个条件,物质具有可燃性是燃烧的首要条件,下列物质中具有可燃性的是___________________(填物质的编号): ①石灰石 ②氮气 ③铁丝 ④红磷 ⑤面粉 ⑥二氧化碳 发生燃烧的另外两个条件分别是_____________________;______________________。 (2)下面是验证燃烧条件的实验装置图。 试题详情
①简要叙述检验该装置气密性的方法: _______________________________________________________________________________________ ______________________________________________________________________________________。 ②已知木炭是一种可燃物。请验证:木炭发生燃烧的另外两个条件中,缺少任何一个条件都不能燃烧(两个条件须分别验证),只有同时具备这两个条件才能燃烧。 在完成气密性检查后填装药品,并已设法在整个装置中充满了氮气。若要求实验过程中不得拆、装仪器,请设计后续的实验步骤,并按要求填表。
在后续实验步骤中,有一步骤为“盖灭酒精灯,待仪器恢复到常温”,请把这一步骤用“题示”两个字填入下表相应步骤的“操作”栏中,且不必填该步骤的“预计现象及得出的结论”栏。 步骤 操作 预计现象及得出的结论 ① ② ③ ④ (3)①有人建议在装置X处作下图Ⅰ所示的改动,以便可随时切断气流。这样的做法可能引起的不良后果是________________________________________________________________。 ②又有人建议在实验开始后,在Y管末端处增添一个燃着的酒精灯(下图Ⅱ),大家讨论后觉得很有必要,请用化学方程式说明理由(不需要文字说明): _________________________________________________________________________________。 试题详情
图Ⅱ 
试题详情
|
|
图Ⅰ 
试题详情
28.(10分)能源和环境是当今人类面临的两大问题。目前,化石燃料是人类生产、生活的主要能源。随着全球能源使用量的增长及不科学使用,化石燃料等不可再生能源将日益枯竭,并对环境产生严重影响。这就迫切要求人们开发氢能、太阳能等新能源。 试题详情
 (1)氢能来源广泛,是高能清洁能源。氢气除了可直接燃烧获得热量外,还可设计成燃料电池。目前使用氢能还面临着氢气的制取和氢气的储存两个问题。右图为模拟氢、氧燃料电池的实验装置。 (1)氢能来源广泛,是高能清洁能源。氢气除了可直接燃烧获得热量外,还可设计成燃料电池。目前使用氢能还面临着氢气的制取和氢气的储存两个问题。右图为模拟氢、氧燃料电池的实验装置。
X、Y均为纱布袋做成的容器,装有活性炭,并与内部的石墨棒紧密接触,导线与石墨连接(石墨和活性炭都能导电)。把X、Y浸在水中,并在水中加一些稀硫酸,以增强水的导电能力。 当电键K与b接通,发生反应的化学方程式为________________________________________。 通电一段时间内没有看到气泡逸出,是因为活性炭具有_________________________性,从而解决了气体储存的问题。此时将电键K与a接通,灯泡发光,说明能量发生了如下转化: 试题详情
  氢能 ________能 光能和热能。 氢能 ________能 光能和热能。
(2)一些常用燃料燃烧时的热值如下表: 燃料 天然气(以CH4计) 液化气(以C4H10计) 原煤(以C计) 热值(kJ/g) 约56 约50 约33
①目前不提倡直接用原煤作燃料的主要原因是: a__________________________________ ,b______________________________________。 ②化石燃料燃烧放出的CO2是一种温室气体,大量向空气中排放CO2将对气候产生负面影响。试通过计算说明,当上表中天然气和液化气充分燃烧获得相等的热量时,哪一种燃料放出的CO2较少? 五、(本题包括2小题,你只需选做其中一个小题,若两小题全做则以29题计分。共8分) 试题详情
29.(8分)地球上的淡水资源是十分有限的。人类生产、生活造成的水体污染加剧了水资源危机。常州市的水资源十分丰富,但作为常州明珠的?湖、长荡湖已受到不同程度污染。 (1)水体富营养化是我市水环境的主要问题之一。水体富营养化是指水体中含氮、磷的化合物过多,这些化合物是水生植物生长、发育的养料。 试题详情
  ①蛋白质是主要的含氮污染物,蛋白质在水中分解:蛋白质 氨基酸 氨(NH3),氨在微生物作用下,与溶解在水中的氧气反应,生成亚硝酸(HNO2)和水,反应的化学方程式为____________________________________________________,亚硝酸进一步在微生物作用下与氧气反应生成硝酸,并以硝酸盐的形式作为水生植物的养料。 ①蛋白质是主要的含氮污染物,蛋白质在水中分解:蛋白质 氨基酸 氨(NH3),氨在微生物作用下,与溶解在水中的氧气反应,生成亚硝酸(HNO2)和水,反应的化学方程式为____________________________________________________,亚硝酸进一步在微生物作用下与氧气反应生成硝酸,并以硝酸盐的形式作为水生植物的养料。
②含磷化合物主要来源于洗涤剂和不合理使用磷肥。洗涤剂中有一种成分的化学式为Na5PxOy,若P的化合价为+a,则a和x、y的关系是:a=___________。 ③白天受阳光照射,充足的养料使绿藻等水生植物迅速繁殖,水体变绿,光合作用的化学方程式是_________________________________________________。晚间由于污染物耗氧和水生植物的____________作用,使水中的含氧量急剧下降,会造成鱼类等水生动物因缺氧而死亡。另外,大量水生植物的残骸腐烂分解出有毒物质,使水质更加恶化。 (2)含酸、碱、重金属离子的工业废水也是重要的水体污染物。如果要处理某工厂产生的酸性污水,你建议用NaOH还是Ca(OH)2进行处理?为什么? _________________________________________________________________________________ ________________________________________________________________________________。 试题详情
30.(8分)小庄因母亲感冒发烧,从药房买了某种阿司匹林水溶片(内服的非处方药,含有可溶于水、具有酸的通性的固体酸),使用的过程中出现的一些现象使她产生了研究的兴趣。以下是小庄用剩余药品进行实验的记录: a.观察药片,为白色片状固体 b.将其放入水中,看到大量气泡,经检验产生的气体为A c.待充分反应后,过滤,得到白色固体与无色澄清滤液 d.把白色固体分成两份,一份加入试剂B,产生气泡;另一份加入某单质的棕黄色溶液C,生成蓝色物质 e.在滤液中加入过量试剂D,得到白色悬浊液,过滤,在过滤后得到的白色沉淀与滤液中分别滴加过量试剂B,均产生气体A,且白色沉淀全部溶解。 试根据小庄以上的实验记录,回答下列问题: (1)根据上述实验过程中的现象可以确定: ①b步骤中产生的气体A为
(填化学式,下同);e步骤中所用的试剂D为
。 ②该水溶片中肯定含有的物质种类有
(填序号); A.单质 B.氧化物 C.碱 D.盐 E.有机物 ③ 写出在e步骤中产生的白色沉淀中加试剂B的化学方程式:
。 (2)根据以上实验,小庄认为该药品成份中存在碳酸钡,你是否同意她的结论,为什么?______________________________________________________________________。 试题详情
| | | | | 
 N2↑+4H2O+Cl2↑+2O2↑,该反应属于()
N2↑+4H2O+Cl2↑+2O2↑,该反应属于()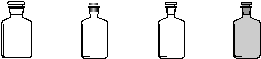
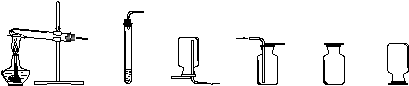 15.下列关于CO2气体的制取、收集、临时存放的实验装置中,正确的是()
15.下列关于CO2气体的制取、收集、临时存放的实验装置中,正确的是()