
2008ÄęÄţ˝ňÖеČѧУŐĐÉúÄŁÄ⿼ĘÔ
»Ż ѧ ĘÔ Ěâ
Ł¨Âú·Ö50·ÖŁ¬żĽĘÔʱĽä50·ÖÖÓŁ©
˵Ă÷Łş1.±ľľíą˛ÓĐ4´óĚ⣬11СĚ⡣ȫľíÂú·Ö50·ÖŁ¬żĽĘÔʱĽäÎŞ60·ÖÖÓ
2.±ľľíżÉÄÜÓõ˝µÄĎŕ¶ÔÔ×ÓÖĘÁżŁş H
µÚ˘ńľíŁ¨ŃˇÔńĚâ ą˛18·ÖŁ©
Ň»ˇ˘ŃˇÔńĚ⣨±ľ´óĚâ°üŔ¨9СĚ⣬ÿСĚâ2·Ö,ą˛18·ÖˇŁĂżĐˇĚâÓĐËĸöѡĎֻÓĐŇ»¸öѡĎî·űşĎĚâŇ⣩
1.ĎÂÁĐʵŃé˛Ů×÷ŐýČ·µÄĘÇ Ł¨ Ł©

A ˇˇB C D
2Ł®żĆѧĽŇ·˘ĎÖijЩÔ×ÓľßÓĐ·ĹÉäĐÔŁ¬Ľ´Ô×ÓÄÜ×Ô¶ŻµŘ·ĹÉäłöһЩąĚ¶¨µÄÁŁ×ÓŁ¬ľÝ´ËÍƶϣ¬µ±Ň»ÖÖÔŞËصÄÔ×Óľąý·ĹÉä±ä»ŻşóŁ¬˝áąű±äłÉÁËÁíŇ»ÖÖÔŞËصÄÔ×ÓˇŁËüŇ»¶¨ĘÇ·ĹÉäÁËŁ¨ Ł©
AŁ®¸ĂÔ×ÓµÄÔ×ÓşË BŁ®ÖĐ×Ó CŁ®µç×Ó DŁ®ÖĘ×Ó
3Ł®2008Äę±±ľ©°ÂÔË»áĎéÔĆ»đľćĘąÓõÄČĽÁĎĘDZűÍ飨C3H8Ł©,ĆäČĽÉյĻŻŃ§·˝łĚʽΪC3H8+5O2==xCO2+yH2O,ĆäÖĐxˇ˘y·Ö±đĘÇŁ¨ Ł©
A. 1
3
B.
4Ł®ĘµŃéĘŇÓĐËĸöŇ©Ć·ł÷Ł¬ŇŃ´ć·ĹČçĎÂŇ©Ć·Łş
ł÷
Ľ× ł÷
ŇŇ ł÷
±ű ł÷
¶ˇ ł÷
Ň© Ć·
ŃÎËᡢÁňËá
ÇâŃő»ŻÄơ˘ÇâŃő»Ż¸Ć
şěÁס˘Áň
͡˘Đż
ʵŃéĘŇĐÂąş˝řһЩ»îĐÔĚżŁ¬Ó¦˝«Ëü´ć·ĹÔÚ ( )
A. Ľ×ł÷ B. ŇŇł÷ C. ±űł÷ D. ¶ˇł÷
5Ł®ĘÔŔűÓĂŇŃѧąýµÄ»ŻŃ§ÖŞĘ¶Ŕ´Ĺжϣ¬´¦ŔíĎÂÁĐÍ»·˘ĘÂĽţ´ëĘ©˛»µ±µÄĘÇ( )
A. ĘŇÄÚ×Ĺ»đ±»Ŕ§Ł¬Á˘Ľ´ÓĂĘŞĂ«˝í¶ÂסżÚ±ÇŁ¬ŮéŮëÇ°˝řŁ¬Ń°ŐŇ°˛Č«łöżÚ
B. ¸ß˛ăס·ż×Ĺ»đŁ¬ÔڵȴýľČԮʱ´ňżŞËůÓĐĂĹ´°
C.·˘ĎÖÓĐČËĂşĆřÖжľŁ¬Á˘Ľ´´ňżŞĂĹ´°ˇ˘ąŘ±Ő·§ĂĹŁ¬˝«ÖжľČËԱתŇƵ˝żŐĆřÇĺеĵط˝
D. Îó·ţʳƷ´üÖеĸÉÔďĽÁŁ¨Ö÷ŇŞłÉ·ÖĘÇÉúĘŻ»ŇŁ©Ł¬Á˘Ľ´şČĘł´×
6Ł®ÎŢɫ͸Ă÷ĆŐͨ˛ŁÁ§Ł¬ĆäÖ÷ŇŞłÉ·ÖÓÖłĆÎŞÄƸƲŁÁ§Ł¨»ŻŃ§Ę˝ÎŞNa2CaSi6O14Ł©Ł¬ĆäÖĐąčÔŞËصĻŻşĎĽŰÎŞ Ł¨ Ł©
AŁ®+4ĽŰ BŁ®+3ĽŰ CŁ®+2ĽŰ DŁ®+1ĽŰ
7Ł®ĎÂÁĐĘÇһЩװÖĂĆřĂÜĐԵļě˛é·˝·¨Ł¬ĆäÖĐŐýČ·µÄĘÇ Ł¨ Ł©
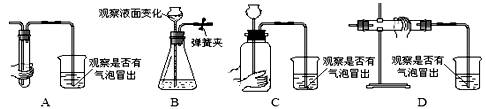
8Ł®ĘłĆ·ÎŔÉú°˛Č«ąŘϵµ˝Ç§ĽŇÍň»§ˇŁÓĂĽîĐÔČÜŇş˝ţĹÝĘ߲ˣ¬ÄÜÓĐЧłýČĄĘ߲ËÉϵIJĐÁôĹ©Ň©Ł¬´Ó¶ř˝µµÍ¶ÔČËĚĺµÄË𺦡ŁŃ§ĐŁĘłĚĂ´ÓĘĐłˇÉĎÂň»ŘŔ´µÄĘ߲ˣ¬ÄăČĎÎŞÓ¦˝ţĹÝÔÚ Ł¨ Ł©
AŁ®ĘłŃÎČÜŇş BŁ®ÉŐĽîČÜŇş CŁ®´żĽîČÜŇş DŁ®Ęł´×ČÜŇş
9. łŁÓĂČĽÉŐ·¨˛â¶¨ÓĐ»úÎďµÄ×éłÉˇŁĎÖȡ
AŁ®˘Ů˘Ú˘Ý BŁ®˘Ů˘Ü˘Ţ CŁ®˘Ů˘Ű˘Ý DŁ®˘Ů˘Ü˘Ý
µÚ˘ňľí Ł¨·ÇѡÔńĚâ ą˛32·ÖŁ©
¶ţˇ˘ĚîżŐÓëĽň´đĚ⣨±ľ´óĚâ°üŔ¨6СĚ⣬łýµÚ7СĚâÍ⣬»ŻŃ§·˝łĚĘ˝1·ÖŁ¬ĆäÓŕĂżżŐ0.5·ÖŁ¬ą˛1Łµ·ÖŁ©
1Ł®Ł¨2·ÖŁ©ĎÂÍĽĘÇČŐłŁÉú»îÖĐĘąÓõÄĚú¶¤Ł¬ÇëÓĂ»ŻŃ§·űşĹ±íĘľĎÂÁĐ´řµăµÄ˛ż·ÖŁş
Ł¨1Ł©Ěú¶¤ÖеÄÖ÷ŇŞłÉ·ÖĘÇ Ł»
Ł¨2Ł©Ěú¶¤ÔÚł±ĘŞµÄżŐĆřÖĐŇ×ÉúłÉŐýČýĽŰĚúµÄŃő»ŻÎĚúĐ⣩ Ł»
Ł¨3Ł©Ěú¶¤ÓëËá·´Ó¦¶ř˛úÉúŃÇĚúŔë×Ó Ł»
Ł¨4Ł©Čô˝«ÉúĐâµÄĚú¶¤·ĹČëϡÁňËáÖĐĆä±íĂćµÄĚúĐ⽫·´Ó¦ÉúłÉÁňËáĚú ˇŁ

2Ł®Ł¨2.5·ÖŁ©ĎÂÍĽĘÇĽŇÍĄľłŁĘąÓõÄŇ»ÖÖµçłŘĽ°×éłÉ¸ĂµçłŘµÄ¸÷ÖÖ˛ÄÁĎŁ¬ľÝÍĽ»Ř´đĎÂÁĐÎĘĚ⣺
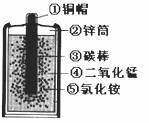
˘Ĺş¬ÓеÄŃő»ŻÎďĘÇŁ¨ĚѧʽŁ© Ł»ş¬ÓеÄŃÎĘÇ Ł¨Ěî±ŕşĹŁ©Ł»
˘ĆĚĽ°ôÔÚµçłŘÖеÄ×÷ÓĂĘÇ Ł»
˘ÇĐ´łöŇ»¸öµçłŘ˛ÄÁĎÖĐ˝đĘôÓëϡÁňËá·˘Éú·´Ó¦µÄ»ŻŃ§·˝łĚĘ˝ ˇŁ
ŁłŁ®Ł¨2·ÖŁ©ŇÔĎÂѡ×ÔijͬѧµÄһƪČŐĽÇŁş˝ńĚěÎŇČĄł¬ĘĐąşÎď·˘ĎÖŁ¬ÓĐЩʳƷ´üÖĐÓĐŇ»´üˇ°Ë«ÎüĽÁˇ±Ł¬ÓĐЩʳƷ´üÄÚ˛ÉÓĂÁËŐćżŐ°ü×°Ł¬¶řÓĐЩʳƷ´üŔďĂćČ´łäČëŇ»ÖÖĆřĚ塡Çë´ÓʳƷ°˛Č«ˇ˘ÎŔÉúĽ°ľĽĂµÄ·˝Ă濼ÂÇŁ¬»Ř´đĎÂÁĐÎĘĚ⣺
Ł¨1Ł©ˇ°Ë«ÎüĽÁˇ±ÄÜÎüĘŐʳƷ´üÖеÄO2şÍH2OŁ¬ŇÔ´ďµ˝·Ŕł±ˇ˘ŃÓł¤±ŁÖĘĆÚµÄÄżµÄˇŁĎÂÁĐÎďÖĘĘĘşĎ×öʳƷˇ°Ë«ÎüĽÁˇ±µÄĘÇŁ¨Ěî±ŕşĹŁ© ______ _Ł»
A.CaO B.Fe·Ű C.şěÁ× D.NaOHąĚĚĺ
Ł¨2Ł©ÇëÎŞłäĆř°ü×°µÄʳƷѡÔńŇ»ÖÖĚîłäĆřĚ壺 Ł¬ŔíÓÉĘÇ__________________Ł»
Ł¨3Ł©ĘÔ·ÖÎöŐćżŐ°ü×°ÄÜŃÓł¤ĘłĆ·±ŁÖĘĆÚµÄÔŇňĘÇ________________________________ˇŁ
Ł´Ł®Ł¨Ł˛·ÖŁ©
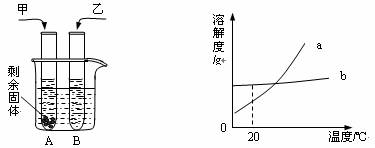
Ł¨1Ł©
Ł¨2Ł©ŇŞĘąAĘÔąÜÖĐĘŁÓŕµÄąĚĚĺĽĚĐřČܽ⣬żÉÍůÉŐ±ŔďµÄË®ÖĐĽÓČëŇ»ÖÖÎďÖĘŁ¬ÄăČĎÎŞŐâÖÖÎďÖĘżÉŇÔĘÇ ˇŁ
Ł¨3Ł©ÉĎÍĽÖбíĘľŇŇÎďÖʵÄČÜ˝â¶ČÇúĎßĘÇ Ł¨Ěaˇ±»ňˇ°bˇ±Ł©Ł»
Ł¨4Ł©´ÓşŁË®ÖĐ»ńµĂĘłŃεķ˝·¨ĘÇ________________
ŁµŁ®Ł¨Ł±·ÖŁ©ĎőËáŇřͨłŁÖü´ćÔÚ×ŘÉ«ĘÔĽÁĆżÖĐŁ¬ËüżÉŇÔ·˘ÉúČçĎ·´Ó¦Łş
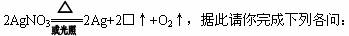
Ł¨1Ł©ˇőÖĐÎďÖʵĻŻŃ§Ę˝ĘÇ________Ł»
Ł¨2Ł©ĎőËáŇřͨłŁÖü´ćÔÚ×ŘÉ«ĘÔĽÁĆżÖеÄÔŇňĘÇ_______________________________ˇŁ
Ł¶Ł®Ł¨1.5·ÖŁ©ĎÂÍĽĘÇÄĆÔŞËء˘·úÔŞËŘÔÚÔŞËŘÖÜĆÚ±íÖеÄλÖĂŇÔĽ°ĎŕąŘÁŁ×ӽṹʾŇâÍĽŁ¬ÇëÍęłÉĎÂÁи÷ÎʡŁ
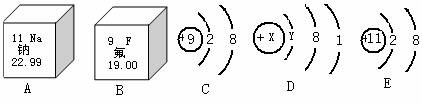
Ł¨1Ł©·úµÄÔ×ÓĐňĘýĘÇ_________Ł»
Ł¨2Ł©ČôDÎŞÄĆÔ×ӵĽṹʾŇâÍĽŁ¬ÔňXµÄÖµĘÇ_________Ł»
Ł¨3Ł©·ú»ŻÄƵĻŻŃ§Ę˝żÉ±íʾΪ_________ˇŁ
Ł·Ł®Ł¨4·ÖŁ©Ľ×ˇ˘Ňҡ˘±űĘÇłőÖĐ»ŻŃ§ÖĐłŁĽűµÄÎďÖĘŁ¬Ćäת»ŻąŘϵČçĎÂÍĽËůĘľŁş
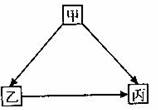
Ł¨1Ł©ČôĽ×ˇ˘ŇŇ×éłÉÔŞËŘĎŕͬŁ¬ÔňĽ×ÎŞŁ¨ĚѧʽŁ© Ł¬Đ´łöŇҡú±űµÄ»ŻŃ§·˝łĚĘ˝ Ł»
Ł¨2Ł©ČôŇҡ˘±ű×éłÉÔŞËŘĎŕͬŁ¬ÔňĽ×żÉÄÜĘÇ Ł»´ËʱĽ×ˇúŇҡ˘Ľ×ˇú±ű·˘ÉúµÄ»ŻŃ§·´Ó¦»ů±ľŔŕĐÍĘÇ ˇŁ
Čýˇ˘ĘµŃéĚ⣨±ľ´óĚ⹲2СĚ⣬ÿżŐ1·ÖŁ¬ą˛Łą·ÖŁ©
8Ł®Ł¨Łµ·ÖŁ©ÄłżÎÍâ»î¶ŻĐˇ×é´ÓʵŃé·ĎŇşÖĐ»ŘĘŐŇřŁ¬ľĽěŃéČ·¶¨ËůµĂŇř·ŰŃůĆ·ÖĐ»ąş¬ÓĐĚú·ŰŁ¬Đˇ×éłÉÔ±şÜżěÄⶨÁ˲ⶨŃůĆ·ÖĐŇřµÄÖĘÁż·ÖĘýµÄʵŃ鲽Ö裺
Aˇ˘ČˇÁ˝Ň©ł×ŃůĆ·ÓÚÉŐ±ÖĐŁ¬˛˘ĽÓČëĘĘÁżµÄÄłČÜŇşŁ¬˝Á°čŁ»
Bˇ˘´ýłä·Ö·´Ó¦şóŁ¨ÓĐĂ÷ĎÔµÄʵŃéĎÖĎóŁ¬ÄÜ׼ȷĹжϷ´Ó¦ĘÇ·ńÍęČ«Ł©Ł¬Čˇłö˛»ČÜÎ
Cˇ˘˛»ČÜÎďľĎ´µÓˇ˘¸ÉÔďşółĆÁżŁ¬˛˘ĽÇĎÂĆäÖĘÁżˇŁ
˘ĹĐ´łö˛˝ÖčAÖĐĽÓČëµÄÄłČÜŇşËů·˘Éú·´Ó¦µÄ»ŻŃ§·˝łĚĘ˝ˇŁ______________________ˇŁ
˘Ć˛˝ÖčBÖĐČçşÎĹжϷ´Ó¦ŇŃľÍęČ«Łż _____________________________ˇŁ
˘Ç˛˝ÖčBÖĐÖ÷ŇŞ˛Ů×÷µÄĂűłĆĘÇ____________Ł¬ĐčŇŞÓõ˝µÄŇÇĆ÷şÍÓĂĆ·ÓĐŁşĚúĽŲ̈Ł¨´řĚúȦŁ©ˇ˘ÉŐ±ˇ˘___________ˇ˘____________ˇ˘____________ˇŁ
˘Č¸ůľÝС×éłÉÔ±µÄÉčĽĆ˝řĐĐʵŃé,ÄÜ·ń´ďµ˝ĘµŃéÄżµÄŁżËµĂ÷ŔíÓɡŁ____________ˇŁ
9Ł®Ł¨4·ÖŁ©ČŐÇ°Ł¬ĘŔ˝ç»·±ŁÁŞĂË˝¨ŇéČ«Ăć˝űÖąÓĂÂČĆř¶ÔŇűÓĂË®Ďű¶ľŁ¬ÍĆąăĘąÓĂ°˛Č«ˇ˘¸ßЧɱľúĎű¶ľĽÁClO2ˇŁ˘ŮClO2ĘÇŇ»ÖÖ»ĆÂĚÉ«ˇ˘ÓĐ´ĚĽ¤ĐÔĆřζµÄĆřĚ壬˘ÚŔäČ´ÖÁ
Ł¨1Ł©¸ůľÝŇÔÉĎĐĹϢŁ¬ÇëÄă×Ü˝áłöClO2µÄÎďŔíĐÔÖĘ___________________ˇŁŁ¨ĚîĐňşĹŁ©Ł»
Ł¨2Ł©ÄżÇ°Ĺ·ÖŢһЩąúĽŇ˛ÉÓĂÂČËáÄĆŁ¨NaClO3Ł©ÓëŨŃÎËá·´Ó¦ÖĆȡClO2Ł¨Kestiog·¨Ł©Ł¬·´Ó¦µÄ»ŻŃ§·˝łĚʽΪŁş2NaClO3 + 4HCl = 2ClO2 + Cl2ˇü+ 2H2O + 2NaCl ÎŇąú×î˝üŃĐľżłÉą¦ÓĂÂČĆřşÍŃÇÂČËáÄĆŁ¨NaClO2Ł©·´Ó¦ÖĆȡClO2Ł¬¸Ă·´Ó¦µÄ»ŻŃ§·˝łĚʽΪCl2+2NaClO3=2ClO2+ 2NaClŁ¬´Ë·¨ÓëKestiog·¨Ďŕ±ČŁ¬ĆäÓŵăĘÇ___________________ˇŁ
Ł¨3Ł©ÄłĘµŃéС×éÓĂĎÂÍĽËůĘľ×°ÖĂĚ˝ľżÓĂł±Ę޵ÄKClO3Óë˛ÝËáÔÚ
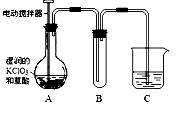
˘ŮÎŞÁËĘŐĽŻµ˝ŇşĚ¬ClO2Ł¬¶Ô×°ÖĂBÓ¦˛ÉȡµÄ´ëĘ©ĘÇ___________________ˇŁ
˘ÚÎŞ˝ĎşĂµŘ·ŔÖąClO2й©Ł¬CµÄÉŐ±ÖĐӦʢ·ĹµÄŇşĚĺĘÇ___________________ˇŁ
Ëġ˘ĽĆËăĚ⣺Ł¨±ľĚâ2СĚ⣬ą˛Ł¸·ÖŁ©
10.Ł¨3·ÖŁ© Ëć×ŵç×ӿƼĽË®Ć˝µÄ˝ř˛˝Ł¬Ňşľ§µçĘÓˇ˘µçÄÔˇ˘ŇDZíµČµç×Ó˛úĆ·ŇŃÖ𽥽řČëÎŇĂǵÄČŐłŁÉú»îˇŁMBBAĘÇŇ»ÖÖŃĐľż˝Ď¶ŕµÄŇşľ§˛ÄÁĎŁ¬Ć仯ѧʽΪC18H21NOŁ¬ÇëĽĆË㣺
Ł¨1Ł©Ň»¸öMBBA·Ö×ÓÖĐş¬ÓĐ ___________¸öÔ×ÓŁ»
Ł¨2Ł©MBBAµÄĎŕ¶Ô·Ö×ÓÖĘÁżĘÇ ___________Ł»
Ł¨3Ł©MBBAÖĐĚĽÔŞËصÄÖĘÁż·ÖĘýĘÇ ˇŁ
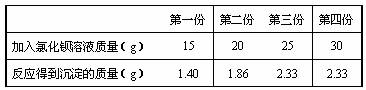
11Ł®Ł¨Łµ·ÖŁ©ÄłÖĐѧżÎÍâ»î¶ŻĐˇ×éÔڲⶨÓÉÂČ»ŻÄĆşÍÁňËáÄĆĐγɻěşĎÎďµÄ×éłÉʱŁ¬˝řĐĐÁËŇÔĎÂʵŃ飺ȡ
Ł¨1Ł©ľÝ±íżÉÍĆÖŞŁş±íÖĐµÚ ·ÝÖĐŁ¬BaCl2 ±»·´Ó¦Í꣬¶ř Na2SO4 ÓĐĘŁÓࡣ
Ł¨2Ł©Ô»ěşĎÎďÖĐÁňËáÄƵÄÖĘÁż·ÖĘýĘǶŕÉŮŁżŁ¨ľ«Č·µ˝ĐˇĘýµăşóһλŁ©
ąúĽĘѧУÓĹѡ - Á·Ď°˛áÁбí - ĘÔĚâÁбí
şţ±±Ęˇ»ĄÁŞÍřÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨Ć˝Ě¨ | ÍřÉĎÓĐş¦ĐĹϢľŮ±¨×¨Çř | µçĐĹթƾٱ¨×¨Çř | ÉćŔúĘ·ĐéÎŢÖ÷ŇĺÓĐş¦ĐĹϢľŮ±¨×¨Çř | ÉćĆóÇÖȨľŮ±¨×¨Çř
ÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨µç»°Łş027-86699610 ľŮ±¨ÓĘĎ䣺58377363@163.com