
2008年济南市高中阶段学校招生考试
理科综合化学部分
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分150分,考试时间120分钟。
相对原子质量:H l C l2 N 14 O 16 Na 23 Mg 24 S 32 Cl 35.5 K 39 Ca 40 Fe 56 Cu 64 I 127 Ba 137
第Ⅰ卷(选择题 共60分)
一、选择题(本大题包括30小题,每小题2分,共60分。每小题给出的四个选项中。只有一个选项最符合题目的要求)
7.下列过程中,没有发生化学变化的是 ( )
A.改良酸性土壤 B.积雪渐渐融化 C.粮食用来酿酒 D.食醋除去水垢
8.保护人类生存环境,人人有责。下列做法中,不合理的是 ( )
A.植物秸秆就地焚烧 B.植树种花,绿化环境
C.限制使用塑料方便袋 C.垃圾的分类处理、再生利用
9.下列示意图中,能表示阴离子的是 ( )
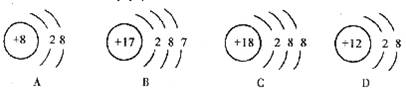
10.提高安全意识,是顺利完成化学实验的保障。下列说法中,不正确的是 ( )
A.烧碱溶液不慎沾到皮肤上,立即用大量水冲洗,然后再涂上硼酸溶液
B.洒出的少量酒精在桌面上燃烧起来,立即用湿抹布盖灭
C.稀释浓硫酸时将水注入盛浓硫酸的烧杯中
D.在实验室里制取氧气,先检查装置的气密性
11.下列有关生活、生产常识的说法中,正确的是 ( )
A.室内养花可防止煤气中毒 B.铵态氮肥可与碱性物质混用
C.适量吸烟有利于人体健康 D.儿童不能以呵可乐代替喝开水
12.生产加碘盐通常是在氯化钠中加入碘酸钾(KIO3)。为检验某食用盐样品中是否含有碘元素,某同学采用以下反应进行实验:KIO3+5KI+3H2SO4==3K2SO4+3H2 O+3X,则物质X的化学式为下列的 ( )
A.O2 B.H
13.有三瓶失去标签的无色溶液,只知道它们分别是稀盐酸、BaCl2溶液和NANO3溶液中的各一种。下列四种试剂中,能将上述三种无色溶液一次鉴别出来的是 ( )
A.NaCl溶液 B.稀硫酸 C.AgNO3溶液 D.Na2CO3溶液
14.下列叙述中,不正确的是 ( )
A.水通过状态变化,实现自身的天然循环
B.实验室电解水时,氢原子和氧原子的数目发生了改变
C.酸雨的形成与大量的二氧化硫气体向空气中排放有关
D.在水中氧元素的化合价为-2价
15.除去下列各组物质中的少量杂质,所用的试剂和方法中,不正确的是 ( )
物质
杂质
除杂质所用试剂和方法
A
FeSO4溶液
CuSO4
加入过量铁粉、过滤
B
NaOH溶液
Na2CO3
加入适量CaCl2溶液、过滤
C
NaNO3溶液
NaCl
加入适量AgNO3溶液、过滤
D
O2
水蒸气
通过盛浓硫酸的洗气瓶
16.下图表示M、N两种不含结晶水的固体物质的溶解度曲线。根据图示判断,下列说法中,正确的是 ( )
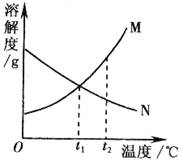
A. M、N的溶解度都随温度的升高而增大
B.将t
C.在t
D.将t
17.向含有AgNO3、Cu(NO3)2的混合溶液中加入一定量的铜粉。充分反应后过滤,则滤出的固体中,一定含有的金属是下列的 ( )
A Ag B.Cu C.Ag、Cu D.无法确定
18.将过量铁粉放入盛有
A.
38.(4分)选择C、H、O、Na四种元素中的适当元素,组成符合下列要求的物质,将其化学式填在空格中:
(1)一种金属单质______________;(2)一种可燃的氧化物______________:
(3)一种可溶的盐______________;(4)一种可溶的碱______________。
39.(3分)“鸟巢”――作为2008年北京奥运会的主会场,气势宏大,建筑技术先进。它采用了特殊钢架结构和单层有机高分子ETFE薄膜材料,该薄膜材料为乙烯四氟乙烯共聚物,其化学组成可表示为 [ CH2CH2CF2CF2 ]n (n为正整数)。
试回答下列问题:

(1)该薄膜材料中,共含有__________种元素。
(2)该薄膜材料中,碳、氢两元素的质量之比为_________ (最简整数比)。
(3)2008年北京奥运会的三大理念为“绿色奥运”“科技奥运”“人文奥运”,清简述你对“绿色奥运”的理解:_______________________________________________________________。
40.(4分)古人云:“民以食为天”。人们一日二餐的主食多为淀粉类食品,如米饭、面包等。食物中的淀粉[(C6H10O5)。]在人体内不能直接被吸收利用,而是在淀粉酶和水的作用下转化为葡萄糖(C6H12O6).并溶解在血液里,提供营养和能量。
试根据题意回答下列问题:
(1)淀粉属于__________(填“无机物”或“有机物”)。
(2)葡萄糖分子中碳、氢、氧的原子个数之比为_________ (最简整数比);葡萄糖在人体内发生如下化学反应:C6H12O6+6O2==6CO2+6H2O,该反应的类型属于_________反应。
(3)欲检验某食物中是否含有淀粉,下列试剂中,最宜选用的是________ (填序号)。
A.石蕊试液 B.碳酸钠溶液 C.稀盐酸 D.碘水 E.氢氧化钠溶液
41.(5分)下面所示(如图)为常见气体制备、干燥和性质实验的部分仪器。试根据题目要求,回答下列问题:

(1)欲在实验室中制备并收集干燥的二氧化碳气体。
①所选仪器的连接顺序为___________(填写仪器序号字母)。
②仪器A中,发生反应的化学方程式为______________________________。
(2)欲用一氧化碳气体测定某不纯氧化铁样品的纯度(杂质不反应),并验证反应中气体生成物的性质。所选仪器的连接顺序为:D→B→C。
①仪器B中看到的现象是______________________________________________。
②仪器C的作用是______________________________________________。
③通过测量反应前、后D处大玻璃管的质量变化,来计算氧化铁样品的纯度。若实验结束后大玻璃管中的物质里还有少许红色氧化铁。则计算出样品纯度的结果将____________ (填“偏大”“偏小”“不影响”其中之一)。
42.(4分)现欲探究一固体混合物A的成分,已知其中可能含有BaCl2、Na2CO3、NaCl、CuCl2,四种物质中的两种或多种。按图所示进行实验.出现的现象如图中所述(设过程中所有可能发生的反应都恰好完全进行)。
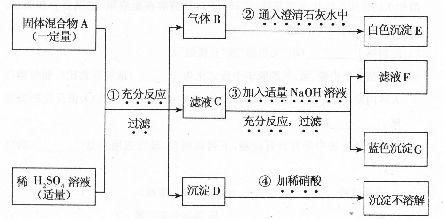
试根据实验过程和发生的现象做出判断,填写以下空白:
(1)沉淀D的颜色为____________。
(2)滤液F中大量存在的金属阳离子为(写离子符号) ______________________。
(3)混合物A中,肯定存在的物质是(写化学式) ______________________。
(4)写出实验过程③中生成沉淀G所发生反应的化学方程式:______________________。
43.(6分)在一烧杯中盛有一定质量的MgCO3固体,向其中滴加溶质的质精分数为10%的H2SO4溶液,至恰好完全反应。得到
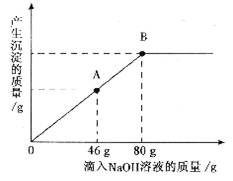
(1)在滴入稀硫酸时,观察到的明显实验现象是______________________________。
(2)当滴入NaOH溶液至图中A点时,烧杯中溶液里含有的溶质是(写化学式) ____________________________________________________________________________。
(3)当滴入10%的NaOH溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com