
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)

| ||
| ||
| ≤Ÿ◊˜≤Ω÷Ë | œ÷œÛ | Ω·¬€ |
»°…Ÿ¡øµƒ“∫Ô⁄ ‘πÐ÷–£¨œÚ∆‰÷–º”»Î…Ÿ¡ø∂˛—ıªØ√à »°…Ÿ¡øµƒ“∫Ô⁄ ‘πÐ÷–£¨œÚ∆‰÷–º”»Î…Ÿ¡ø∂˛—ıªØ√à |
»Ù∑¥”¶≤˙…˙∆¯≈ð »ÙŒÞœ÷œÛ »Ù∑¥”¶≤˙…˙∆¯≈ð »ÙŒÞœ÷œÛ |
∏√“∫ÃÂŒ™À´—ıÀÆ ∏√“∫ÃÂŒ™’Ù¡ÛÀÆ ∏√“∫ÃÂŒ™À´—ıÀÆ ∏√“∫ÃÂŒ™’Ù¡ÛÀÆ |
| µ—È≤Ÿ◊˜ | µ—Èœ÷œÛ | µ—ÈΩ·¬€ªÚ◊ÐΩ· | ||
| ∏˜≤Ω÷ËΩ·¬€ | ◊ÐΩ· | |||
| µ—È“ª | ‘⁄“ª÷ß ‘πÐ÷–µπ»Î“ª∂®¡øµƒπ˝—ıªØ«‚»Ð“∫£¨…ϻΥ¯ª–«µƒƒæÃı£¨ | ”–º´…Ÿ¡øµƒœ∏–°∆¯≈𣨃æÃı≤ª∏¥»º | π˝—ıªØ«‚»Ð“∫≥£Œ¬œ¬ƒÐ≤˙…˙º´…Ÿ¡øµƒ—ı∆¯ | ∫Ï◊©∑€ «π˝—ıªØ«‚∑÷Ω‚µƒ¥þªØº¡ |
| µ—È∂˛ | º”»Î…Ÿ¡ø∫Ï◊©∑€£¨…ϻΥ¯ª–«µƒƒæÃı£¨ | ƒæÃı∏¥»º | π˝—ıªØ«‚»Ð“∫∫Õ∫Ï◊©∑€ªÏ∫œƒÐ—∏ÀŸ≤˙…˙—ı∆¯£Æ | |
µ—È “≥£”√œ¬¡–◊∞÷√¿¥÷∆»°—ı∆¯£∫

(1)–¥≥ˆÕº÷–”–±Í∫≈“«∆˜µƒ√˚≥∆£∫a °¢b £ª
(2)”√À´—ıÀÆ∫Õ∂˛—ıªØ√ÿ¥÷∆»°—ı∆¯ ±£¨ø…—°”√µƒ∑¢…˙◊∞÷√ « (ÃÓ–Ú∫≈)£¨ ’ºØ∫√µƒ—ı∆¯
”¶ £®°∞’˝∑≈°±ªÚ°∞µπ∑≈°±£© µ—Èî…œ£¨–¥≥ˆ∏√∑¥”¶µƒ∑˚∫≈±Ì¥Ô Ω___________________
(3)ºÏ—È—ı∆¯ «∑Һج˙µƒ∑Ω∑® « °£
£®4£©ªØ—ß–À»§–°◊È‘⁄ µ—È “”√π˝—ıªØ«‚»Ð“∫∫Õ∂˛—ıªØ√Ã∑€ƒ©÷∆»°—ı∆¯£¨µ´∂‘¿œ ¶Ã·π©µƒ“ª∆ø±Í«©ƒ£∫˝µƒ°∞°ˆ°ˆÀÆ°±≤˙…˙¡À’˘“È£¨–°√˜»œŒ™ «’Ù¡ÛÀÆ£¨–°ª™»œŒ™ «À◊≥∆°∞À´—ıÀÆ°±µƒπ˝—ıªØ«‚»Ð“∫.«Îƒ„∞Ô÷˙À˚√«ºÏ—È∏√∆ø ‘º¡°£
| ≤Ÿ◊˜≤Ω÷Ë | œ÷œÛ | Ω·¬€ |
£®5£© –°ª™Õ¨—ߥ”◊ ¡œ…œø¥µΩ°∞∫Ï◊©∑€ø…◊˜Œ™π˝—ıªØ«‚»Ð“∫∑÷Ω‚∑¥”¶÷–µƒ¥þªØº¡°±£¨æÕ’‚“ª√¸Ã‚£¨À˝…˺∆≤¢ÕÍ≥…¡Àœ¬±ÌÀ˘ 浃ÃΩæø µ—È£∫
| µ—È≤Ÿ◊˜ | µ—Èœ÷œÛ | µ—ÈΩ·¬€ªÚ◊ÐΩ· | ||
| ∏˜≤Ω÷ËΩ·¬€ | ◊ÐΩ· | |||
| µ—È“ª | ‘⁄“ª÷ß ‘πÐ÷–µπ»Î“ª∂®¡øµƒπ˝—ıªØ«‚»Ð“∫£¨…ϻΥ¯ª–«µƒƒæÃı£¨ | ”–º´…Ÿ¡øµƒœ∏–°∆¯≈𣨃æÃı≤ª∏¥»º | π˝—ıªØ«‚»Ð“∫≥£Œ¬œ¬ƒÐ≤˙…˙º´…Ÿ¡øµƒ—ı∆¯ | ∫Ï◊©∑€ «π˝—ıªØ«‚∑÷Ω‚µƒ¥þªØº¡ |
| µ—È∂˛ | º”»Î…Ÿ¡ø∫Ï◊©∑€£¨…ϻΥ¯ª–«µƒƒæÃı£¨ | ƒæÃı∏¥»º | π˝—ıªØ«‚»Ð“∫∫Õ∫Ï◊©∑€ªÏ∫œƒÐ—∏ÀŸ≤˙…˙—ı∆¯°£ |
¢Ÿ ‘⁄–°ª™µƒÃΩæø µ—È÷–£¨ µ—È“ª∫Õ µ—È∂˛∆µƒ◊˜”√ « £ª
¢⁄ –°√˜Õ¨—ß»œŒ™Ωˆ”……œ ˆ µ—Ȫπ≤ªƒÐÕÍ»´µ√≥ˆ±Ìƒ⁄°∞◊ÐΩ·°±£¨À˚≤π≥‰…˺∆¡À¡Ω∏ˆ∑Ω√ʵƒ
ÃΩæø µ—È£¨◊Ó÷’ÕÍ≥…¡À∂‘°∞√¸Ã‚°±µƒ µ—È÷§√˜°£
µ⁄“ª∑Ω√ʵƒ µ—È≤Ÿ◊˜÷–∞¸∫¨¡À¡Ω¥Œ≥∆¡ø£¨∆‰ƒøµƒ «£∫ £ªµ⁄∂˛∑Ω√ʵƒ µ—È «–Ë“™÷§√˜ °£
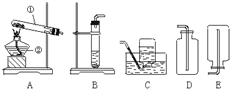 œ¬√Ê « µ—È “÷∆»°—ı∆¯µƒ◊∞÷√Õº£¨∏˘æð◊∞÷√Õºªÿ¥œ¬¡–Œ £∫
œ¬√Ê « µ—È “÷∆»°—ı∆¯µƒ◊∞÷√Õº£¨∏˘æð◊∞÷√Õºªÿ¥œ¬¡–Œ £∫
| ||
| °˜ |
| ||
| °˜ |
| ||
| ||
| µ—È≤Ω÷Ë | µ—Èœ÷œÛ | µ—ÈΩ·¬€ | |
| µ—È“ª | Ω´¥¯ª–«µƒƒæÃı…Ï»Î◊∞”–π˝—ıªØ«‚»Ð“∫µƒ ‘πÐ÷– Ω´¥¯ª–«µƒƒæÃı…Ï»Î◊∞”–π˝—ıªØ«‚»Ð“∫µƒ ‘πÐ÷– |
”–…Ÿ¡ø∆¯≈ð ƒæÃı≤ª∏¥»º |
≥£Œ¬œ¬π˝—ıªØ«‚»Ð“∫∑÷Ω‚ÀŸ¬ ∫Ь˝£Æ |
| µ—È∂˛ | ‘⁄◊∞”–π˝—ıªØ«‚»Ð“∫µƒ ‘πÐ÷–º”»Î…Ÿ¡øAl2O3£¨»ª∫ÛΩ´¥¯ª–«µƒƒæÃı…ϻΠ‘πÐ÷– | ≤˙…˙¥Û¡øµƒ∆¯≈ðƒæÃı∏¥»º | º”»ÎAl2O3ƒÐº”øÏπ˝—ıªØ«‚»Ð“∫µƒ∑÷Ω‚ÀŸ¬ º”»ÎAl2O3ƒÐº”øÏπ˝—ıªØ«‚»Ð“∫µƒ∑÷Ω‚ÀŸ¬ |
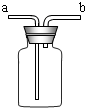
 œ¬√Ê « µ—È “÷∆»°—ı∆¯µƒ◊∞÷√Õº£¨∏˘æð◊∞÷√Õºªÿ¥œ¬¡–Œ £∫
œ¬√Ê « µ—È “÷∆»°—ı∆¯µƒ◊∞÷√Õº£¨∏˘æð◊∞÷√Õºªÿ¥œ¬¡–Œ £∫ ________πÐø⁄Õ®»Î∆ø÷–£ª¢€»ÙΩ´∆ø÷–◊∞»Î∞Î∆ø’Ù¡ÛÀÆø…”√”⁄≤°»À ‰ÀÕ◊∞÷√£¨________∂À¡¨Ω”÷¸—ı∆¯∏÷∆ø£¨‘⁄ ‰ÀÕµƒπ˝≥Ã÷–£¨’‚“ª◊∞÷√ƒÐ∆µΩµƒ◊˜”√ «________°¢________°¢________£Æ
________πÐø⁄Õ®»Î∆ø÷–£ª¢€»ÙΩ´∆ø÷–◊∞»Î∞Î∆ø’Ù¡ÛÀÆø…”√”⁄≤°»À ‰ÀÕ◊∞÷√£¨________∂À¡¨Ω”÷¸—ı∆¯∏÷∆ø£¨‘⁄ ‰ÀÕµƒπ˝≥Ã÷–£¨’‚“ª◊∞÷√ƒÐ∆µΩµƒ◊˜”√ «________°¢________°¢________£Æ| µ—È≤Ω÷Ë | µ—Èœ÷œÛ | µ—ÈΩ·¬€ | |
| µ—È“ª | ________ | ”–…Ÿ¡ø∆¯≈ð ƒæÃı≤ª∏¥»º | ≥£Œ¬œ¬π˝—ıªØ«‚»Ð“∫∑÷Ω‚ÀŸ¬ ∫Ь˝£Æ |
| µ—È∂˛ | ‘⁄◊∞”–π˝—ıªØ«‚»Ð“∫µƒ ‘πÐ÷–º”»Î…Ÿ¡øAl2O3£¨»ª∫ÛΩ´¥¯ª–«µƒƒæÃı…ϻΠ‘πÐ÷– | ≤˙…˙¥Û¡øµƒ∆¯≈ðƒæÃı∏¥»º | ________ |
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com