
ÌâÄżÁбí(°üÀšŽđ°žșÍœâÎö)
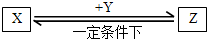
Łš1Ł©Ò»¶šÌőŒțÏÂÄłÌțÓëH2°ŽÎïÖÊ”ÄÁżÖź±È1:2ŒÓłÉÉúłÉ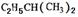 ŁŹÔòžĂÌț”ÄœáččŒòÊœÎȘ______________________________Ł»
ŁŹÔòžĂÌț”ÄœáččŒòÊœÎȘ______________________________Ł»
Łš2Ł©ÄłÓĐ»úÎïX·ÖŚÓÖĐÖ»șŹCĄąHĄąOÈęÖÖÔȘËŰŁŹÏà¶Ô·ÖŚÓÖÊÁżĐĄÓÚ110ŁŹÆäÖĐŃőÔȘËŰ”ÄÖÊÁż·ÖÊęÎȘ14.8%ŁŹÒŃÖȘžĂÎïÖÊżÉÓëFeCl3ÈÜÒș·ąÉúÏÔÉ«·ŽÓŠŁŹÔòX”Ä·ÖŚÓÊœÎȘ__________ĄŁ
Èô1 mol XÓëĆšäćËź·ŽÓŠÊ±ÏûșÄÁË3 mol Br2ŁŹÔòX”ÄœáččŒòÊœÎȘ____________________ĄŁ
Łš3Ł©·ÖŚÓÊœÎȘC4H8”ÄÌțŁŹșËŽĆčČŐńÇâÆŚÍŒÖĐÓĐÁœžöÎüÊշ棏·ćĂæ»ę±ÈÎȘ3:1ŁŹÇëĐŽłö·ûșÏÌőŒț”ÄËùÓĐÎïÖʔĜáččŒòÊœ
Łš4Ł©ÏÂÁĐÀšșĆÄÚÎȘÔÓÖÊŁŹœ«łęÈ„ÏÂÁĐžśŚé»ìșÏÎïÖĐÔÓÖÊËùĐè”ÄÊÔŒÁșÍ·œ·šÌîĐŽÔÚșáÏßÉÏĄŁ
ąÙ äćÒÒÍ飚ÒÒŽŒŁ©____________________________________________________________
ąÚ ±œ·ÓŁš±œŁ©______________________________________________________________________
ĐŽłöąÚČÙŚśÖĐÉ挰”œ”Ä·ŽÓŠ”Ä»ŻŃ§·œłÌÊœ________________________________________
Łš5Ł©ÒŃÖȘŁș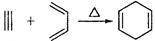 ŁŹÈçčûÒȘșÏłÉ
ŁŹÈçčûÒȘșÏłÉ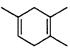 ËùÓĂ”ÄÔÊŒÔÁÏżÉÒÔÊÇŁš Ł©
ËùÓĂ”ÄÔÊŒÔÁÏżÉÒÔÊÇŁš Ł©
AŁź2-ŒŚ»ù-lŁŹ3-¶Ą¶țÏ©șÍ2-¶ĄÈČ BŁź2ŁŹ3-¶țŒŚ»ù-1ŁŹ3-Îì¶țÏ©șÍÒÒÈČ
CŁź2ŁŹ3-¶țŒŚ»ù-lŁŹ3-¶Ą¶țÏ©șͱûÈČ DŁź1ŁŹ3-Îì¶țÏ©șÍ2-¶ĄÈČ
 ŁŹÔòžĂÌț”ÄœáččŒòÊœÎȘ______________________________Ł»
ŁŹÔòžĂÌț”ÄœáččŒòÊœÎȘ______________________________Ł» ŁŹÈçčûÒȘșÏłÉ
ŁŹÈçčûÒȘșÏłÉ ËùÓĂ”ÄÔÊŒÔÁÏżÉÒÔÊÇŁš Ł©
ËùÓĂ”ÄÔÊŒÔÁÏżÉÒÔÊÇŁš Ł©| ÔȘËŰ | ĐÔÖÊ»òÔŚÓœáčč |
| A | ÔŚÓșËÄÚÖ»ÓĐÒ»žöÖÊŚÓ |
| B | ”„ÖÊÊÇżŐÆűÖĐșŹÁżŚî¶à”ÄÆűÌć |
| X | ԌӔČîÍâČă”çŚÓÊęÊÇŽÎÍâČă”çŚÓÊę”Ä3±¶ |
| Y | ¶ÌÖÜÆÚÔȘËŰÖĐÔŚÓ°ëŸ¶ŚîŽó”ÄÔȘËŰ |
| Z | ŚîžßŐ껯șÏŒÛÓëŚî”Ížș»Żșό۔ĎúÊęșÍÎȘ6 |
| ||
| Ąś |
| ||
| Ąś |
| Ê”ŃéČÙŚś | Ê”ŃéÏÖÏó | œáÂÛŒ°œâÊÍ |
| ąÙÈĄÉÙÁżNaBr ÈÜÒșÓÚÊÔčÜÖĐŁŹ”ÎŒÓ ÂÈËź ÂÈËź ŁŹŐń”ŽŁ»ąÚÔÙŒÓÈëÉÙÁżCCl4ŁŹŐń”ŽŁŹŸČÖĂŁź |
ąÙÈÜÒșÓÉÎȚÉ«±äÎȘłÈ»ÆÉ«Łź ąÚÈÜÒș·ÖČ㣏 ÉÏČăÒșÌćŒžșőÎȘÎȚÉ«ŁŹÏÂČăÒșÌćÎȘłÈșìÉ« ÉÏČăÒșÌćŒžșőÎȘÎȚÉ«ŁŹÏÂČăÒșÌćÎȘłÈșìÉ« Łź |
Ńő»ŻĐÔŁșZ ”„ÖÊŁŸBr2 ÀëŚÓ·œłÌÊœ Cl2+2Br-šT2Cl-+Br2 Cl2+2Br-šT2Cl-+Br2 |
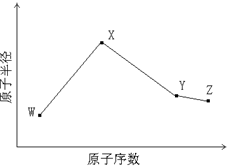 WĄąXĄąYĄąZÊÇËÄÖÖłŁŒû”ĶÌÖÜÆÚÔȘËŰŁŹÆäÔŚÓ°ëŸ¶ËæÔŚÓĐòÊę±ä»ŻÈçÏÂÍŒËùÊŸŁźÒŃÖȘW”ÄÒ»ÖÖșËËŰ”ÄÖÊÁżÊęÎȘ14ŁŹÖĐŚÓÊęÎȘ7Ł»X”ÄÀëŚÓÓëNH4+ŸßÓĐÏàÍŹ”ÄÖÊŚÓĄą”çŚÓÊęÄżŁ» WÓëY”ÄŃő»ŻÎïŸùÄÜ”ŒÖÂËáÓê”ÄĐγɣ»Z”Ä·ÇœđÊôĐÔÔÚÍŹÖÜÆÚÖśŚćÔȘËŰÖĐŚîÇżŁź
WĄąXĄąYĄąZÊÇËÄÖÖłŁŒû”ĶÌÖÜÆÚÔȘËŰŁŹÆäÔŚÓ°ëŸ¶ËæÔŚÓĐòÊę±ä»ŻÈçÏÂÍŒËùÊŸŁźÒŃÖȘW”ÄÒ»ÖÖșËËŰ”ÄÖÊÁżÊęÎȘ14ŁŹÖĐŚÓÊęÎȘ7Ł»X”ÄÀëŚÓÓëNH4+ŸßÓĐÏàÍŹ”ÄÖÊŚÓĄą”çŚÓÊęÄżŁ» WÓëY”ÄŃő»ŻÎïŸùÄÜ”ŒÖÂËáÓê”ÄĐγɣ»Z”Ä·ÇœđÊôĐÔÔÚÍŹÖÜÆÚÖśŚćÔȘËŰÖĐŚîÇżŁź| ʱŒä | Ćš¶ÈŁšmol/LŁ© | ||
| cŁšW2Ł© | cŁšBŁ© | cŁšAŁ© | |
| ”Ú0min | 4.0 | 9.0 | 0 |
| ”Ú10min | 3.8 | 8.4 | 0.4 |
| ”Ú20min | 3.4 | 7.2 | 1.2 |
| ”Ú30min | 3.4 | 7.2 | 1.2 |
| ”Ú40min | 3.6 | 7.8 | 0.8 |
čúŒÊѧУÓĆŃĄ - Á·Ï°ČáÁбí - ÊÔÌâÁбí
șț±±ÊĄ»„ÁȘÍű΄·šșÍČ»ÁŒĐĆÏąŸÙ±šÆœÌš | ÍűÉÏÓĐșŠĐĆÏąŸÙ±šŚšÇű | ”çĐĆŐ©ÆŸÙ±šŚšÇű | ÉæÀúÊ·ĐéÎȚÖśÒćÓĐșŠĐĆÏąŸÙ±šŚšÇű | ÉæÆóÇÖÈšŸÙ±šŚšÇű
΄·šșÍČ»ÁŒĐĆÏąŸÙ±š”ç»°Łș027-86699610 ŸÙ±šÓÊÏäŁș58377363@163.com