
题目列表(包括答案和解析)
下图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B原子的质量数。B原子核内质子数和中子数相等。下列叙述不正确的是( )
| A |
| C |
|
| B |
|
A、三种元素的原子半径的大小顺序是:B>C>A
B、A元素最高价氧化物对应的水化物具有强氧化性
C、B元素的氧化物、氢化物的水溶液都呈酸性
D、C元素是非金属性最强的元素
【解析】考查元素周期表的结构和元素周期律的应用。因为质子数和中子数之和是质量数,若A的原子序数是x,则B是x+9,C是x+2。根据题意可知x+x+2+x+9=2×(x+9),解得x=7,则A、B、C分别是N、S、F。同主族元素自上而下原子半径逐渐增大,非金属性逐渐减弱,金属性逐渐增强。同周期元素自左向右原子半径逐渐减小,非金属性逐渐增强,金属性逐渐减弱。A不正确,应该是B>A>C,硝酸是氧化性酸,B正确。硫酸和氢硫酸都属于酸,C正确。F是最强的非金属元素,D正确,所以答案是A。
下图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B原子的质量数。B原子核内质子数和中子数相等。下列叙述不正确的是( )
|
A |
|
C |
|
|
B |
|
A、三种元素的原子半径的大小顺序是:B>C>A
B、A元素最高价氧化物对应的水化物具有强氧化性
C、B元素的氧化物、氢化物的水溶液都呈酸性
D、C元素是非金属性最强的元素
【解析】考查元素周期表的结构和元素周期律的应用。因为质子数和中子数之和是质量数,若A的原子序数是x,则B是x+9,C是x+2。根据题意可知x+x+2+x+9=2×(x+9),解得x=7,则A、B、C分别是N、S、F。同主族元素自上而下原子半径逐渐增大,非金属性逐渐减弱,金属性逐渐增强。同周期元素自左向右原子半径逐渐减小,非金属性逐渐增强,金属性逐渐减弱。A不正确,应该是B>A>C,硝酸是氧化性酸,B正确。硫酸和氢硫酸都属于酸,C正确。F是最强的非金属元素,D正确,所以答案是A。
依题意可知:
![]()
含CuO(4.24 - 0.02×12)÷80=0.05 mol
若CuO全部被还原为Cu,其质量应为0.05×64=3.20g。
故反应后的混合物应由Cu和Cu2O组成,
其中Cu2O:(3.36-3.20)÷16=0.01 mol
Cu2O质量的分数为:
0.01×144÷3.36×100%=42.9%
Cu的质量分数为:1- 42.9%=57.1%</PGN0093B.TXT/PGN>
| ①先后加入沉淀剂A、B |
| ②过滤 |
| ③先后通入NH3CO2 |
| ④过滤 |
| ⑤煅烧 |

| 84n-53m |
| 31m |
| 84n-53m |
| 31m |
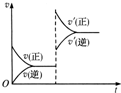 对达到平衡的可逆反应X+Y?W+Z,增大压强则正、逆反应速率(v)的变化如图,分析可知X,Y,Z,W的聚集状态可能是( )
对达到平衡的可逆反应X+Y?W+Z,增大压强则正、逆反应速率(v)的变化如图,分析可知X,Y,Z,W的聚集状态可能是( )| A、Z,W为气体,X,Y中之一为气体 | B、Z,W中之一为气体,X,Y为非气体 | C、X,Y,Z皆为气体,W为非气体 | D、X,Y为气体,Z,W中之一为气体 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com