
题目列表(包括答案和解析)
某同学用如下所示装置探究物质的性质。其中气体A的主要成分是氯气,还含有少量水蒸气。请回答下列问题:
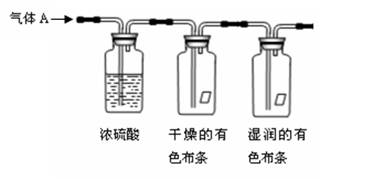
(1)该实验观察到的实验现象是 。
(2)浓硫酸的作用是 。
(3)该实验设计还存在事故隐患,因此还需增加 装置。
某同学为了探究氯化铵的性质,进行了如下实验,请你按要求回答下列问题。
(1)配制100mL1mol/L的NH4Cl溶液。该同学应用托盘天平称量NH4Cl固体的质量为 g。
有以下仪器:烧杯、胶头滴管、玻璃棒等玻璃仪器。
 ①还缺少的仪器有 ;
①还缺少的仪器有 ;
②使用容量瓶前必须进行的一步操作是 ;
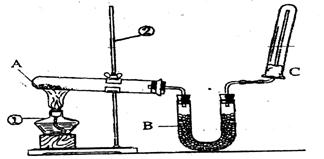
(2)该同学又用下图所示的装置做了有关氨气的性质实验。
①写出实验室制氨气的化学方程式: ;
②写出B中盛放的是碱石灰其作用是 ;
③氨气极易溶于水,在氨水中滴加酚酞现象是 ;
④检验氨气的方法是 。
Ⅱ.(6分)在稀硝酸中放入足量的铜片:
(1)反应的化学方程式为 ;
(2)待反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,其原因是 。(用离子方程式表示)
(3)若将12.8g铜跟一定量的浓硝酸反应,铜消耗完时,共产生气体5.6L(标
准状况下)。则所消耗的硝酸的物质的量是 。
Ⅰ.(8分)某同学为了探究氯化铵的性质,进行了如下实验,请你按要求回答下列问题。
(1)配制100mL1mol/L的NH4Cl溶液。该同学应用托盘天平称量NH4Cl固体的质量为 g。
有以下仪器:烧杯、胶头滴管、玻璃棒等玻璃仪器。
①还缺少的仪器有 ;
②使用容量瓶前必须进行的一步操作是 ;
(2)该同学又用下图所示的装置做了有关氨气的性质实验。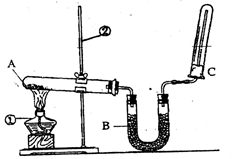
①写出实验室制氨气的化学方程式: ;
②写出B中盛放的是碱石灰其作用是 ;
③氨气极易溶于水,在氨水中滴加酚酞现象是 ;
④检验氨气的方法是 。
Ⅱ.(6分)在稀硝酸中放入足量的铜片:
(1)反应的化学方程式为 ;
(2)待反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,其原因是 。(用离子方程式表示)
(3)若将12.8g铜跟一定量的浓硝酸反应,铜消耗完时,共产生气体5.6L(标
准状况下)。则所消耗的硝酸的物质的量是 。
Ⅰ.(8分)某同学为了探究氯化铵的性质,进行了如下实验,请你按要求回答下列问题。
(1)配制100mL1mol/L的NH4Cl溶液。该同学应用托盘天平称量NH4Cl固体的质量为 g。
有以下仪器:烧杯、胶头滴管、玻璃棒等玻璃仪器。
①还缺少的仪器有 ;
②使用容量瓶前必须进行的一步操作是 ;
(2)该同学又用下图所示的装置做了有关氨气的性质实验。
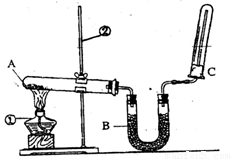
①写出实验室制氨气的化学方程式: ;
②写出B中盛放的是碱石灰其作用是 ;
③氨气极易溶于水,在氨水中滴加酚酞现象是 ;
④检验氨气的方法是 。
Ⅱ.(6分)在稀硝酸中放入足量的铜片:
(1)反应的化学方程式为 ;
(2)待反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,其原因是 。(用离子方程式表示)
(3)若将12.8g铜跟一定量的浓硝酸反应,铜消耗完时,共产生气体5.6L(标
准状况下)。则所消耗的硝酸的物质的量是 。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com