
题目列表(包括答案和解析)
(10分) 向氢氧化钠溶液中慢慢地通入二氧化硫气体,反应生成正盐,当继续通入过量二氧化硫时,正盐便转化成酸式盐。
⑴ 写出上述反应的化学方程式 ①
②
⑵ 标准状态下,向100 mL 2 mol/L的NaOH溶液中通入3 . 36 L二氧化硫气体,反应后溶液中溶质的成分为 。
⑶ 试计算,在标准状态下,100 mL 2 mol/L的NaOH溶液中最多可吸收多少体积二氧化硫气体?
(10分) 向氢氧化钠溶液中慢慢地通入二氧化硫气体,反应生成正盐,当继续通入过量二氧化硫时,正盐便转化成酸式盐。
⑴写出上述反应的化学方程式①
②
⑵标准状态下,向100mL2mol/L的NaOH溶液中通入3.36L二氧化硫气体,反应后溶液中溶质的成分为 。
⑶试计算,在标准状态下,100mL2mol/L的NaOH溶液中最多可吸收多少体积二氧化硫气体?
(10分) 向容积为2L的密闭容器中加入2 mol A、0.6 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图1所示。图2为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。
已知t3-t4阶段为使用催化剂;图1中t0-t1阶段c(B)未画出。
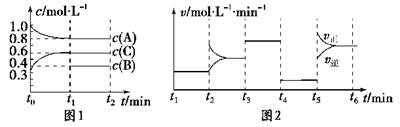
(1) 若t1=15 min,则t0-t1阶段以C浓度变化表示的反应速率为v(C)= 。
(2) t4-t5阶段改变的条件为 ,B的起始物质的量为 。各阶段平衡时对应的平衡常数如下表所示:
|
t1~t2 |
t2~t3 |
t3~t4 |
t4~t5 |
t5~t6 |
|
K1 |
K2 |
K3 |
K4 |
K5 |
则K1、K2、K3、K4、K5之间的关系为 (用“>”“<”或“=”连接)。
(3) 在相同条件下,若起始时容器中加入a mol A、b mol B和c mol C,达到平衡时体系中各物质的量与t1时刻相等,a、b、c要满足的条件为 。
(10分)向一个固定体积的密闭容器充入2 mol A和1 mol B,发生如下反应:
2A(g) + B(g)![]() 3C(g) + D(g),2分钟后,反应达到平衡,C的浓度为1.2 mol/L。
3C(g) + D(g),2分钟后,反应达到平衡,C的浓度为1.2 mol/L。
(1)用A表示2分钟内平均反应速率 ,A在第1分钟平均速率 第2分钟平均速率(填“<”、“>”、“=”)。
(2)器温度升高,平衡时混合气体的平均相对分子质量减小,则正反应为________(填“吸热”或“放热”)反应。
(3)大B的转化率,可采取的措施是_________(用序号填空)
①加入A ②加入B ③加压 ④再加入1.6 mol A+ 0.8 molB ⑤将C分离出容器
(4)体积可变,维持容器压强和温度不变,按下列方法加入起始物质,达到平衡时C的浓度仍为1.2 mol/L的是_________(用序号填空)
①4 mol A + 2 mol B ②3mol C + 1 mol D + l mol B
③3 mol C + 2 molD ④1.6 mol A+ 0.8 mol B + 0.6 mol C + 0.2 mol D
(10分)向含有0.8 mol的稀硝酸中慢慢加入22.4 g的铁粉,假设反应分为两个阶段。
第一阶段为:Fe+HNO3(稀)―→Fe(NO3)3+NO↑+H2O
(1)写出这两个阶段发生反应的离子方程式:
第一阶段: 。
第二阶段: 。
(2)正确表达这两个阶段反应中,加入铁粉的物质的量与溶液中铁元素存在的形式的关系
。
(3)在图中画出溶液中Fe2+、Fe3+、NO的物质的量随加入铁粉的物质的量变化的关系图象(横坐标为加入铁粉的物质的量,纵坐标是溶液中离子的物质的量)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com