
题目列表(包括答案和解析)
有一实验①如图所示,将30 mL 0.1 mol/L Ba(OH)2溶液置于烧杯中,然后边搅拌边慢慢加入0.1 mol/L某第3周期元素形成的某酸溶液共25 mL,加入酸溶液的体积V和电流强度I的I-V图如图②所示.
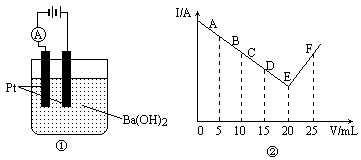
(1)此酸的化学式为________.
(2)处于C点时,溶液中导电的阳离子主要是________.
(3)处于F点时,溶液中导电的阴离子主要是________.
(4)烧杯中刚加入酸时,观察到的现象是________.
(5)图②中,从A→E电流强度I变小的主要原因是________.
有一实验如图a所示,将一定量的Ba(OH)2溶液置于烧杯中,然后边搅拌边慢慢加入溶质的质量分数一定的H3PO4溶液(一种三元弱酸).加入磷酸溶液的体积V和电流强度I的变化关系I-V图如图b所示.
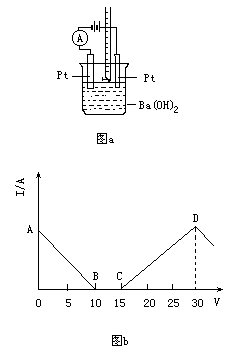
(1)处于AB之间时,溶液中导电的阴离子主要是:________;
(2)烧杯中刚加入H3PO4时,观察到的现象是:________;
(3)图b中,从A→B电流强度I变小的主要原因是:________.
有一实验如图所示:
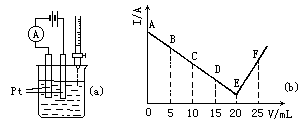
将30 mL 0.1mol/L 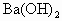 溶液置于烧杯中,然后边搅拌边慢慢加入0.1 mol/L由某第三周期元素形成的某酸溶液25 mL.加入酸溶液的体积V和安培计读数的坐标如上图所示.
溶液置于烧杯中,然后边搅拌边慢慢加入0.1 mol/L由某第三周期元素形成的某酸溶液25 mL.加入酸溶液的体积V和安培计读数的坐标如上图所示.
(1)此酸的化学式为_______.
(2)处于C点时,溶液中导电的阳离子主要是________.
(3)处于F点时,溶液中导电的阴离子主要是________.
(4)烧杯中刚加入酸时,观察到的现象是_______.
(5)图b中,从A→E电流强度I变小的主要原因是________.
实验室里有一瓶KCl与CaCl2的固体混合物,通过下面实验可确定该混合物中KCl和CaCl2的质量比,也可制得纯净的KCl,根据实验步骤填写下列空白:

(1)调整零点时,若指针偏向左边,应将左边的螺丝帽向(填左、右)______旋动。
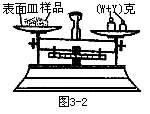
(2)某学生用已知质量y克的表面皿,准确称取W克样品,他在托盘天平的右盘放入(W+y)克砝码,在左盘的表面皿中加入样品,这时指针偏向右边,如图3-2示。
下面的操作应该是_______和______。
(3)加入的A是______,检验A是否过量的方法是______。

(4)过滤时,某学生的操作如图3-3所示,用文字说明图中的错误_____。
(5)滤液中加入的B物质是_______,应该加入过量B物质,理由是_____。
(6)为检验沉淀是否洗净,应在最后几滴洗出液中加入______,若______,表示沉淀已洗净。
(7)得到的固体C是_______。
(8)该混合物中KCl和CaCl2质量比的计算式是_____。
(9)配制100mL0.20mol·L-1的KCl溶液:某学生将准确称取的1.49gKCl固体放入烧杯中,加入约30mL蒸馏水,用玻璃棒搅拌使其溶解,将溶液由烧杯转移到100mL容量瓶中,然后往容量瓶中小心地加蒸馏水,直到液面接近标线2—3cm处,改用胶头滴管加蒸馏水,使溶液凹面最低点恰好与刻度相切,把容量瓶盖盖好,振荡摇匀,该学生操作中错误的是_____。
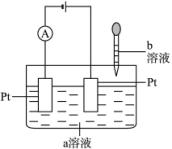
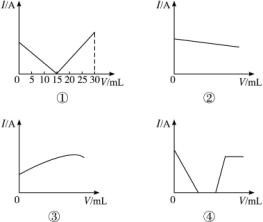
(1)若a为Ba(OH)2,D为H2SO4溶液,应选上图_________。
(2)若a为NH3·H2O,b为CH3COOH溶液,应选上图_________。
(3)若a为稀Ba(OH)2,b为浓HNO3溶液,应选上图_________。
(4)若a为Ba(OH)2,b为H3PO4溶液〔注Ba3(PO4)2、BaHPO4难溶于水,Ba(H2PO4)2易溶于水〕,应选上图_____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com