
题目列表(包括答案和解析)
(13分)有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B—少一个电子层,B原子得一个电子填入3p轨道后, 3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A+与D2—离子数之比为2:1。请回答下列问题:
(1)A元素形成的晶体属于密置堆积方式,则其晶体晶胞类型属于 。(填写“六方”、“面心立方”或“体心立方”)。
(2)B—的电子排布式 ,在CB3分子中C元素原子的原子轨道发生的是_______杂化。
(3)C的氢化物空间构型为 ,其氢化物在同族元素所形成的氢化物中沸点最高的原因是 。
(4)B元素的电负性 D元素的电负性(填“>”,“<”或“=”);用一个化学方程
式说明B、D两元素形成的单质的氧化性强弱: 。
(5)如上图所示是R形成的晶体的晶胞,设晶胞的边
长为acm。则R晶体的密度为 。(阿伏加德数常数用NA表示)
(13分)有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B—少一个电子层,B原子得一个电子填入3p轨道后, 3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A+与D2—离子数之比为2:1。请回答下列问题:
(1)A元素形成的晶体属于密置堆积方式,则其晶体晶胞类型属于 。(填写“六方”、“面心立方”或“体心立方”)。
(2)B—的电子排布式 ,在CB3分子中C元素原子的原子轨道发生的是_______杂化。
(3)C的氢化物空间构型为 ,其氢化物在同族元素所形成的氢化物中沸点最高的原因是 。
(4)B元素的电负性 D元素的电负性(填“>”,“<”或“=”);用一个化学方程
式说明B、D两元素形成的单质的氧化性强弱: 。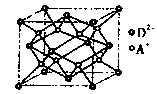
(5)如上图所示是R形成的晶体的晶胞,设晶胞的边
长为acm。则R晶体的密度为 。(阿伏加德数常数用NA表示)
(13分)有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B—少一个电子层,B原子得一个电子填入3p轨道后, 3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A+与D2—离子数之比为2:1。请回答下列问题:
(1)A元素形成的晶体属于密置堆积方式,则其晶体晶胞类型属于 。(填写“六方”、“面心立方”或“体心立方”)。
(2)B—的电子排布式 ,在CB3分子中C元素原子的原子轨道发生的是_______杂化。
(3)C的氢化物空间构型为 ,其氢化物在同族元素所形成的氢化物中沸点最高的原因是 。
(4)B元素的电负性 D元素的电负性(填“>”,“<”或“=”);用一个化学方程
式说明B、D两元素形成的单质的氧化性强弱: 。
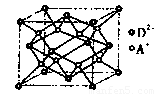
(5)如上图所示是R形成的晶体的晶胞,设晶胞的边
长为acm。则R晶体的密度为 。(阿伏加德数常数用NA表示)
实验室在制取某些产品时,当产品的沸点高于反应物的沸点时常常要用冷凝回流的方法,以提高反应的利用率,若已有试剂:a.液溴、b.铁粉、c.苯、d.NaOH液液、e.蒸馏水,又知下列物质的沸点:

今有主要装置(本题铁架台、铁夹等固定装置都已略去)如图所示:
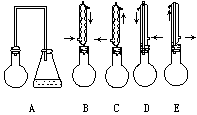
实验室欲制取溴苯时:
(1)为了提高溴苯的产率,选用________装置为最佳(填序号).
(2)向容器中加入试剂的顺序应为________(填试剂序号).
(3)发生反应的化学方程式为:________
(4)你选择的装置有缺欠吗?________(填“有”或“没有”).若有应该如何完善?________________________________________________________.
(5)用这种方法制得的溴苯常呈褐色,欲除去褐色应加入试剂________(填试剂名称).
(6)为了获得纯净的溴苯应把进行(5)操作后的混合液进行________(填一种操作名称),再进行________(填一种操作名称).
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com