
题目列表(包括答案和解析)
T(℃) | 0 | 10 | 20 | 30 | 40 |
S(克/100克水) | 11.5 | 15.1 | 19.4 | 24.4 | 37.6 |
若把质量分数为22%的该盐溶液由60℃逐渐冷却,则开始析出晶体的温度应( )
A.0℃~10℃ B.10℃~20℃ C.20℃~30℃ D.30℃~40℃
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤


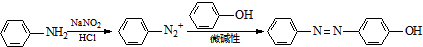
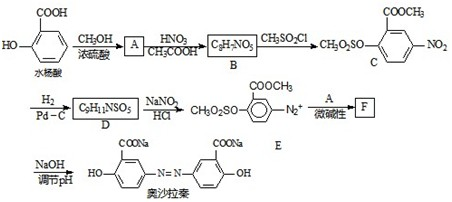
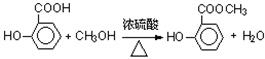

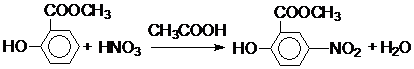
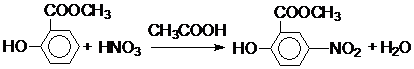
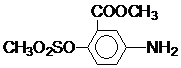
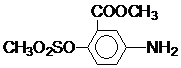
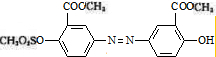
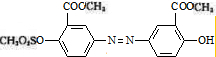
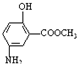 )也可用于合成奥沙拉秦.它的一种同分异构体X是α-氨基酸,能与FeCl3发生显色反应,其分子中共有6种化学环境不同的H原子.X的结构简式为
)也可用于合成奥沙拉秦.它的一种同分异构体X是α-氨基酸,能与FeCl3发生显色反应,其分子中共有6种化学环境不同的H原子.X的结构简式为

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com