
ĖâÄŋÁÐąí(°üĀĻīð°ļšÍ―âÎö)
ÄģŧŊŅ§Ņ§Ï°ÐĄŨéÍŽŅ§ļųūÝĘĩŅéĘŌÏÖÓÐĩÄÖÆČĄ°ąÆøĩÄŌĐÆ·ĢŽÉčžÆÁËÓŌÍžËųĘūĩÄĘĩŅéŨ°ÖÃĢĻēŋ·ÖžÐģÖŌĮÆũÎīŧģöĢĐĢŽÖÆČĄēĒĖ―ūŋ°ąÆøĩÄŧđÔÐÔĄĒžėŅé·īÓĶēúÎïĄĢĮëŧØīðÏÂÁÐÎĘĖâĢš
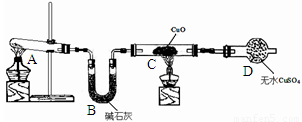
ĢĻ1ĢĐAÖзĒÉú·īÓĶĩÄŧŊŅ§·―ģĖĘ―ĘĮ ĄĢ
ĢĻ2ĢĐBÖОîĘŊŧŌĩÄŨũÓÃĘĮ ĄĢ
ĢĻ3ĢĐCÖКÚÉŦđĖĖåąäšėĢŽĮŌēúÉúĩÄÆøĖåķÔŋÕÆøÎÞÎÛČūĢŽÐīģöļ÷īÓĶĩÄŧŊŅ§·―ģĖĘ― Ģŧ
DÖзĒÉúĩÄÏÖÏóĘĮ________________________________________________________________________ĄĢ
ĢĻ4ĢĐļÃŨ°ÖÃīæÔÚÃũÏÔČąÏÝĢŽļÃČąÏÝĘĮ ĄĢ
ĢĻ5ĢĐđĪŌĩÖÐģĢÓÃĩŠÆøÓëĮâÆøÔÚļßÎÂĄĒļßŅđĄĒĖúīĨÃ―ŨöīßŧŊžÁĩÄĖõžþÏšÏģÉ°ąÆøĢŽļÃÐĄŨéÍŽŅ§ÄĢÄâļÃĖõžþŌēšÏģÉģöÁË°ąÆøĄĢŌŅÖŠÆðʞʹĢŽ―Ŧ2 mol N2ĄĒ6 mol H2ģäČëŌŧļöČÝŧýΊ2 LĩÄÃÜąÕČÝÆũÖзĒÉú·īÓĶĢŽđýÁË5 minšóĢŽŧėšÏÆøĖåĩÄŨÜÎïÖĘĩÄÁŋžõÉŲÁË1 molĢŽĮóÔÚÕâķÎĘąžäÄÚŌÔH2ąíĘūĩÄŧŊŅ§·īÓĶËŲÂĘ
Ί ĄĢ
ÄģŧŊŅ§Ņ§Ï°ÐĄŨéÍŽŅ§ļųūÝĘĩŅéĘŌÏÖÓÐĩÄÖÆČĄ°ąÆøĩÄŌĐÆ·ĢŽÉčžÆÁËÓŌÍžËųĘūĩÄĘĩŅéŨ°ÖÃĢĻēŋ·ÖžÐģÖŌĮÆũÎīŧģöĢĐĢŽÖÆČĄēĒĖ―ūŋ°ąÆøĩÄŧđÔÐÔĄĒžėŅé·īÓĶēúÎïĄĢĮëŧØīðÏÂÁÐÎĘĖâĢš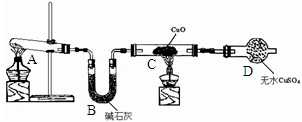
ĢĻ1ĢĐAÖзĒÉú·īÓĶĩÄŧŊŅ§·―ģĖĘ―ĘĮ ĄĢ
ĢĻ2ĢĐBÖОîĘŊŧŌĩÄŨũÓÃĘĮ ĄĢ
ĢĻ3ĢĐCÖКÚÉŦđĖĖåąäšėĢŽĮŌēúÉúĩÄÆøĖåķÔŋÕÆøÎÞÎÛČūĢŽÐīģöļ÷īÓĶĩÄŧŊŅ§·―ģĖĘ― Ģŧ
DÖзĒÉúĩÄÏÖÏóĘĮ________________________________________________________________________ĄĢ
ĢĻ4ĢĐļÃŨ°ÖÃīæÔÚÃũÏÔČąÏÝĢŽļÃČąÏÝĘĮ ĄĢ
ĢĻ5ĢĐđĪŌĩÖÐģĢÓÃĩŠÆøÓëĮâÆøÔÚļßÎÂĄĒļßŅđĄĒĖúīĨÃ―ŨöīßŧŊžÁĩÄĖõžþÏšÏģÉ°ąÆøĢŽļÃÐĄŨéÍŽŅ§ÄĢÄâļÃĖõžþŌēšÏģÉģöÁË°ąÆøĄĢŌŅÖŠÆðʞʹĢŽ―Ŧ2 mol N2ĄĒ6 mol H2ģäČëŌŧļöČÝŧýΊ2 LĩÄÃÜąÕČÝÆũÖзĒÉú·īÓĶĢŽđýÁË5 minšóĢŽŧėšÏÆøĖåĩÄŨÜÎïÖĘĩÄÁŋžõÉŲÁË1 molĢŽĮóÔÚÕâķÎĘąžäÄÚŌÔH2ąíĘūĩÄŧŊŅ§·īÓĶËŲÂĘ
Ί ĄĢ
ÄģŧŊŅ§Ņ§Ï°ÐĄŨéÍŽŅ§ļųūÝĘĩŅéĘŌÏÖÓÐĩÄÖÆČĄ°ąÆøĩÄŌĐÆ·ĢŽÉčžÆÁËÓŌÍžËųĘūĩÄĘĩŅéŨ°ÖÃĢĻēŋ·ÖžÐģÖŌĮÆũÎīŧģöĢĐĢŽÖÆČĄēĒĖ―ūŋ°ąÆøĩÄŧđÔÐÔĄĒžėŅé·īÓĶēúÎïĄĢĮëŧØīðÏÂÁÐÎĘĖâĢš
ĢĻ1ĢĐAÖзĒÉú·īÓĶĩÄŧŊŅ§·―ģĖĘ―ĘĮĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄ ĄĢ
ĢĻ2ĢĐBÖОîĘŊŧŌĩÄŨũÓÃĘĮĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄ ĄĢ
ĢĻ3ĢĐCÖКÚÉŦđĖĖåąäšėĢŽĮŌēúÉúĩÄÆøĖåķÔŋÕÆøÎÞÎÛČūĢŽÐīģöļ÷īÓĶĩÄŧŊŅ§·―ģĖĘ―ĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄ ĢŧDÖзĒÉúĩÄÏÖÏóĘĮ__________________________ĄĢ
ĢĻ4ĢĐļÃŨ°ÖÃīæÔÚÃũÏÔČąÏÝĢŽļÃČąÏÝĘĮĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄ ĄĢ
ĢĻ5ĢĐđĪŌĩÖÐģĢÓÃĩŠÆøÓëĮâÆøÔÚļßÎÂĄĒļßŅđĄĒĖúīĨÃ―ŨöīßŧŊžÁĩÄĖõžþÏšÏģÉ°ąÆøĢŽļÃÐĄŨéÍŽŅ§ÄĢÄâļÃĖõžþŌēšÏģÉģöÁË°ąÆøĄĢŌŅÖŠÆðʞʹĢŽ―Ŧ2 mol N2ĄĒ6 mol H2ģäČëŌŧļöČÝŧýΊ2 LĩÄÃÜąÕČÝÆũÖзĒÉú·īÓĶĢŽđýÁË5 minšóĢŽŧėšÏÆøĖåĩÄŨÜÎïÖĘĩÄÁŋžõÉŲÁË1 molĢŽĮóÔÚÕâķÎĘąžäÄÚŌÔH2ąíĘūĩÄŧŊŅ§·īÓĶËŲÂĘΊĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄĄ ĄĢ


ÎŌđúŧŊđĪŨĻžŌšîĩ°ņĩÄĄ°šîĘÏÖÆžî·ĻĄąÔøΊĘĀ―įÖÆžîđĪŌĩŨöģöÁËÍŧģöđąÏŨĄĢËûŌÔNaClĄĒNH3ĄĒCO2ĩČΊÔÁÏÏČÖÆĩÃNaHCO3ĢŽ―øķøÉúēúģöīŋžîĄĢÓÐđØ·īÓĶĩÄŧŊŅ§·―ģĖĘ―ÎŠĢš
NH3ĢŦCO2ĢŦH2O NH4HCO3 Ģŧ NH4HCO3ĢŦNaCl NaHCO3ĄýĢŦNH4Cl Ģŧ
2NaHCO3![]() Na2CO3ĢŦCO2ĄüĢŦH2O
Na2CO3ĢŦCO2ĄüĢŦH2O
ĢĻ1ĢĐĖžËáĮâï§ÓëąĨšÍĘģŅÎËŪ·īÓĶĢŽÄÜÎöģöĖžËáĮâÄÆū§ĖåĩÄÔŌōĘĮ ĢĻĖîŨÖÄļąęšÅĢĐĢŧ
aĢŪĖžËáĮâÄÆÄŅČÜÓÚËŪ
bĢŪĖžËáĮâÄÆĘÜČČŌŨ·Ö―â
cĢŪĖžËáĮâÄÆĩÄČÜ―âķČÏāķÔ―ÏÐĄĢŽËųŌÔÔÚČÜŌšÖÐĘŨÏČ―áū§Îöģö
ĢĻ2ĢĐÄģĖ―ūŋŧîķŊÐĄŨéļųūÝÉÏĘöÖÆžîÔĀíĢŽ―øÐÐĖžËáĮâÄÆĩÄÖÆąļĘĩŅéĢŽÍŽŅ§ÃĮ°īļũŨÔÉčžÆĩÄ·―°ļĘĩŅéĄĢ
ĒŲ ŌŧÎŧÍŽŅ§―ŦķþŅõŧŊĖžÆøĖåÍĻČ뚎°ąĩÄąĨšÍĘģŅÎËŪÖÐÖÆąļĖžËáĮâÄÆĢŽĘĩŅéŨ°ÖÃČįÓŌÍžËųĘūĢĻÍžÖОÐģÖĄĒđĖķĻÓÃĩÄŌĮÆũÎīŧģöĢĐĄĢ
ĘÔŧØīðÏÂÁÐÓÐđØÎĘĖâĢš

![]() ĢĻĒņĢĐŌŌŨ°ÖÃÖÐĩÄĘÔžÁĘĮ
ĢĻĒņĢĐŌŌŨ°ÖÃÖÐĩÄĘÔžÁĘĮ
ĢĻĒōĢĐķĄŨ°ÖÃÖÐÏĄÁōËáĩÄŨũÓÃĘĮ
ĢĻĒóĢĐĘĩŅé―áĘøšóĢŽ·ÖĀëģöNaHCO3 ū§ĖåĩÄēŲŨũĘĮ ĢĻĖî·ÖĀëēŲŨũĩÄÃûģÆĢĐĄĢ
ĢĻIVĢĐĮëÄãÔŲÐīģöŌŧÖÖĘĩŅéĘŌÖÆČĄÉŲÁŋĖžËáĮâÄÆĩÄ·―·ĻĢš ĄĢ
đúžĘŅ§ÐĢÓÅŅĄ - Á·Ï°ēáÁÐąí - ĘÔĖâÁÐąí
šþąąĘĄŧĨÁŠÍøÎĨ·ĻšÍēŧÁžÐÅÏĒūŲąĻÆ―ĖĻ | ÍøÉÏÓКĶÐÅÏĒūŲąĻŨĻĮø | ĩįÐÅÕĐÆūŲąĻŨĻĮø | ÉæĀúĘ·ÐéÎÞÖũŌåÓКĶÐÅÏĒūŲąĻŨĻĮø | ÉæÆóĮÖČĻūŲąĻŨĻĮø
ÎĨ·ĻšÍēŧÁžÐÅÏĒūŲąĻĩįŧ°Ģš027-86699610 ūŲąĻÓĘÏäĢš58377363@163.com