
题目列表(包括答案和解析)
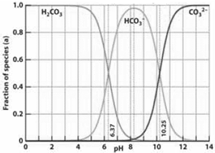 右图是一水溶液在pH从0至14的范围内H2CO3、HCO3-、CO32-三种成分平衡时组成分数,下列叙述不正确的是( )
右图是一水溶液在pH从0至14的范围内H2CO3、HCO3-、CO32-三种成分平衡时组成分数,下列叙述不正确的是( )| A.人体血液的pH约为7.4,则CO2在血液中多以HCO3-形式存在 |
| B.在pH为10.25时,溶液中c(HCO3-)=c(CO32-) |
| C.若用CO2和NaOH反应制取Na2CO3,溶液的pH必须控制在12以上 |
| D.此图是1.0mol/L碳酸钠溶液滴定1.0mol/LHCl溶液的滴定曲线 |
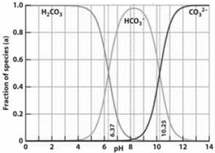
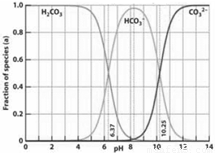
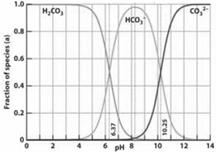 右图是一水溶液在pH从0至14的范围内H2CO3、HCO3-、CO32-三种成分平衡时组成分数,下列叙述不正确的是
右图是一水溶液在pH从0至14的范围内H2CO3、HCO3-、CO32-三种成分平衡时组成分数,下列叙述不正确的是
![]()
A.人体血液的pH约为7.4,则CO2在血液中多以HCO3-形式存在
![]()
B.在pH为10.25时,溶液中c(HCO3-)=c(CO32-)
C.若用CO2和NaOH反应制取Na2CO3,溶液的pH必须控制在12以上
![]()
D.此图是1.0 mol/L 碳酸钠溶液滴定1.0 mol/L HCl溶液的滴定曲线
右下图是一水溶液在pH从0至14的范围内,H2CO3、HCO![]() 、CO
、CO![]() 三种成分平衡时的各组分分数,下列叙述正确的是
三种成分平衡时的各组分分数,下列叙述正确的是

A.pH=2时,H2CO3、HCO![]() 、CO
、CO![]() 共存
共存
B.在pH为6.37及10.25时,溶液中
![]() c(H2CO3)= c(HCO
c(H2CO3)= c(HCO![]() )= c(CO
)= c(CO![]() )
)
![]() C.人体血液的pH约为7.4,则CO2在血液中多以HCO
C.人体血液的pH约为7.4,则CO2在血液中多以HCO![]() 的形式存在
的形式存在
![]() D.若用CO2和NaOH反应制取Na2CO3,溶液的pH必须控制在12以上
D.若用CO2和NaOH反应制取Na2CO3,溶液的pH必须控制在12以上
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com