
题目列表(包括答案和解析)
- 2 |
- 4 |
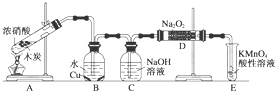
已知,室温下存在反应3HNO2===HNO3+2NO↑+H2O;在酸性溶液中,NO![]() 可将 MnO
可将 MnO![]() 还原为Mn2+且无气体生成。某化学兴趣小组设计了如下探究实验:
还原为Mn2+且无气体生成。某化学兴趣小组设计了如下探究实验:

请回答下列问题:
(1)装置A的试管中发生反应的化学方程式是 。
(2)B瓶中可以观察到的现象是 ,C瓶出来的气体是 。
(3)实验时观察到D 管内固体颜色逐渐变为白色。据此甲同学认为D管中生成物是NaNO3,而乙同学则认为D管中生成的是NaNO2,如何证明乙同学的观点正确?
| 实验方法 | 实验现象 | 反应的离子方程式 |
(4)E装置的作用是 。
(5)同学们经讨论认为上述装置仍有缺陷,为了避免D管中生成NaOH,你认为应该进行的改进是 。
已知,室温下存在反应3HNO2===HNO3+2NO↑+H2O;在酸性溶液中,NO![]() 可将 MnO
可将 MnO![]() 还原为Mn2+且无气体生成;酸性KMnO4溶液可吸收氮的氧化物。某化学兴趣小组设计了如下探究实验(实验前先排尽装置中的空气):
还原为Mn2+且无气体生成;酸性KMnO4溶液可吸收氮的氧化物。某化学兴趣小组设计了如下探究实验(实验前先排尽装置中的空气):

请回答下列问题:
(1)装置A的试管中发生反应的化学方程式是 。
(2)B瓶中可以观察到的现象是 ,C瓶出来的气体是 。
(3)实验时观察到D 管内固体颜色逐渐变为白色。据此甲同学认为D管中生成物是NaNO3,而乙同学则认为D管中生成的是NaNO2,如何证明乙同学的观点正确?
| 实验操作 | 实验现象 | 实验结论 |
| D管生成的是NaNO2 |
(4)E装置的作用是 。
(5)同学们经讨论认为上述装置仍有缺陷,为了避免D管中生成NaOH,你认为应该进行的改进是 。
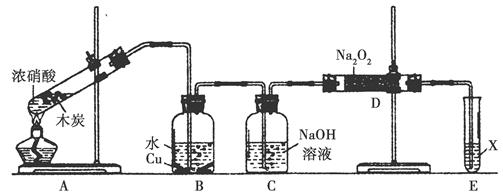
某化学兴趣小组以木炭和浓硝酸为起始原料,探究一氧化氮与过氧化钠反应制备亚硝酸钠。设计装置如下(忽略装置中空气的影响),请回答下列问题: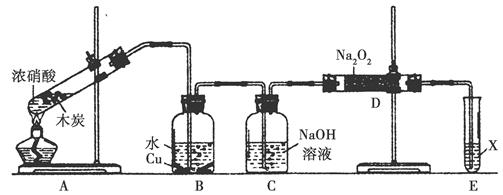
(1)组装好仪器后,必须进行的一项操作是_________________。
(2)装置A的试管中发生反应的化学方程式是_______________。
(3)推测B中可以观察到的主要现象是________;C装置的作用是________。
(4)装置D中除生成NaNO2外,还有另一种固态物质Y,Y的化学式是________;可以通过适当改进,不产生Y物质,请你提出改进方法:______________________。
(5)已知:亚硝酸是弱酸,不稳定,室温下存在反应3HNO2=HNO3+2NO↑+H2O;在酸性溶液中,NO2-可将MnO4-还原为Mn2+且无气体生成。
①写出检验D中产物是亚硝酸钠的方法:_________________;
②E装置中试剂X可以是________。
| A.稀硫酸 | B.酸性高锰酸钾溶液 |
| C.稀硝酸 | D.水 |
| A.稀硫酸 | B.酸性高锰酸钾溶液 |
| C.稀硝酸 | D.水 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com