
题目列表(包括答案和解析)
7、在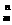 X
X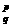 中,m、n、p、q表示某元素X的四个角码,若X1与X2的q均为1,m、p的值相等,而n值不相等,则X1和X2表示的可能是
中,m、n、p、q表示某元素X的四个角码,若X1与X2的q均为1,m、p的值相等,而n值不相等,则X1和X2表示的可能是
A.相同原子 B.不同元素
C.同种元素不同原子形成的离子 D.不同元素的离子
6、某元素的质量数为A,它的阴离子Xn-核外有x个电子,w克这种元素的原子核内中子数为
A.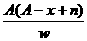 molB.
molB. 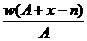 mol C.
mol C.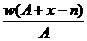 mol D.
mol D. mol
mol
5、某元素X的最高价氧化物的分子式为X2O5,在它的氢化物中含氢3.85%,则该元素的原子量为
A. 14 B.31 C.74.9 D.121.8
4、下列说法正确的是
A.形成阳离子的过程一定是还原反应
B.形成阴离子的过程一定是氧化反应
C.由单质形成离子化合物的过程一定是氧化还原反应
D.燃烧反应所形成的化合物一定是离子化合物
3、已知X、Y、Z为三种原子序数相连的元素,最高氧化物对应水化物的酸性相对强弱是:HXO4 >H2YO4 >H3ZO4,则下列判断正确的是
A.气态氢化物的稳定性:HX> H2Y >ZH3 B.非金属活泼性:Y<X<Z
C.原子半径:X > Y > Z D.原子最外层上电子数的关系:Y=
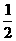 (X+Y)
(X+Y)
2、下列原子结构示意图中,正确的是
A.  B.
B. 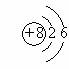 C.
C. 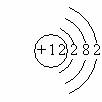 D.
D. 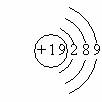
P102.7 105.9 111.3 115.17 116.6 130.4 132.2 133.11 134.7 136.6
1、质量数为37的原子,应该有 ( )
A .18个质子、19个中子、19个电子 B.17个质子、20个中子、18个电子
C.19个质子、18个中子、20个电子 D. 18个质子、19个中子、18个电子
16.将多少克钠投入10 g水中,反应后生成溶液在10℃时刚好饱和?此饱和溶液的质量分数是多少?(已知10℃时该溶液溶质的溶解度为22 g)
15.(6分)为了测定某种碱金属的原子量而设计的装置如右图所示,该装置(包括水)的总质量为a g,将质量为b g?(不足量)的某碱金属放入水中,立即塞紧瓶塞。完全反应后,再称此装置总质量为c g。则:

(1)列式计算该碱金属原子量的数学表达式 。
(2)无水氯化钙的作用是 。
(3)如果不用无水CaCl2,求出的原子量比实际的原子量偏大还是偏小,为什么?
14.(8分)已知有四种钠的化合物W、X、Y、Z,根据下列关系推断W、X、Y、Z的化学式。
W X+CO2+H2O
X+CO2+H2O
Z+CO2 X+O2
X+O2
Z+H2O Y+O2
Y+O2
X+Ca(OH)2 Y+CaCO3↓
Y+CaCO3↓
(1)有关化学式为X Y Z W
(2)写出Y+W反应的化学方程式
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com