
题目列表(包括答案和解析)
26、(1)C5H9O4N(2分)
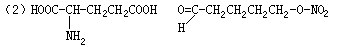 |
(各1分) |
25、(1)C32H14(1分) (2)(Ⅰ)1(1分) (Ⅱ)4(1分)
(3)不在同一平面内(1分)
23、C、D、F(4分) 24、(1)六边(2分) (2)n(2分)
|
19、全反射(2分) 倒影(2分) 20、 |
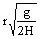 |
(4分) |
21、1×104(4分) 22、400(2分) 100(2分)
36、(20分)核电站中采用核反应堆使重核裂变,将释放出的巨大能量转换成电能。
(1)完成下列核反应式:
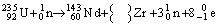 |
+反中微子 |
(反中微子的质量数和电荷数均为零)
(2)写出核裂变反应和一般化学反应的不同点。(请答3点)
(3)核电站在热量的循环系统中应用了钠钾合金作为传热介质,试根据钠钾合金的性质说明这一应
用的两点理由。
(4)依据上述核反应方程式,计算1kg铀235全部裂变可产生多少kJ的能量?需要燃烧多少千克标准
煤才能释放出相同的能量?
已知:铀(U)核的质量为235.0439u,中子(n)质量为1.0087u,钕(Nd)核的质量为142.9098u,
锆(Zr)核的质量为89.9047u,1u=1.6606×10-27kg,燃烧1kg标准煤能产生2.93×104kJ的热量。
35、(20分)铅蓄电池放电时起原电池的作用,充电时起电解池的作用,铅蓄电池在放电和充电时发
生的化学反应可用下式表示:
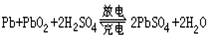
(1)蓄电池使用日久后正负极标志模糊,现根据下列两种条件,如何来判断正负极:
①氯化铜溶液,两根带有铜导线的碳棒 。
②硫酸铜溶液,两根铜导线 。
(2)假如采用第②种方法进行实验,实验前后分别精确称重硫酸铜溶液和两根铜导线的总质量,假
如不考虑实验误差,前者质量将 (填“增大”、“减小”或“不变”);后者将 (填“增加”、
“减少”或“不变”)。假使两根铜导线质量之差为0.32g,则铅蓄电池内部要消耗H2SO4 mol。
(3)铅蓄电池的电压正常情况下保持2.0V,电压下降到约1.85V时需要重新充电,铅蓄电池充电时,
阴极反应式为 。
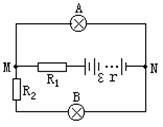
(4)现将这种铅蓄电池五节串联起来作为电源接入下图的电路中,每节蓄电池电动势为2V,内阻
|
为0.2Ω,R2=2Ω,灯A的标号为“6V,6W”,灯B是“4V,4W”,求: ①如果要使B灯正常发光,R1应是多大? ②这时灯A的实际功率是多少? |
 |
34、(28分)材料一:酸雨是英国化学家R·A·Smith 1872年最先提出的,一般是指PH值小于5.6的
雨、雪、雾等大气降水,是大气污染的表现。酸雨被称作“空中死神”。据某市区1998年环境状况公报
载,市区酸雨频率为41.3%,比上年上升了5.5个百分点。降水年平均值为4.87,降水酸性污染较严重,表
现为煤烟型污染特征。
材料二:①某地一场较大范围的酸雨,植物叶面遭腐蚀,产生大量斑点和坏死,导致西瓜大面积绝
产,损失惨重。
②酸雨使植物阳离子从叶面析出。使钙、镁、铁等离子迅速从土壤中损失,土壤营养状况降低。还使
光合作用抑制,影响植物生长。
③铝对生物来说是有害元素,土壤中以氧化铝存在,PH=5.6时几乎不溶解,当PH值为4.6时,铝的溶
解度增加100倍,并转化成硫酸铝,造成树木死亡。四川某林场,华山松死亡率达96%,就是酸雨使土壤中
硫酸铝浓度增高,危及于华山松。
材料三:某校科技小组同学采集酸雨样品,每隔一段时间测定PH,得到下列数据:
|
时 间 |
开 始 |
8小时 |
16小时 |
24小时 |
32小时 |
40小时 |
48小时 |
|
PH |
5.0 |
4.8 |
4.5 |
4.3 |
4.2 |
4.0 |
4.0 |
请依据材料回答:
(1)酸雨的形成是工业生产过程中大量矿物燃料使用,使空气中 气体较多,与降水结合产
生,请写出酸雨形成的化学反应方程式 。
(2)酸雨对高等植物的影响,表现在哪几方面?
A、 ,
B、 ,
C、 。
(3)大气污染,一方面影响动、植物生长,另一方面对人类 系统危害最大,影响呼吸过程
的 ,常见疾病有 。
(4)解释酸雨放置时,PH变化的主要原因。
(5)写出PH变化的离子方程式。
(6)请根据所学的生物、化学知识,对该市的酸雨防治提出合理化建议(至少三条)。
0.001)为 。
(3)此晶体化学式为 。
33、(16分)钢铁是最重要的金属材料。我国年产钢铁产量已超过1亿吨,居世界第一位。
(1)工业上用铁矿石和焦炭来炼铁。请写出用菱铁矿石(主要成分是FeCO3)和焦炭为原料来炼铁的
化学方程式 。
(2)从高炉冶炼得到的生铁,含铁约95%左右,要得到纯铁(含铁99.9%以上)可采用电解的方法。
电解槽的阳极材料应选用 ,阴极材料应选用 电解质溶液应采用溶液。要获取1.0kg纯铁,
电极上通过的电量理论值为 。(电子电量e=1.60×10-19C)
|
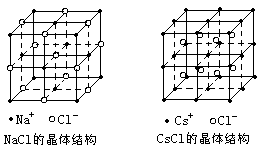
(3)1183k以下纯铁晶体的基本结构单元与CsCl相同, 1183k以上转变为与干冰相似(如图示)两种晶体中最邻近的 铁原子间距离相同。求转变温度时两者的密度比(取两位有 效数字)。 |
 |
|
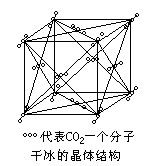
(4)FeO晶体基本结构单元为NaCl型(如图示)。实际上FeO晶体中存在着 空位、错位、杂质原子等缺陷。晶体缺陷对晶体的性质产生重大影响。由于晶体 缺陷,在FeO晶体中Fe和O的比值发生了变化,变为FeXO,x值小于1,测知FexO晶 体密度为5.71g·cm-3,基本结构单元边长为4.28×10-10m。求: |
 |
(1)FexO中x值(精确至0.01)为 。
(2)晶体中的Fe分别为Fe2+、Fe3+,在Fe2+和Fe3+的总数中,Fe3+所占分数(用小数表示精确至
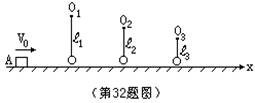
32、(16分)如图所示,滑块A质量m=0.01kg,与水平地面间的动摩擦因数μ=0.2,用细线悬挂的小
球质量均为m=0.01kg,沿x轴排列,A与第1只小球相邻两小球间距离均为S=2m,线长分别为l1、l2、l3……
(图中只画出三只小球)。开始时,滑块以速度V0=10m/S沿x轴正向运动,设滑块与小球碰撞时不损失机
械能,碰撞后小球均恰能在竖直平面内完成完整的圆运动。求:
|
(1)滑块能与几个小球碰撞? (2)求出碰撞中第n个小球悬线长ln的表达式。 |
 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com