
ĚâÄżÁбí(°üŔ¨´đ°¸şÍ˝âÎö)
17Ł®ĎÂÁĐĐđĘöŐýČ·µÄĘÇ(ˇˇ )
ˇˇ ˇˇˇˇ ˇˇAŁ®ÄłżÉČÜĐÔÎďÖʵÄĦ¶űÖĘÁż´óÓÚ18 g/molŁ¬Ôň¸ĂÎďÖʵÄŨČÜŇşµÄĂܶČŇ»¶¨´óÓÚ1 g/cm3
ˇˇ ˇˇˇˇ ˇˇBŁ®ÄłÎ¶ČʱŁ¬NaCl±ĄşÍČÜŇşµÄÖĘÁż·ÖĘýÎŞa %Ł¬NaClµÄČÜ˝â¶ČÎŞS gŁ¬ÔňaŇ»¶¨´óÓÚS
ˇˇ ˇˇˇˇCŁ®˝«90 %µÄH2SO4ČÜŇşÓë10 %µÄH2SO4ČÜŇşµČĚĺ»ý»ěşĎŁ¬ËůµĂ»ěşĎČÜŇşÖĐH2SO4µÄÖĘÁż·ÖĘýŇ»¶¨µČÓÚ50 %
ˇˇˇˇ DŁ®±ĄşÍKClČÜŇşµÄĂܶČÎŞ¦ŃgŁŻcm3Ł¬ÎďÖʵÄÁżĹ¨¶ČÎŞc molŁŻLŁ¬Ôň´ËČÜŇşÖĐKClµÄÖĘÁż·ÖĘýÎŞ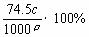
16Ł®ĎÂÁĐ»ěşĎÎďµÄ·ÖŔë»ňĚá´ż˛Ů×÷Öв»ŐýČ·µÄĘÇ(ˇˇˇˇ )
ˇˇ ˇˇˇˇ ˇˇAŁ®łýČĄN2ÖеÄÉŮÁżO2Ł¬żÉͨąý×ĆČȵÄCuÍřŁ¬ĘŐĽŻĆřĚĺ
ˇˇ ˇˇˇˇ ˇˇBŁ®łýČĄFe(OH)3˝şĚĺÖĐ»ěÓеÄCl-Ŕë×ÓŁ¬żÉÓĂąýÂ˵ķ˝·¨
ˇˇ ˇˇˇˇ ˇˇCŁ®łýČĄŇŇ´ĽÖеÄÉŮÁżNaClŁ¬żÉÓĂŐôÁóµÄ·˝·¨
ˇˇ ˇˇˇˇ ˇˇDŁ®Öؽᾧˇ˘ÝÍȡ˛Ů×÷¶ĽżÉÓĂÓÚĚá´żÎďÖĘ
15Ł®ÔÚÉú»îˇ˘Éú˛úĽ°»ŻŃ§ŃĐľżÖĐŁ¬ČËĂÇľłŁĐčŇŞ¸ůľÝ˛»Í¬Ô×Óˇ˘·Ö×Ó»ňŔë×ÓµÄijЩĚŘŐ÷·´Ó¦¶ÔÎďÖĘ˝řĐĐÇř±đˇ˘ĽěŃéµČˇŁĎÂÁĐ˵·¨ŐýČ·µÄĘÇ(ˇˇ )
A. ÓĂKOHČÜŇşżÉŇÔ˝«(NH4) 3PO4ˇ˘NaBrˇ˘CuSO4ˇ˘AlCl3Çř±đżŞ
ˇˇ ˇˇ ˇˇBŁ®MnO2ˇ˘CuOˇ˘FeČýÖÖÎďÖʵķŰÄ©¶ĽĘÇşÚÉ«µÄŁ¬ÓĂϡŃÎË᲻ÄÜ˝«ËüĂÇÇř±đżŞ
C. ÄłČÜŇşÖĐĽÓČëϡŃÎËáÓĐÎŢÉ«ĆřĚĺ˛úÉúŁ¬¸ĂĆřĚĺÄÜĘąłÎÇĺĘŻ»ŇË®±ä»ë×ÇŁ¬Ôň´ËČÜŇşÖĐŇ»¶¨ş¬ÓĐCO32¯
ˇˇ ˇˇ ˇˇDŁ®żÉŇÔÓĂBaCl2ČÜŇşşÍϡĎőËáĽěŃéNa2SO3 ĘÇ·ń±äÖĘ
14. ĎÂÁĐ˵·¨ŐýČ·µÄĘÇ(ˇˇ )
AŁ®ľ˛â¶¨Ň»ĆżĆřĚĺÖĐÖ»ş¬Á˝ÖÖÔŞËŘŁ¬ÔňŐâĆżĆřĚ岻żÉÄÜĘÇŇ»ÖÖµĄÖĘşÍŇ»ÖÖ»ŻşĎÎďµÄ»ěşĎÎď
BŁ®µç×ÓĘýĎŕͬµÄ΢ÁŁ˛»Ň»¶¨ĘÇͬһÖÖÔŞËŘ
CŁ®Ň»°ăÇéżöĎÂŁ¬şĎ˝đµÄČ۵ăşÍÓ˛¶Č¶Ľ±ČłÉ·Ö˝đĘô¸ß
DŁ®˝şĚĺÇř±đÓÚĆäËű·ÖɢϵµÄ±ľÖĘĚŘŐ÷ĘÇľßÓжˇ´ď¶űĎÖĎó
13Ł®˝řĐĐ»ŻŃ§ĘµŃ飬ąŰ˛âʵŃéĎÖĎóŁ¬Í¨ąý·ÖÎöÍĆŔíµĂłöŐýČ·µÄ˝áÂŰĘÇ»ŻŃ§Ń§Ď°µÄ·˝·¨Ö®Ň»ˇŁĎÂÁжÔÓĐąŘʵŃéĘÂʵµÄ˝âĘÍŐýČ·µÄĘÇ(ˇˇ )
ˇˇˇˇ AŁ®SO2ĆřĚĺĘą¸ßĂĚËáĽŘČÜŇşÍĘÉ«Ł¬±íĎÖÁËSO2µÄĆŻ°×ĐÔ
BŁ®ÔÚş¬ÓĐCu(NO3)2ˇ˘Mg(NO3)2şÍAgNO3µÄČÜŇşÖĐĽÓČëĘĘÁżĐż·ŰŁ¬Ę×ĎČÖĂ»»łöµÄĘÇCu
CŁ®Ĺ¨ĎőËáÔÚąâŐŐĚőĽţϱä»ĆŁ¬ËµĂ÷ŨĎőËáŇ×·Ö˝âÉúłÉÓĐÉ«˛úÎďÇŇČÜÓÚŨĎőËá
D. łŁÎÂĎÂŁ¬˝«ÂÁƬ·ĹČëŨÁňËáÖĐŁ¬ÎŢĂ÷ĎÔĎÖĎóŁ¬ËµĂ÷ÂÁ˛»ÓëŔäµÄŨÁňËá·˘Ó¦
12Ł®ÔÚÄÜÓëÂÁ·´Ó¦˛úÉúÇâĆřµÄČÜŇşÖĐŁ¬Ň»¶¨ÄÜ´óÁżą˛´ćµÄŔë×Ó×éĘÇ(ˇˇ )
ˇˇˇˇ A. NH4+ˇ˘Cu2+ˇ˘Cl-ˇ˘NO3-ˇˇˇˇˇˇˇˇˇˇˇˇˇˇ ˇˇˇˇ B. K+ˇ˘Na+ˇ˘SO32-ˇ˘S2-ˇˇ
C. K+ˇ˘Na+ˇ˘AlO2-ˇ˘SO42-ˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ D. Ba2+ˇ˘Na+ˇ˘ClŁˇ˘Br--
11.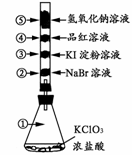 ŇŃÖŞłŁÎÂĎÂÂČËáĽŘÓëŨŃÎËá·´Ó¦ÄÜ·ĹłöÂČĆřŁ¬ĎÖ°´ÓŇĎÂÍĽ˝řĐбËصÄĐÔÖĘʵŃ顣˛ŁÁ§ąÜÄÚ·Ö±đ×°ÓеÎÓĐÉŮÁż˛»Í¬ČÜŇşµÄ°×É«ĂŢÇňŁ¬·´Ó¦Ň»¶ÎʱĽäşóŁ¬¶ÔÍĽÖĐÖ¸¶¨˛żÎ»ŃŐÉ«ĂčĘöŐýČ·µÄĘÇ(ˇˇ )
ŇŃÖŞłŁÎÂĎÂÂČËáĽŘÓëŨŃÎËá·´Ó¦ÄÜ·ĹłöÂČĆřŁ¬ĎÖ°´ÓŇĎÂÍĽ˝řĐбËصÄĐÔÖĘʵŃ顣˛ŁÁ§ąÜÄÚ·Ö±đ×°ÓеÎÓĐÉŮÁż˛»Í¬ČÜŇşµÄ°×É«ĂŢÇňŁ¬·´Ó¦Ň»¶ÎʱĽäşóŁ¬¶ÔÍĽÖĐÖ¸¶¨˛żÎ»ŃŐÉ«ĂčĘöŐýČ·µÄĘÇ(ˇˇ )
|
ˇˇ |
˘Ů |
˘Ú |
˘Ű |
˘Ü |
|
A |
»ĆÂĚÉ« |
łČÉ« |
Ŕ¶É« |
şěÉ« |
|
B |
»ĆÂĚÉ« |
łČÉ« |
Ŕ¶É« |
°×É« |
|
C |
»ĆÂĚÉ« |
ÎŢÉ« |
×ĎÉ« |
şěÉ« |
|
D |
ÎŢÉ« |
łČÉ« |
×ĎÉ« |
°×É« |
10Ł®ĎÂÁĐĚőĽţĎÂŁ¬Á˝ĆżĆřĚĺËůş¬µÄÔ×ÓĘýŇ»¶¨ĎŕµČµÄĘÇ(ˇˇ )
AŁ®Í¬ÖĘÁżˇ˘˛»Í¬ĂܶȵÄO2şÍO3ˇˇˇˇˇˇˇˇˇˇˇˇ BŁ®Í¬Î¶ȡ˘Í¬Ěĺ»ýµÄCOşÍN2
CŁ®Í¬Ěĺ»ýˇ˘Í¬ĂܶȵÄSO2şÍNO2ˇˇˇˇˇˇˇˇˇˇ DŁ®Í¬ŃąÇżˇ˘Í¬Ěĺ»ýµÄN2OşÍCO2ˇˇ
9. Éč°˘·üĽÓµÂłŁĘýÎŞNAŁ¬ÔňĎÂÁĐ˵·¨ŐýČ·µÄĘÇ(ˇˇ )
Aˇ˘łŁÎÂĎÂŁ¬2.7 gÂÁÓë×ăÁżµÄÇâŃő»ŻÄĆČÜŇş·´Ó¦Ę§ČĄµÄµç×ÓĘýÎŞ0.3NA
ˇˇ ˇˇ BŁ®100 mL l molˇ¤LŁ1 Na2SO4ČÜŇşÖĐş¬SO42Ł¸öĘýÎŞ0.1NA
CŁ®1.7 g NH3ÖĐş¬µç×ÓĘýÎŞNA
DŁ®11.2 L CO2Óë8.5 g NH3Ëůş¬·Ö×ÓĘýĎŕµČ
8. °Ń×ăÁżµÄĚú·ŰͶČëµ˝ÁňËáşÍÁňËá͵ĻěşĎČÜŇşÖĐŁ¬łä·Ö·´Ó¦şóŁ¬ĘŁÓŕ˝đĘô·ŰÄ©µÄÖĘÁżÓëÔĽÓČëĚú·ŰµÄÖĘÁżĎŕµČŁ¬ÔňÔČÜŇşÖĐH+ şÍSO42- µÄÎďÖʵÄÁżĹ¨¶ČÖ®±ČĘÇ(ˇˇ )
ˇˇ ˇˇˇˇ ˇˇA. 2:7ˇˇˇˇˇˇˇˇˇˇˇˇˇˇ B. 3:8ˇˇˇˇˇˇˇˇˇˇˇˇˇˇ C.1:2ˇˇˇˇˇˇˇˇˇˇ ˇˇˇˇD. 1:4
ąúĽĘѧУÓĹѡ - Á·Ď°˛áÁбí - ĘÔĚâÁбí
şţ±±Ęˇ»ĄÁŞÍřÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨Ć˝Ě¨ | ÍřÉĎÓĐş¦ĐĹϢľŮ±¨×¨Çř | µçĐĹթƾٱ¨×¨Çř | ÉćŔúĘ·ĐéÎŢÖ÷ŇĺÓĐş¦ĐĹϢľŮ±¨×¨Çř | ÉćĆóÇÖȨľŮ±¨×¨Çř
ÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨µç»°Łş027-86699610 ľŮ±¨ÓĘĎ䣺58377363@163.com