
题目列表(包括答案和解析)
4、碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s)
下列说法错误的是
A.电池工作时,锌失去电子
B.电池工作时,电子由正极通过外电路流向负极
C.电池正极的电极反应式为:
2MnO2(s)+H2O(1)+2e-== Mn2O3(s)+2OH-(aq)
D.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g
3、M能层最多含有的轨道数为
A、3 B、 5 C、 7 D、 9
2、2008夏季奥运会将在我国举行,这次奥运会要突出“绿色奥运、科技奥运、人文奥运”的理念,其中“绿色奥运”是指
A.把环境保护作为奥运设施规划和建设的首要条件
B.严禁使用兴奋剂,使运动员公平竞争
C.所有奥运用品和食品全都是绿色的
D.奥运场馆建设均使用天然材料,不使用合成材料
1、下列化学用语正确的是
A.碳-12原子 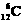 B.羟基的电子式 ∶
B.羟基的电子式 ∶ ∶H
∶H
C.硫离子的结构示意图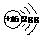 D.乙烯的结构简式CH2CH2
D.乙烯的结构简式CH2CH2
21.(10分稀硝酸和铜反应的化学方程式如下:
3Cu+8HNO3 =3Cu( NO3 )2+2NO+4H2O
(1)指出该氧化还原反应的氧化剂和还原剂,并用双线桥法表示出电子转移的方向和数目(在上面方程式中标出)。
(2)若生成标准状况下11.2LNO气体,计算参加反应的铜的质量以及反应中被还原的HNO3的物质的量。
20、 (6分)右图是医院病人输液使用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液标签,请认真观察标签上所列内容后填写:
(6分)右图是医院病人输液使用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液标签,请认真观察标签上所列内容后填写:
(1)该溶液中含水 g
(2)该溶液的密度约为 g/mL。
(3)该溶液的物质的量浓度为 。
18.(10分)有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、CaCl2、NaCl等混合组成,为了检验它们所含的物质,做了以下实验。
①将固体溶于水,搅拌后得到无色透明溶液;②往此溶液中滴加硝酸钡溶液,有白色沉淀生成;③过滤,将沉淀置于稀硝酸中,发现沉淀全部溶解。
(1)试判断:固体混合物中肯定含有____________,肯定没有_______________________,可能含有________________。
(2)对可能有的物质,可采用往滤液中滴加____________方法来检验,如果含有该物质,其现象是 ,反应的离子方程式为 。
17.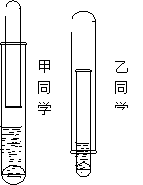 (10分)有一乡村中学由于条件有限,仅有一大一小两种试管和稀硫酸。甲、乙两个学生找来铝和废牙膏皮,各自设计了一种装置,制取并收集一试管氢气。
(10分)有一乡村中学由于条件有限,仅有一大一小两种试管和稀硫酸。甲、乙两个学生找来铝和废牙膏皮,各自设计了一种装置,制取并收集一试管氢气。
(1)哪个学生设计的装置比较合理? 。
另一个装置不合理的原因 。
(2)用较合理的装置制取氢气,要使氢气充满收集氢气的试管,
应该采取的措施是 。
(3)还可以用哪些物品代替牙膏皮和稀硫酸完成实验?
16.(8分)根据教材中的分类方法作答:
(1)根据交叉分类法,请用斜线将下面框图的酸与酸的分类连接起来:

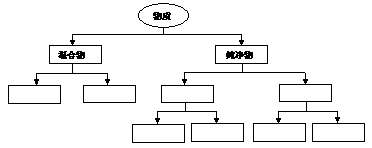
(2)根据树状分类法,请将:均匀混合物、非均匀混合物、有机化合物、无机化合物、单质、化合物、金属单质、非金属单质,填入下图的方框中。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com