
题目列表(包括答案和解析)
27. (8分)实验室欲配制500mL O.1 mol·L-1-CuS04溶液,请回答
(8分)实验室欲配制500mL O.1 mol·L-1-CuS04溶液,请回答
(1)应称取胆矾(CuSO4·5H2O) g。
(2)托盘天平使用前应首先调整零点,调整零点时游码应放在标尺的 (填
“左端”、“右端”或“中间”)。调节平衡螺母,使指针指向刻度盘的正中央或指针左右摆动幅度相等,若指针右偏,应将右侧平衡螺母往 (填“左”或“右”)旋。称量时应将腐蚀性的药品放入 中再称量。
(3)准确配制该溶液时,除天平(含附件)、烧杯、药匙、量筒、胶头滴管外,还必须用到的仪器有 。
 25.(4分)有一包白色粉末由Na2CO3、KCI、KNO3、AgNO3中的两种
25.(4分)有一包白色粉末由Na2CO3、KCI、KNO3、AgNO3中的两种
化合物组成,为测定其组成,完成了以下实验:
(1)在焰色反应时,透过监色钴玻璃观察到紫色;(2)加足量水溶解后,有沉淀生
成。此白色粉末由 和 组成,有关反应的离子方程式为 。
26.(7分)由甲元素的单质蒸气制得的电光源已被大量应用到道路雨
 广场的照明和航标灯。甲单质存在如图关系。
广场的照明和航标灯。甲单质存在如图关系。
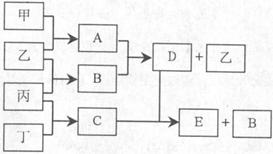
其中甲、乙、丙、丁为单质,A-E为化合物。
常温下,B为液态:乙、丙、丁为气态。丁单质显黄绿色。
(1)试推断(填化学式)甲: ,A: ,E: ,
(2)写出向D溶液中通入少量CO2反应的化学方程式:
。
(3)将丁通入到滴有石蕊试液的B中,可观察到的现象是
24. (6分)(1)13.8g氮的氧化物(NOx中含氮原子0. 3mol,),则NOx的摩尔质量为 ,x的数值为 ,该质量
(6分)(1)13.8g氮的氧化物(NOx中含氮原子0. 3mol,),则NOx的摩尔质量为 ,x的数值为 ,该质量
的NOx在标准状况下的体积为 L。
(2)现有100mL0.1mol·L-1A12(SO4)3溶液,取山l0mL,则C(SO4)为 mol·L-
n(Al3+)的量浓度为 mol;若将该10mL溶液加水稀释至500mL,所得硫酸铝溶液的物质的量浓度为mol l·L-1。
23. (7分)
(7分)
(1)写出钠盐与盐酸反应的离子方程式: ,
其中还原剂是 。
(2)实验室制取氯气的化学方程式为: ,
若在标准状况下生成448mL的氯气,则被氧化的化台物质量为 g,转移电
子 mol。
22.4
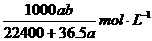
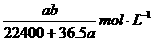 C. D.
C. D.
唐山市2008-2009学年度高一第一次教学质量检测
化 学 试 卷
卷II (非选择题,共47分)
22.将标准状况下的口LHCI气体溶于1000mL水中,得到的盐酸密度为b g·cm-3,则该
盐酸的物质的量浓度为
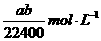 A.
A.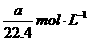 B.
B.
21.同温同压下,相同质量的S02(气体)和S03(气体)相比较,下列有关叙述正确的是
①它们所含的分子数目之比为4:5②它们所含的氧原子数目之比为5:6③它们所
含的原子总数之比1:1④它们所含的硫原子数目之比为5:4⑤它们的密度之比为4:5
A.②③⑤ B.①④⑤ C.②④⑤ D.①②⑤
20.配制一定体积、一定物质的量浓度的溶液时,下列情况可能使溶液浓度偏小的是
A.容量瓶中原有少量蒸馏水
B.溶液从烧杯转移到容量瓶后没有洗涤烧杯
C.定容时观察液面俯视
D.溶解固体后未冷却至室温即定容
19.用NA表示阿伏加德罗常数,下列说法不正确的是
A.在常温常压下,lmol氦气含有的原子数为N。
B.32g氧气和32g臭氧所含原子数均为2N。
C.在常温常压下,16g甲烷所含电子数为8N^
D.在标准状况下,2.24L二氧化碳与二氧化硫混合气体中所含分子数约为0.1NA
18.已知X2、Y、Z2存在如下下列反应:
(1)X2+Y2--Y+2X-;(2)Z2+2X--2Z+X2:(3)Y+H2-H2Y:由上述反应可知,氧化性由强到弱的顺序是
A.x2>Y> Z2>H2 B.Y>X2>H2>Z2
C.Y>X2>Z2>H2 D.Z2>X2>Y>H2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com