
题目列表(包括答案和解析)
1.假说:是以 为依据,面对
所提出的一种 。假说提出后须得到 ,才能成为
。


 2.模型:是以
为依据建立起来的,是对
的简化模拟。模型一般可分为
和
两大类。
2.模型:是以
为依据建立起来的,是对
的简化模拟。模型一般可分为
和
两大类。
 名师讲题
名师讲题
模块一、研究物质性质的基本方法和基本程序
 例1.按图2-5所示的方法研究某气体的性质,这种方法属于( )
例1.按图2-5所示的方法研究某气体的性质,这种方法属于( )
A.实验法 B.观察法
C.分类法 D.比较法
解析:这是用鼻子闻气体的气味,这样的方法属于观察法。
答案:B
评析:观察一般包括看、闻、听、摸等四种动作。 图2-5
[自主研学]:
3.Cl2跟碱液的反应
[自主研学]:
将氯气通入到碱液中可制得次氯酸盐,次氯酸盐是一些漂白剂和消毒剂的有效成分。
(1).漂白粉的制取:
2Cl2+2Ca 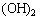 =
=
漂白粉的主要成分 和 ,有效成分 。 漂白原
理(用方程式表示): 。漂白粉在空气中放置过长,会与空气中的CO2和H2O反应生成HClO,HClO分解就会导致漂白粉失效,有关反应的方程式:
由此,说明HClO的酸性比H2CO3的酸性 (强或弱)。
(2).“84”消毒液的制取:
Cl2+2NaOH= ,漂白、消毒、杀菌的原理
(用化学方程式表示): 。
特别提示:
具有漂白性的物质有:活性炭、Na2O2 、HClO 、ClO2
[质疑激趣]:通过观察和实验认识了物质的性质后,人们往往要探究产生相关性质的原因,这就要涉及物质结构方面的问题,这些问题仅通过一般实验无法解决的,还需要利用模型,假说等方法进行有关研究。
2.氯气的特性--氯气跟水的反应
(1).预测氯气可能与水反应
(2).实验设计:①.取三支盛氯水的试管,
分别向其中加入镁条、石蕊溶液、硝酸银溶液, 图2-3
观察现象(如图2-3)。
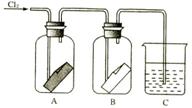 ②.将干燥的氯气依次通过盛有干燥红纸条
②.将干燥的氯气依次通过盛有干燥红纸条
的集气瓶A中和盛有湿润红纸条的集气瓶B中,
观察现象(如图2-4)。
 图2-4
图2-4
(3).实验记录:
|
实验内容 |
实验现象 |
实验结论 |
|
氯水与镁 |
生成气体 |
氯水中含酸 |
|
氯水与石蕊溶液 |
先变红后褪色 |
氯水中含酸,也含有漂白性物质 |
|
氯水与硝酸银溶液 |
生成白色沉淀 |
氯水中含有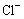 |
|
氯气与干燥红纸条 |
红纸条不褪色 |
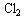 无漂白作用 无漂白作用 |
|
氯气与湿润红纸条 |
红纸条褪色 |
 和H2O的反应产物有漂白作用 和H2O的反应产物有漂白作用 |
(4).整合结论:
①.Cl2不仅能溶解于水,还能与水反应生成盐酸和次氯酸, 具有漂白性,反应的化学方程式是: 。
②.新制取的氯水中含有的微粒:分子: 、 、 ;
离子:
、
、 。(由于HClO见光易分解:2HClO 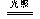 2HCl+O2↑,久置的氯水变成稀盐酸)
2HCl+O2↑,久置的氯水变成稀盐酸)
[质疑激趣]:Cl2跟水反应生成两种酸,则Cl2是否也与碱液反应?
3.实验探究氯气的化学性质
(1).与金属的反应
[操作探究]:把烧得红热的一束细铁丝伸入充满氯气的集气瓶中,观察现象;然后向集气瓶中加入少量的水,振荡,观察溶液的颜色。
[实验现象]:细铁丝在氯气中燃烧,充满红棕色的烟,加入少量的水,溶液呈黄色。反应的化学方程式: 。
特别提示:
氯气与可变价的金属发生反应时,生成金属的高价氯化物。如:氯气与铁和铜的反应,
反应的化学方程式:3Cl2+2Fe  2FeCl3; Cl2+Cu
2FeCl3; Cl2+Cu  Cu Cl2
Cu Cl2
(2).与非金属的反应
[操作探究]:在空气中点燃氢气,然后导气管伸入盛满氯气的集气瓶中,观察氢气在氯气中燃烧时发生的现象。
[实验现象]:氢气在氯气中安静的燃烧,发出苍白色的火焰,在瓶口处生成大量的白雾。反应的化学方程式: 。
特别提示:
燃烧是可燃物与氧气发生的发光发热的剧烈的氧化反应,燃烧的条件是温度达到着火点和必须有氧气参加。但铁、铜等金属与氢气等非金属在氯气中也燃烧,同样也是发光发热的剧烈的氧化反应,因此,燃烧的概念将扩大化为:任何发光发热的剧烈的氧化反应。故:在以后,燃烧的条件中并不一定有氧气参加。
 [质疑激趣]:除了上述与氧气类似的性质外,氯气还具有什么特性呢?
[质疑激趣]:除了上述与氧气类似的性质外,氯气还具有什么特性呢?
2.预测氯气的化学性质
[自主研学]: 图2-2
氯气是一种非常 的非金属单质,它可以与 、 等金属反应,还可以与非金属单质 反应。
 [质疑激趣]:研究物质性质的基本程序,怎样应用到具体物质上?
[质疑激趣]:研究物质性质的基本程序,怎样应用到具体物质上?
1.认识氯气的物理性质
[操作探究]:(1).取一只盛满氯气的集气瓶,观察氯气的颜色;
 稍打开玻璃片,用手轻轻地在瓶口煽动,仅使极少量的氯气飘
稍打开玻璃片,用手轻轻地在瓶口煽动,仅使极少量的氯气飘
进鼻孔,闻氯气的气味(如图2-1)。 图2-1
 (2).取一支盛满氯气的试管,将其倒扣在水槽中,
(2).取一支盛满氯气的试管,将其倒扣在水槽中,
静置一段时间后,观察现象。(如图2-2)
[实验结论]:氯气是 色,具有 气味的
体,具有 性,密度比空气 (填大或小),
溶解性 (填能或否)溶于水。
4.解释及结论。需要对实验现象进行 、 、推论,概括出
。一般运用 的方法,归纳出物质的 及 ,并
实验结论。
3.实验和观察。根据预测进行 并 ,然后通过对实验现象的 , 出与预测一致的性质;如果实验中出现预测以外的特殊现象,则需要进一步 ,提出 和做出 ,并再进行
,验证 。
2. 物质的性质。运用 的方法,根据 或
预测物质的性质。
[质疑激趣]:人们对物质性质的研究就是一种科学探究的过程,在探究物质性质时,运用基本方法的同时,也运用了研究物质性质的基本程序,基本程序有是怎样?
[自主研学] :
1. 物质的外观性质。了解物质存在的 、 、
等。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com