
题目列表(包括答案和解析)
15.下列离子方程式正确的是( )
A.锌和硝酸亚铁溶液反应: Zn+Fe2+=Zn2++Fe
B.氢氧化镁与硫酸溶液反应: OH-+H+=H2O
C.碳酸钙与醋酸溶液反应:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑
D.铁与稀硫酸反应: 2Fe+6H+=2Fe3++3H2↑
14.配制一定物质的量浓度的KOH溶液时,造成实验结果偏低的原因是 ( )
A.容量瓶中原有少量蒸馏水 B.洗涤烧杯和玻璃棒的洗涤液未转入容量瓶中
C.定容时俯视 D.定容时仰视
13.由(NH4)2SO4和MgSO4组成的混合物共192g,溶于水中配成10L溶液。测得此溶液中c(SO42-)=0.15 mol/L,则原混合物中NH4+离子的物质的量是( )
A.0.1mol B.0.5mol C.1mol D.2mol
12.能用“Ba2+ + SO42- = BaSO4↓”表示的反应是( )
A.硫酸钾与氢氧化钡反应 B.硫酸与氢氧化钡反应
C.硫酸与硝酸钡反应 D.硫酸与碳酸钡反应
11.12C相对原子质量为12,12C原子的质量为bg,A原子的质量为ag,NA为阿伏加德罗常数的值,则A的相对原子质量的表达式为( )
A.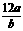 B.
B.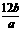 C.
C.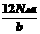 D.NAa
D.NAa
10.血红蛋白的相对分子质量约为68000,已知其中含铁0.33%,则平均每个血红蛋白的分子中铁原子数约为( )
A.5 B.4 C.3 D.2.408×1024
9.在相同的温度和压强下,A容器中的H2和B容器中的NH3所含的原子数相等,则A、B两容器的容积比为( )
A.2:1 B.1:2 C.2:3 D.1:1
8.CaCl2溶解在1mol H2O中,使Cl-与H2O分子的物质的量之比为1:10时,CaCl2为( )
A.0.1mol B.10mol C.0.5mol D.0.05mol
7.下列叙述中正确的是( )
A.碘在酒精中的溶解度很大,所以可以用酒精萃取碘水
B.滤纸不能用来过滤强酸、强碱是因为强酸、强碱有腐蚀性
C.往溶液中滴加氯化钡,有白色沉淀生成,说明溶液中有硫酸根离子
D.蒸发中要等全部蒸干才可停止加热
6.下列混合物能够用过滤法分离的是( )
A.汽油和水 B.食盐和蔗糖 C.泥沙和食盐 D.铜粉和铝粉
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com