
题目列表(包括答案和解析)
25. (8分) 研究性学习小组进行SO2的制备及性质探究实验。
根据反应Na2SO3(固)+H2SO4(浓)= Na2SO4 + SO2↑+ H2O,制备SO2气体。
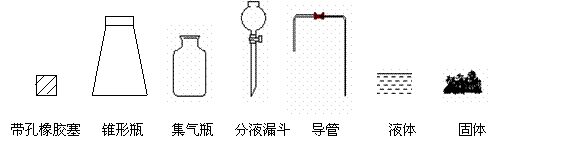
(1)在下图方框中画出制备并收集SO2的实验装置示意图:


(2)将SO2气体分别通入下列溶液中:
①品红溶液,现象是 ;
②溴水溶液,现象是 ;
③硫化钠溶液,现象是________________________________________________。
24.(8分)在通常情况下,A是固体单质,A、B、C、D、E五种物质均含有一种元素,它们的相互关系如图所示。

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
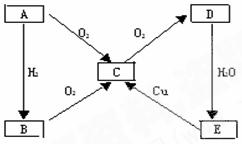
(1)写出A、B、D、E的化学式:
A: B: D: E: 。
(2)完成下列转化的化学反应方程式:
 B C :
,
B C :
,
 E
C:
。
E
C:
。
23.(6分)有A、B、C、D四种元素,A元素形成的-2价阴离子比氦的核外电子数多8,B元素的一种氧化物为淡黄色固体,该固体遇到空气能生成A的单质.C为原子核内有12个中子的二价金属,当2.4g C与足量热水反应时,在标准状况下放出H2 2.24升,D的M层上有7个电子。据此推断:
(1)A元素是 ,D元素是
(填元素符号)

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
(2)写出B、C、D最高价氧化物对应水合物的分子式,并比较其酸碱性。
B : C: D: 。
其酸碱性: 。
(3)比较D的气态氢化物与H2S、HF的稳定性:
。
22.(8分)下表是周期表的一部分:

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
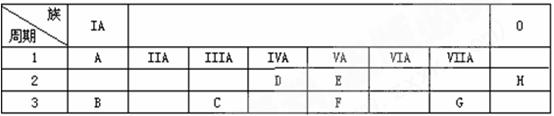 (1)写出A---H的相应的元素符号:D F 。
(1)写出A---H的相应的元素符号:D F 。
(2)根据A-H 元素在周期表中的位置,选用适当的分子式,填入有关的空白:
①氧化性最强的单质是 ,还原性最强的单质是 。
②最高价氧化物对应水化物酸性最强的物质是
。

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
③G的单质与B的氢氧化物的水溶液反应的离子方程式是 。
④按碱性逐渐减弱、酸性增强的顺序,将B、C、E、F、G五种元素的最高价氧化物的水化物分子式排列顺序是: 。
21.(6分)高一化学教材里描述:“过氧化氢(H2O2)是一种粘稠的液体,其水溶液又名双氧水,具有氧化性和弱酸性。”
(1)过氧化氢的电子式为 .
(2)实验室里可以用过氧化氢来快速制备氧气,写出反应方程式 .
(3) 过氧化氢(H2O2)的酸性与碳酸类似,写出过氧化氢(H2O2)电离的离子方程式:
.
(4)下列反应说明过氧化氢的氧化性的是 ;说明过氧化氢的酸性的是 .(填番号)
A.在过氧化氢溶液中投入镁条,有可燃性气体产生。

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
B.医院里用过氧化氢溶液来杀菌消毒。
C.在SO2 + H2O2 = H2SO4中
D.Ag2O + H2O2 =2Ag + O2 ↑ + H2O
20.下列离子方程式中,正确的是 ( )
A.K2CO3 + 2H+ = 2K+ + CO2 ↑ + H2O
B.BaCO3 + 2H+ = Ba2+ + CO2 ↑ + H2O
C.Cu + 2H+ = Cu2+ + H2↑
D.Ba2+ + OH- +
H+ + SO42- = BaSO4↓
+ H2O[

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
19.在2H2S + SO2 = 3S + 2H2O反应中,被氧化的元素与被还原的元素间的质量比是( )
A. 1:1 B. 1:2 C. 2:1 D.1:3
18.检验Na2SO3是否被氧化所用的试剂为 ( )
A.BaCl2和HCl B.Ba(NO3)2和HNO3
C.Ba(OH)2和HCl
D. Ba(NO3)2和HCl

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
17.在体积为V L 的密闭容器中,通入 a mol NO ,b mol O2 ,反应后容器内N原子和O原子数之比为( )
A a/ b B a /( a+2b)
C a/2b D a/ 2(a+b)
16.下列各组离子在溶液中能同时大量共存,并且溶液呈无色的是( )

 w_w w. k#s5_u.c o*
w_w w. k#s5_u.c o*
A K+ Al3+ NO3- AlO2- B Cu2+ Al3+ Cl- NO3-
C Mg2+ Na+ Cl- NO3- D K+ H+ MnO4- SO42
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com