
题目列表(包括答案和解析)
12.环保检测中,有害气体的浓度常用1L有害气体的毫克值(mg/L)来表示,如对某气体样品中所含一氧化碳的浓度进行测定,其方法和实验步骤如下:
①首先将2.00 L的气体样品通过盛有I205固体的加热管,反应后生成C02和I2;
②用30.0mL 5.00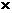 10
10 mol/L的硫代硫酸钠溶液吸收所产生的碘,发生的反应为:
mol/L的硫代硫酸钠溶液吸收所产生的碘,发生的反应为:
I2+2S20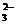 ==2I
==2I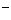 +S4O
+S4O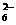 。
。
③从②中溶液取出1/5,加入1.00 mL1.00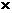 10
10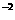 mol/L碘水,正好将所取溶液中过量的硫代硫酸钠完全氧化。
mol/L碘水,正好将所取溶液中过量的硫代硫酸钠完全氧化。
(1)写出步骤①中CO通过盛I205加热管的有关反应的化学方程式。
(2)计算样品中CO的浓度。
答案与解析
11. 有效地利用现有能源和开发新能源已受到各国的普遍重视。
(1)可用改进汽油组成的办法来改善汽油的燃烧性能。例如,加入CH30C(CH3)3来生产“无铅汽油”。 CH30C(CH3)。分子中必存在的原子间连接形式有 (填写编号)
①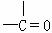 ②
②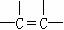 ③
③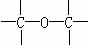 ④
④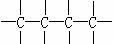
(2)天然气的燃烧产物无毒、热值高,而且管道输送方便,将成为我国西部开发的重点项目之一。天然气常和石油伴生,其主要的成分是 。能说明它是正四面体而非正方形平面结构的理由是 (填写编号)。
①其一氯取代物不存在同分异构体 ②其二氯取代物不存在同分异构体
③它是非极性分子 ④它的键长和键角都相等
(3)1980年我国首次制得一辆燃烧氢气的汽车,乘员12人,以50 km/h行驶了40km。为了有效开展民用氢能源,首先必须制得廉价的氢气,下列可供开发又较经济的制氢方法是 (填写编号)。
①电解水②锌和稀硫酸反应③光解海水
其次,制得纯氢气后还需要解决的问题是 (写出其中一个)。
10.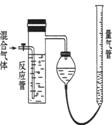 工业上测量S02、N2、O2混合气体中S02含量的装置如右图。反应管中装有碘的淀粉溶液。S02和I2发生的反应为(N2、02不与I2反应):
工业上测量S02、N2、O2混合气体中S02含量的装置如右图。反应管中装有碘的淀粉溶液。S02和I2发生的反应为(N2、02不与I2反应):
SO2+I2 +2H20==H2SO4+2HI
(1)混合气体进入反应管后,量气管内增加的水的体积等
于 的体积(填写气体的分子式)。
(2)反应管内的溶液蓝色消失后,没有及时停止通气,则测得的S02含量 (填“偏高”、“偏低”或“不受影响”)。
(3)反应管内的碘的淀粉溶液也可以用 代替(填写物质名称)。
(4)若碘溶液体积为V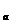 mL,浓度为cmol·L
mL,浓度为cmol·L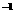 。N2与02的体积为V
。N2与02的体积为V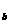 mL(已折算为标准状况下的
mL(已折算为标准状况下的
体积)。用c、V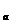 、V
、V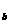 表示SO2的体积百分含量为:
。
表示SO2的体积百分含量为:
。
(5)将上述装置改为简易实验装置,除导管外,还需选用的仪器为 (选下列仪器的编号)。
a.烧杯b.试管c.广口瓶d.容量瓶巴量筒 f.单孔塞g.双孔塞
9.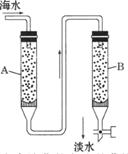 随着现代科学的不断发展,生产和生活所需淡水日益增多,甚至超过人类所能支配的淡水量,使地球上淡水资源发生危机,这就把海水淡化问题提到了科学家的面前。磺化媒(代表式NaR)是一种钠型离子交换树脂,它能使海水中的Ca
随着现代科学的不断发展,生产和生活所需淡水日益增多,甚至超过人类所能支配的淡水量,使地球上淡水资源发生危机,这就把海水淡化问题提到了科学家的面前。磺化媒(代表式NaR)是一种钠型离子交换树脂,它能使海水中的Ca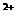 、Mg
、Mg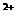 交换除去。
交换除去。
现代海水的淡化方法:使海水按顺序通过两种离子交换树脂,其流程如图所示。
(1)最早用于海水淡化的方法是蒸馏法,其原理是 。
(2)现有氢型阳离子交换树脂(HR)和羟型阴离子交换树脂(ROH),则离子交换柱中应分别装入的离子交换树脂(填其代表式)为:A柱 ,B柱 。
(3)说明按上述顺序装柱的理由是 。
8.准确称取某种铁的氧化物2.88 g,用足量的CO进行还原,将生成的C02全部用足量的澄清石灰水吸收,得到沉淀4g,则这种铁的氧化物为 ( )
A.Fe3O4 B.Fe203 C.FeO D.以上都不是
7.“飘尘”是物质燃烧时产生的粒状飘浮物,颗粒很小(直径小于10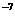 m),不易沉降(可飘浮数小时甚至数年),它与空气中S02、O2接触时,SO2部分转化为S03,使空气酸度增加,形成酸雨。飘尘所起的主要作用是
( )
m),不易沉降(可飘浮数小时甚至数年),它与空气中S02、O2接触时,SO2部分转化为S03,使空气酸度增加,形成酸雨。飘尘所起的主要作用是
( )
A.氧化剂 B.还原剂 C.吸附剂 D.催化剂
6.汽车排放的尾气中因含有氮的氧化物而污染大气。产生氮的氧化物的主要原因是 ( )
A.燃烧含氮的化合物燃料引起的 B.燃烧含铅汽油引起的
C.是由燃烧不充分引起的 D.是在汽缸中N2被氧化生成的
5.人造光卤石(KCl·MgCl2·6H20)是盐化工生产的中间产物。以光卤石为原料制得金属镁,可有下列步骤:
①过滤 ②溶解 ③加入适量Ca(OH)2 ④蒸发 ⑤用盐酸溶解 ⑥电解熔融MgCl2
⑦在HCl气流中强热MgCl2·6H20晶体正确的顺序是 ( )
A.⑤③①②④⑥⑦ B.②③①⑤④⑦⑥
C.②④①③⑦⑤⑥ D.⑤③①④②⑦⑥
4.下列转化不属于煤或石油的综合利用的是 ( )
A.将煤干馏制得煤焦油和焦炭
B. 在一定条件下将煤与氢气转化为液体燃料
C. 将煤变为煤饼作燃料
D.将石油裂解制得乙烯等化工原料
3.下列氧化物不能跟铝粉组成铝热剂的是 ( )
A.W03 B.MnO2 C.MgO D.V205
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com