
题目列表(包括答案和解析)
15.用惰性电极实现电解,下列说法正确的是( )
A.电解稀硫酸溶液,实质上是电解水,故溶液H+ 浓度不变
B.电解稀氢氧化钠溶液,要消耗OH-,故溶液H+ 浓度增大
C.电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1∶2
D.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1∶1
[解析]选D。电解稀H2SO4,实质上是电解水,硫酸的物质的量不变,但溶液体积减少,浓度增大,故溶液H+ 浓度增大。电解稀NaOH溶液,阳极消耗OH-,阴极消耗H+,实质也是电解水,NaOH溶液浓度增大,故溶液的H+ 浓度减小。电解Na2SO4溶液时,在阳极发生反应:4OH--4e- ====2H2O+
O2↑,在阴极发生反应:2H+
+2e-
====H2↑,由于两电极通过电量相等,故放出H2与O2的物质的量之比为2∶1,电解CuCl2溶液 时,阴极反应为Cu2+ +2e- ====Cu,阳极反应为2Cl--2e- ====Cl2↑,两极通过电量相等时,Cu和Cl2的物质的量之比为1∶1。
时,阴极反应为Cu2+ +2e- ====Cu,阳极反应为2Cl--2e- ====Cl2↑,两极通过电量相等时,Cu和Cl2的物质的量之比为1∶1。
第Ⅱ卷(非选择题 共55分)
14.(多选)下列化合物,苯环上的氢原子被溴原子取代,所得一溴代物有三种同分异构体的是( )
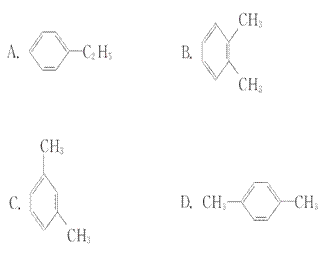
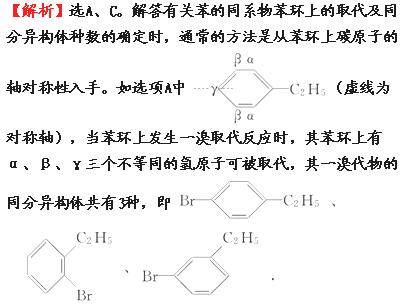
同理分析B、C、D三个选项易知它们苯 环上一溴代物的同分异构体数目分别为2种、3种、1种。
环上一溴代物的同分异构体数目分别为2种、3种、1种。
13.在一定温度下,反应:2A(s)+2B(g)  C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是( )
C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是( )
A.容器内的压强不随时间而变化
B.混合气体的密度不再随时间而变化
C.A的质量不再改变
D.平衡混合气体的平均相对分子质量不再改变
[解析]选A。所给反应是一个反应前后气体物质的量不变的反应,所以压强不变不是反应达到平衡的标志。选A。
12.(2009·海南高考)同一短周期的元素W、X、Y、Z的原子序数依次增加,下列叙述正确的是( )
A.单质的化学活泼性:W<X<Y<Z
B.原子最外层电子数:W<X<Y<Z
C.单质的氧化能力:W<X<Y<Z
D.元素的最高化合价:W<X<Y<Z
[解析]选B。本题中元素为同一周期,从左至右最外层电子数依次增加。而单质的活泼性分金属与非金属,氧化能力随着单质晶体形态及分子内的化学键不同有变化,最高化合价随原子序数的递增而增加,有特例(O、F无正价)。
11.下列变化过程中,无化学键断裂或生成的是( )
A.石墨转化为金刚石
B.NaCl晶体溶于水
C.干冰升华
D.HCl溶于水
[解析]选C。A.石墨与金刚石属于不同的单质,故转化过程中既断裂共价键,又生成共价键。B.NaCl晶体溶于水,发生电离NaCl====Na+ +Cl-,断裂离子键。C.干冰升华,CO2分子间距离增大,破坏分子间作用力,不破坏化学键。D.HCl溶于水,发生电离HCl===H+ +Cl-,断裂共价键。
10.下列对指定电极的反应式书写不正确的是( )
A.铜锌(稀硫酸作电解质溶液)原电池的正极: Zn-2e- ====Zn2+
B.钢铁发生电化学腐蚀的负极:Fe-2e- ====Fe2+
C.电解CuCl2溶液的阳极:2Cl--2e- ====Cl2↑
D.电解熔融氧化铝的阴极 :Al3+ +3e- ====Al
:Al3+ +3e- ====Al
[解析]选A。铜锌原电池的正极发生还原反应,电极反应式为:2H+ +2e- ====H2↑。
9.“化学反应的绿色化”要求原料物质中所有的原子被安全利用且全部转入期望的产品中。下列符合“化学反应的绿色化”的是( )

[解析]选C。原子利用率为100%,是绿色化学的目标,A、B两项反应物没有全部转化为所需产物。D项中要保证稀硫酸和铁屑过量,故只有C项正确。
8.用一定体积、一定浓度的稀硫酸和过量的锌反应,制取一定体积的氢气,要提高反应速率而又不改变生成氢气的体积,下 列措施中合理的是(
)
列措施中合理的是(
)
A.加少量稀盐酸
B.加入一定量的ZnSO4溶液
C.加水
D.加少量蓝矾晶体
[解析]选D。D选项加入蓝矾晶体后,将形成原电池,反应速率加快,其他各选项均不符合题意。
7.某有机物的结构简式为 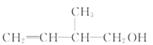
下列关于该有机物的叙述不正确的是( )
A.能与金属钠发生反应并放出氢气
B.能在催化剂作用下与H2发生加成反应
C.能发生银镜反应
D.可以发生酯化反应
[解析]选C。该有机物中含有-OH故能与Na反应产生H2,可以与酸发生酯化反应,A、D正确。该有机物含有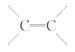 与H2发生加成反应
与H2发生加成反应 ,B正确。该有机物不含
,B正确。该有机物不含
-CHO,故C错误。
6.(2009·上海高考)1- 丁醇和乙酸在浓硫
酸作用下,通过酯化反应制得乙酸丁酯,反应
温度为115 ℃-125 ℃,反应装置如图。下列
对该实验的描述错误的是( )
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D.加入过量乙酸可以 提高1-
丁醇的转化率
提高1-
丁醇的转化率
[解析]选C。该酯化反应需要的温度为115 ℃-1 25 ℃,水浴的最高温度为100 ℃,A项正确。长导管可以起到冷凝回流的作用,B项正确。乙酸丁酯在氢氧化钠溶液中容易发生水解,C项错。在可逆反应中,增加一种反应物浓度可以提高另一种反应物的转化率,D项正确。
25 ℃,水浴的最高温度为100 ℃,A项正确。长导管可以起到冷凝回流的作用,B项正确。乙酸丁酯在氢氧化钠溶液中容易发生水解,C项错。在可逆反应中,增加一种反应物浓度可以提高另一种反应物的转化率,D项正确。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com