
题目列表(包括答案和解析)
7、全部由第二周期元素形成的化合物是
A.Na2O B.H2O C.CO2 D.MgCl2
6、下列离子中核外电子排布不与氖原子相同的是
A.Cl- B.F- C.Al3+ D.Na+
5、下列叙述不正确的是
A.原子半径:H<Al<Mg<Na
B.热稳定性:HCl>H2S>PH3
C.P、S、Cl元素最高价氧化物对应的水化物酸性依次增强
D.N、O、F元素非金属性依次减弱
4、周期表中16号元素与4号元素的原子相比较,前者的下列数据是后者的4倍的是
A.K层电子数 B.最外层电子数
C.电子层数 D.次外层电子数
3、据报道,上海某医院正在研究用放射性同位素53125I治疗肿瘤。该同位素原子核内的中子数与核外电子数之差是
A.72 B.19 C.53 D.125
2、11H、12H、13H、H+、H2是
A.氢的五种同位素 B.五种氢元素
C.氢的五种同素异形体 D.氢元素的五种不同微粒
1、2008年北京奥运会火炬使用丙烷作燃料。丙烷属于
A.无机物 B.有机物 C.氧化物 D.混合物
26、(7分)粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:①取适量A进行铝热反应,产物中有单质B生成;②另取20g A全部溶于0.20L 4.5mol·L-1的盐酸中,得溶液C;③将①中得到的单质B和溶液C反应,放出1.12L(标准状况)气体,同时生成溶液D,还残留有固体物质B;④用KSCN溶液检验时溶液D不变色,请填空:
(1)①中发生的反应的化学方程式是______ _________________________________。
_________________________________。
(2)③中所发生的各反应的离子方程式是___________________________________。
(3)若溶液D的体积仍视为0.20L,计算溶液中Mg2+、Fe2+的浓度。
武汉二中2010--2011学年上学期高一年级期末考试
25、(8分)常见的非金属黄色晶体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,也能溶于强碱。E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶液吸收得到无色溶液F。溶液F在空气中长期放置与氧气发生反应,溶液呈强碱性,生成物之一为H。H的组成元素与F相同,其结构和化学性质与过氧化钠相似,溶液显黄色。
请回答下列问题:
(1)B与氢氧化钠溶液反应的化学方程式为: 。
(2)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯。该反应的氧化产物为 ,当生成2mol二氧化氯时,转移电子 mol。
(3)溶液F在空气中长期放置生成H的化学反应方程式为: 。
(4)H的溶液与稀硫酸反应产生的现象为 。
24、(6分)现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。F的水溶液为浅绿色。物质D的焰色为黄色。

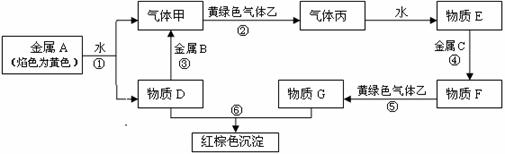
回答下列问题:
(1)写出下列物质的化学式:D 、丙 。
(2)向反应③的生成物溶液中滴加金属B的阳离子溶液会发生什么反应:
(用离子反应方程式表示)。
(3)描述F溶液中滴加D溶液后的现象 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com