
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
4ЃЎЩшNAБэЪОАЂЗќМгЕТТоГЃЪ§жЕЃЌЯТСаа№Ъіе§ШЗЕФЪЧ
AЃЎ54g H218OжаКЌгаЕчзгзмЪ§ЮЊ30NAИі
BЃЎ11.2L H2жаКЌгаЕФЕчзгЪ§ЮЊNAИі
CЃЎ23gNa+КЌгаЕФзюЭтВуЕчзгЪ§ЮЊNAИі
DЃЎ16gбѕЦјКЭ16gГєбѕКЌгаЕФКЫЭтЕчзгзмЪ§ОљЮЊ8NAЁЁЁЁ
3. ЯТСаБэЪОЮяжЪзщГЩЁЂНсЙЙЕФЛЏбЇгУгяе§ШЗЕФЪЧ
ЯТСаБэЪОЮяжЪзщГЩЁЂНсЙЙЕФЛЏбЇгУгяе§ШЗЕФЪЧ
 AЃЎЕЊЗжзгЕФНсЙЙЪНЃКNЁдN ЁЁЁЁЁЁЁЁBЃЎCl-ЕФНсЙЙЪОвтЭМЃКЁЁЁЁЁЁ
AЃЎЕЊЗжзгЕФНсЙЙЪНЃКNЁдN ЁЁЁЁЁЁЁЁBЃЎCl-ЕФНсЙЙЪОвтЭМЃКЁЁЁЁЁЁ
CЃЎNaClЕФЕчзгЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ8ИіжазгЕФЬМдзгЕФЗћКХЃК12C
2. ЯТСаЗДгІМШЪєгкбѕЛЏЛЙдЗДгІЃЌгжЪЧЮќШШЗДгІЕФЪЧ
AЃЎаПСЃгыЯЁСђЫсЕФЗДгІЁЁЁЁЁЁЁЁ ЁЁBЃЎМзЭщдкПеЦјжаШМЩеЕФЗДгІ
ЁЁ ЁЁCЃЎзЦШШЕФФОЬПгыCO2ЕФЗДгІЁЁЁЁЁЁ DЃЎBa(OH)2•8H2OОЇЬхгыNH4ClОЇЬхЕФЗДгІ
1.ШеБОЕие№в§Ц№ЕФКЫаЙТЉЃЌЗХЩфадЮяжЪжївЊЪЧCsКЭ131IЁЃЦфжаЙигкЦеЭЈ127Iгы131IЕФЫЕЗЈе§ШЗЕФЪЧ
A. 127Iгы131IЕФаджЪЯрЭЌЁЁЁЁЁЁЁЁЁЁ B. 127Iгы131IЛЅЮЊЭЌЮЛЫи
C. 127Iгы131IЪЧЭЌвЛжжКЫЫиЁЁЁЁЁЁЁЁ D.IгыClОљЪєVIIAзхЃЌIБШClЛюЦУ
27.(8Зж)ФГЮТЖШЪБЃЌдквЛИі2 LЕФУмБеШнЦїжаЃЌXЁЂYЁЂZШ§жжЮяжЪЕФЮяжЪЕФСПЫцЪБМфЕФБфЛЏЧњЯпШчЭМЫљЪОЁЃИљОнЭМжаЪ§ОнЃЌЪдЬюаДЯТСаПеАзЃК
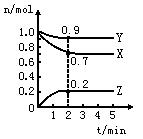 (1)ИУЗДгІЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЃ
(1)ИУЗДгІЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЃ
(2)ЗДгІПЊЪМжС2 minЃЌвдЦјЬхZБэЪОЕФЦНОљЗДгІЫйТЪЮЊЁЁЁЁЁЁЁЁ ЁЃ
(3)ШєXЁЂYЁЂZОљЮЊЦјЬхЃЌ2 minКѓЗДгІДяЕНЦНКтЃЌЗДгІДяЦНКтЪБЃКЂйДЫЪБЬхЯЕЕФбЙЧПЪЧПЊЪМЪБЕФЁЁЁЁЁЁЁЁЁЁЁЁ БЖЃЛ
ЂкДяЦНКтЪБЃЌШнЦїФкЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПБШЦ№ЪМЭЖСЯЪБ____________(ЬюЁАдіДѓЁБЁАМѕаЁЁБЛђЁАЯрЕШЁБ)ЁЃ
ЬЦЩНвЛжа2010-2011бЇФъЖШЕкЖўбЇЦкЦкжаПМЪд
26. (9Зж)ЂХЧтЦјЪЧвЛжжРэЯыЕФаТФмдДЃЌгыЛЏЪЏШМСЯЯрБШЃЌЧтФмдДгаФФШ§ДѓгХЕу_____________ЁЂЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ _________ЁЁЁЁЁЁЁЁ ЁЂЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЂЦ 4 gМзЭщдкбѕЦјжаШМЩеЩњГЩCO2КЭвКЬЌЫЎЃЌЗХГі222.5 KJШШСПЃЌаДГіМзЭщШМЩеЕФШШЛЏбЇЗНГЬЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)В№ПЊ1mol HЃHМќЁЂ1mol NЃHМќЁЂ1mol NЁдNМќЗжБ№ашвЊЕФФмСПЪЧ436 kJЁЂ391 kJЁЂ946 kJЃЌдђКЯГЩАБЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊ__________________________________________ЁЃ
(4)вбжЊЃКH2 (g) + 1/2O2(g) == H2O (g)ЁЁ ЁїH = Ѓ241.8 KJ/mol ЃЛC (s) + O2(g) == CO2(g)ЁЁ
ЁїH = Ѓ393.5 KJ/molЃЛЯжга0.2 molЕФЬПЗлКЭЧтЦјзщГЩЕФаќИЁЦјЃЌвђЛьКЯЮядкбѕЦјжаЭъШЋШМЩеЃЌЙВЗХГі63.53 KJШШСПЃЌдђЛьКЯЮяжаCгыH2ЕФЮяжЪЕФСПжЎБШЮЊ________________ЁЃ
25.(7Зж)AЁЂBЁЂCЁЂDЫФжждЊЫиЃЌдзгађЪ§вРДЮдіДѓЃЌAдзгЕФзюЭтВуЩЯга4ИіЕчзгЃЛBЕФвѕРызгКЭCЕФбєРызгОпгаЯрЭЌЕФЕчзгВуНсЙЙЃЌСНдЊЫиЕФЕЅжЪЗДгІЃЌЩњГЩвЛжжЕЛЦЩЋЕФЙЬЬхEЃЌDЕФLВуЕчзгЪ§ЕШгкKЁЂMСНИіЕчзгВуЩЯЕФЕчзгЪ§жЎКЭЁЃ
(1)CРызгНсЙЙЪОвтЭМ ЁЁЁЁЁЁЁЁЁЃDдкжмЦкБэжаЮЛжУ ЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(2)аДГіEЕФЕчзгЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)AЁЂDСНдЊЫиаЮГЩЛЏКЯЮяЪє ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ(ЬюЁАРызгЁБЛђЁАЙВМлЁБ)ЛЏКЯЮяЁЃ
(4)аДГіDЕФзюИпМлбѕЛЏЮяЕФЫЎЛЏЮяКЭAЗДгІЕФЛЏбЇЗНГЬЪНЃК
ЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
24. (8Зж)ЯТБэЮЊдЊЫижмЦкБэжаЕФвЛВПЗжЃЌБэжаСаГі8жждЊЫидкжмЦкБэжаЕФЮЛжУЃЌАДвЊЧѓЛиД№ЯТСаЮЪЬтЁЃ
|
ЁЁЁЁ зх жмЦк |
ЂёA |
ЂђA |
ЂѓA |
ЂєA |
ЂѕA |
ЂіA |
ЂїA |
0 |
|
2 |
ЁЁ |
ЁЁ |
ЁЁ |
Ђм |
ЁЁ |
Ђо |
ЁЁ |
ЁЁ |
|
3 |
Ђй |
Ђк |
Ђл |
Ђн |
ЁЁ |
ЁЁ |
Ђп |
Ђр |
ЂХ дкЂй-ЂрдЊЫижаЛЏбЇаджЪзюВЛЛюЦУЕФдЊЫиЕФУћГЦЪЧЁЁЁЁЃЌН№ЪєадзюЧПЕФдЊЁЁ ЫиЕФУћГЦЪЧЁЁЁЁ ЁЁЁЃ
(2) ЂлЁЂЂмЁЂЂоШ§жждЊЫижаЕФдзгАыОЖзюаЁЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюдЊЫиЗћКХ)ЁЃ
(3) ЂйЁЂЂкЁЂЂлШ§жждЊЫиаЮГЩЕФРызгЃЌРызгАыОЖгЩДѓЕНаЁЕФЫГађЪЧЁЁЁЁЁЁЁЁ ЁЁ(гУРызгЗћКХЬюаД)ЁЃ
(4) ЂмгыЂоаЮГЩЕФЛЏКЯЮяЕФЕчзгЪНЮЊ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(5) ЂмгыЧтаЮГЩКЌЧтСПзюИпЕФЛЏКЯЮяЕФНсЙЙЪН________________________ЁЃ
(6) аДГіЂйКЭЂлСНжждЊЫиЕФзюИпМлбѕЛЏЮяЖдгІЕФЫЎЛЏЮяЯрЛЅЗДгІЕФРызгЗНГЬЪНЃК
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
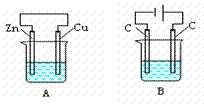
23.(12Зж)ШчЯТЭМЫљЪОЃЌAЁЂBСНИізАжУжаСНИіЩеБЗжБ№ЪЂгазуСПЕФCuSO4ШмвКЃК
 ЁЁ
ЁЁ
(1)AЁЂBСНИізАжУжаЪєгкдЕчГиЕФЪЧ_____(ЬюБъКХ,ЯТЭЌ)ЃЌЪєгкЕчНтГиЕФЪЧ____ЁЃ
(2)AГижаZnЪЧ___МЋ,ЗЂЩњ______(ЬюбѕЛЏЛђЛЙд)ЗДгІ,ЕчМЋЗДгІЪНЮЊ____________ЃЛ
CuМЋЕчМЋЗДгІЪНЮЊ_________________ЃЛAжазмЗДгІЕФРызгЗНГЬЪНЮЊ_______________
_______________________________________ЁЃ
(3)BГижазѓБпCЪЧ___МЋ,ЗЂЩњ______(ЬюбѕЛЏЛђЛЙд)ЗДгІ,ЕчМЋЗДгІЪН____________ЃЛ
гвБпCМЋЕчМЋЗДгІЪНЮЊ___________________________ЃЛBжазмЗДгІЕФЛЏбЇЗНГЬЪНЮЊ__________________________________________________ЁЃ
22.ФГбЇЩњЩшМЦСЫвЛИіЁАКкБЪаДКьзжЁБЕФШЄЮЖЪЕбщЁЃТЫжНЯШгУТШЛЏФЦЁЂЮоЩЋЗгЬЊЕФЛьКЯвКНўЪЊЃЌШЛКѓЦНЦЬдквЛПщВЌЦЌЩЯЃЌНгЭЈЕчдДКѓЃЌгУЧІБЪдкТЫжНЩЯаДзжЃЌЛсГіЯжКьЩЋзжМЃЁЃОнДЫЃЌЯТСаа№Ъіе§ШЗЕФЪЧ



A.ЧІБЪЖЫзїбєМЋЃЌЗЂЩњЛЙдЗДгІЁЁЁЁ B.ВЌЦЌЖЫзївѕМЋЃЌЗЂЩњбѕЛЏЗДгІ
C.ЧІБЪЖЫгаЩйСПЕФТШЦјВњЩњЁЁЁЁЁЁЁЁ D.aЕуЪЧИКМЋЃЌbЕуЪЧе§МЋ
ОэЂђ(ЗЧбЁдёЬтЁЁ ЙВ44Зж)
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com