
题目列表(包括答案和解析)
28、50ml0.2mol·L-1溶液与15g10%的H2SO4溶液(密度为1.9g·cm-3)混合,计算:
(1)生成沉淀的质量:
(2)反应结束后,溶液中剩余物质(酸或盐)的物质的量浓度(设溶液的总体积不变)。
27、在浓硝酸中入入铜片
(1)开始反应时产生的气体是________,或铜有剩余,则反应将要结束时产生的气体是________,待反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,该气体是________
(2)加入稀硫酸又产生气泡的原因是________。
(3)若将12.8g铜跟 一定量浓硝酸反应,铜消耗完时,共产生标准状况下的气体5.6L,则所消耗的硝酸的物质的量为________,所得气体的平均相对分子质量为________
26、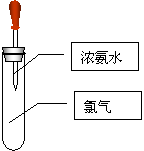
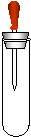 (9分)如图所示:试管中集满干燥的氯气,胶头滴管中装有供反应的足量浓氨水。滴入浓氨水,开始时试管内发生的反应有氧化还原反应:NH3 + Cl2 == N2 + HCl(未配平),并产生红光和白烟。请根据以上反应和现象回答下列问题:
(9分)如图所示:试管中集满干燥的氯气,胶头滴管中装有供反应的足量浓氨水。滴入浓氨水,开始时试管内发生的反应有氧化还原反应:NH3 + Cl2 == N2 + HCl(未配平),并产生红光和白烟。请根据以上反应和现象回答下列问题:
(1)标志反应全部完成的现象是________
(2)反应产生的白烟的主要成份是________

 (3)反应完毕后,将试管浸入水中并倒立,取下滴管,
(3)反应完毕后,将试管浸入水中并倒立,取下滴管,

 有水进入试管。在室温时,进入试管内的水约占
有水进入试管。在室温时,进入试管内的水约占
试管容积的________
25、(18分)如图是A~E五种相互转化关系图,其中A、B、C、D常温下均为气体,且A为单质,B为红棕色气体。
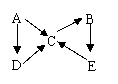 (1)写出C和E的化学式________,________。
(1)写出C和E的化学式________,________。
(2)写出A分子的电子式________。
(3)D的分子构型为________;
D转化为C的化学方程式为________。
(4)实验室制取C,只能用________法收集,制取D只能用________分收集,干燥D可用________。
24、(6分)某物质A为白色粉末,易溶于水。向A的溶液中加入AgNO3溶液,产生白色沉淀,再加稀硝酸沉淀不溶解。加取少量A物质的溶液,加入NaOH溶液,并加热,产生有刺激性气味的气体,该气体能使湿润的红色石蕊试纸变蓝,试回答:
(1)A的化学式是:________
(2)A与AgNO3溶液反应,A与NaOH溶液反应的离子方程式分别是:
________________________________、________________________________。
23、(6分)在一定温度下,把2molSO2和 1molO2 通入固定体积的密闭容器里,发生如下反应:
2SO2 + O2 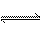 2SO3当此反应进行一定程度时,反应混合物就处于化学平衡状态。现在该容器中,维持温度不变,令a、b、c分别代表初始加入的SO2、O2、SO3的物质的量(mol)。如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的百分含量仍跟上述平衡时完全相同,请填写下列空白:
2SO3当此反应进行一定程度时,反应混合物就处于化学平衡状态。现在该容器中,维持温度不变,令a、b、c分别代表初始加入的SO2、O2、SO3的物质的量(mol)。如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的百分含量仍跟上述平衡时完全相同,请填写下列空白:
(1)C的最大值可等于________
(2)a、b、c取值必须满足的一般条件是(用二个方程式表示,其中一个只含a和c,另一个只含b和c):________________、________。
21、(4分)在一定条件下,RO3n-和F2可发生如下反应:RO3n- + F2 + 2OH-== = RO4- + 2F- + H2O,由此可得RO3n-中的n值为_____、R原子的最外层电子数为_________
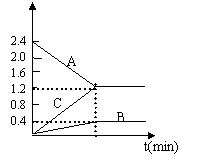
|
(1)该反应的反应物是:________
(2)该反应的化学方程式为:________
(3)若达到平衡状态的时间是2min,A物质的平均反应速率为________。
20、有下列几种粒子:OH-、Na+、NH4+、NH3、Mg2+、H+其中在溶液中能两两发生反应的共有:
A、四组 B、五组 C、六组 D、七组
19、氢阴离子(H-)能和NH3反应:H- + NH3== NH2- + H2 ,据此反应事实可以得出的正确结论是
A、NH3有还原性 B、H2为还原产物 C、H-是很强的还原剂 D、该反应属置换反应
18、在体积为VL的密闭容器中,通入amol和bmol ,反应后容器内N原子和O原子的物质的量之比为:
A、a/b B、a/(a + 2b) C、a/2b D、a/(2a + 2b)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com