
题目列表(包括答案和解析)
31. (20分)(1)(10分)下图表示人体内某些物质的转化过程。请回答下列问题:
(20分)(1)(10分)下图表示人体内某些物质的转化过程。请回答下列问题:
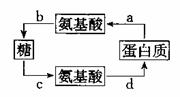
①蛋白质分子经a过程形成氨基酸时,所消耗的水中的氢参与形成氨基酸
的 (填基团)。
②b过程进行时必须首先发生的物质变化过程是 作用。当人体血糖浓度降低时,胰岛中的某种细胞产生的 可以促进b过程的进行。
③上图中 过程形成的氨基酸一定是非必需氨基酸。
④d过程进行的场所在细胞内的 上,此时氨基酸的排列顺序直接由 来决定。
(2)(10分)棉花的纤维有白色的,也有紫色的;植株有抗虫的,也有不抗虫的。为鉴别有关性状的显隐性关系,有人做了以下两组杂交试验,结果如下表。(假定控制两对性状的基因独立遗传;颜色和抗虫与否的基因可分别用A、a和B、b表示),请分析回答:
|
组合序号 |
杂交组合 |
子代的表现型和植株数目 |
|||
|
紫色不抗虫 |
紫色抗虫 |
白色不抗虫 |
白色抗虫 |
||
|
1 |
白色不抗虫(甲)×紫色不抗虫 |
753 |
251 |
762 |
248 |
|
2 |
白色不抗虫(乙)×紫色抗虫 |
0 |
0 |
1508 |
1529 |
①上述两对性状中, 是显性性状。
②杂交组合1的子代中出现白色抗虫和紫色抗虫植株的原因是 。
③杂交组合1的子代中白色不抗虫植株的基因型是 。
④若要利用亲本中的棉花品种获得可稳定遗传的白色抗虫棉,最简单的方法是:
。
⑤已知题中所给杂交组合1、2的亲本中A的基因频率为40%,若它们的子一代中所有个体全部存活无一被淘汰,则该子一代群体中a的基因频率是 。
30.(22分) (1)(10分)下图是生活在适宜环境中的C2植物光合作用部分过程图解,其中A、B、C表示三种化合物,a、b表示两个生理过程。
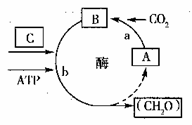
①该过程发生的场所在叶绿体的 。
②C物质既作为b过程进行时的还原剂,又为b过程进行提供 。
③形成ATP和C物质时需要的能量是由 将光能转换成的电能。
④若将植物突然转移到高温、强光照、干燥的环境中,叶片气孔将逐渐关闭,此时叶肉细胞内B物质含量的变化是 。
⑤将该植物的一叶片置于恒温的密闭小室,调节小室的CO2浓度,在适宜的光照条件下测定叶片光合作用的强度(以CO2的吸收速率表示),测定结果如下图:
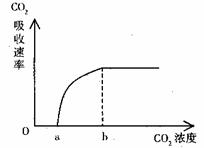
若降低光照强度后重新测定,请在原图中用虚线表示出最可能的测定结果。
(2)(12分)植物体所需要的矿质元素进入植物体后,有的仍然呈离子状态,可以转移再度利用;有的形成不够稳定的化合物,可以分解转移再利用;有的形成难溶解的稳定的化合物,不能被植物体再度利用。
①Mg元素是构成叶绿体中 的组成元素,缺乏该元素,植物叶片会呈现 色。
②某研究性学习小组想利用溶液培养法来探究叶绿体中含镁的色素是一种稳定的化合物还是不稳定的化合物。请帮助他们完成实验步骤和回答有关问题。
实验步骤:
第一步:配制 培养液。
第二步:选取 的植物若干,平均分成两组,将这两组植物分别置于盛有上述培养液的容器中。
第三步:将两组植物放在相同且适宜的条件下培养。
第四步:一段时间后观察 ,并做好记录。
预测结果及结论:
如果 ,则说明叶绿体中含镁的色素是一种不稳定的化合物。
如果 ,则说明叶绿体中含镁的色素是一种稳定的化合物。
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入12.2g苯甲酸和20ml甲醇(密度约0.79g·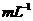 ),再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
),再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
(1)浓硫酸的作用是 ;
若反应产物水分子中有同位素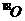 ,写出能表示反应前后
,写出能表示反应前后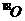 位置的化学方程式
位置的化学方程式
。
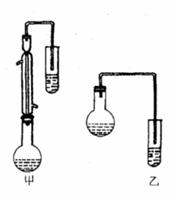 (2)甲和乙两位同学分别设计了如右下图两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。
(2)甲和乙两位同学分别设计了如右下图两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。
根据有机物的沸点,最好采用 装置(填“甲”或“乙”)。
理由是
。
(3)反应物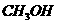 应过量,理由是
应过量,理由是
。
Ⅱ.粗产品的精制
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用下列流程进行精制,请在流程图中方括号内填入恰当操作方法的名称。
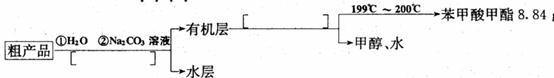
(5)以上流程中加入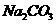 溶液后,放入分液漏斗中振荡、静置,要得到有几层,其具体操作是:
溶液后,放入分液漏斗中振荡、静置,要得到有几层,其具体操作是:
。
(6)通过计算,苯甲酸甲酯的产率为 。
29.(16分)某化学小组以苯甲酸为原料,制取苯甲酸甲酯。已知有关物质的沸点如下表:
|
物质 |
甲醇 |
苯甲酸 |
苯甲酸甲酯 |
|
沸点/℃ |
64.7 |
249 |
199.6 |
28.(13分)
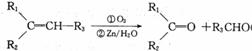 已知:
已知:
Ⅰ(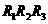 代表烷烃基)
代表烷烃基)
Ⅱ.烯醇式结构,即碳碳双键连接羟基(如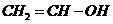 )不能稳定存在。
)不能稳定存在。
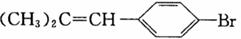 某有机物
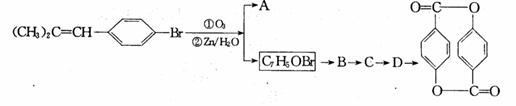
有如下转化关系:
某有机物
有如下转化关系:
(1)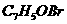 中官能团名称为
中官能团名称为
(2) 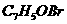 与银氨溶液在加热时反应的化学方程式是(有机物写结构简式,下同):
;
与银氨溶液在加热时反应的化学方程式是(有机物写结构简式,下同):
;
实验现象是 。
(3)从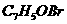 合成D通常要经过几步有机反应,其中最佳顺序瘦是
(填序号)。
合成D通常要经过几步有机反应,其中最佳顺序瘦是
(填序号)。
a.水解、酸化、氧化 b.氧化、水解、酸化
c.水解、酸化、还原 d.氧化、水解、酯化
(4)若按“最佳顺序”进行,写出一定条件下B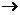 C的化学反应方程式:
C的化学反应方程式:
(5)A有一种同分异构体,能与Na反应放出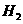 ,则其结构简式为:
,则其结构简式为:
该有机物在一定条件下能发生加聚反应,其化学方程式为:
该反应所形成的高聚物吸水性强,原因可能是
27.(15分)有7种物质:NH3、Mn2O3、ZnCl2、MnO2、NH4Cl、Zn和H2O,分别是锌一锰电池中氧化还原反应的反应物和生成物。
(1)①完成并配平该氧化还原方程式:
_______+________+___NH4Cl=_________+_________+_______+___NH3
②发生还原反应的物质是_______,被氧化的元素是_________。
 ③若有17.4 g氧化剂参与反应,则电子转移数目为_______NA(NA表示阿伏加德罗常数)
③若有17.4 g氧化剂参与反应,则电子转移数目为_______NA(NA表示阿伏加德罗常数)
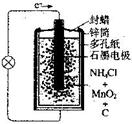
(2)普通锌一锰干电池是利用上述反应原理设计的,其结构如右图所示。回答下列问题:
①电池中电解质溶液为___________________________。
②正极材料为_____________________________________;
正极电极反应为____________________________________________________________。
③放电时NH4+向__________ (填“正极”、“负极”)移动。
④普通锌一锰电池的缺点是电量小、放电电流弱。为增大放电电流,可把负极锌片改为锌粉,其理由是__________________________________________________________。
26.(16分)W、X、Y、Z四种短周期元素,原子序数依次增大,在周期表中W与X相邻、Y与z相邻。已知W元素的氢化物与Z元素的氢化物反应只生成一种盐a;X、Y位于同一族,它们能组成YX2、YX3两种常见化合物。请回答下列问题:
(1)X元素位于周期表中第________族(用字母表示);
(2)X、Y、Z三种元素形成的单质中,氧化性最弱的是_______ (填化学式);
(3)Y与Z可形成共价化合物Y2Z2,分子中Y与Z均满足8电子稳定结构,则Y2Z2的电子式为__________________________________________________________________。
(4)a溶液的pH_____7(填“>”、“<”或“=”),用离子方程式解释为:若在a溶液中加入少量镁粉,可观察到的现象是:____________________________________________。
(5)取pH=0的W的最高价氧化物对应水化物的溶液100.0 mL于某容器中,加入0.90 g Cu、Ag合金样品,充分反应后测得生成WO(其中O表示氧元素)气体的体积为156.8 mL(标准状况下),反应后容器中溶液的c(H+)=0.72 mol·L-1反应后溶液体积不变)。
若设Cu、Ag的物质的量分别为x、y。欲求算x、y的值,可列出下列计算式:
I.64x+108y=0.90 该计算式是依据________________________关系列出的;
Ⅱ.2x+y=1mol·L-1×0.1 L-(0.72 mol·L-1×0.1 L+0.1568 L/22.4 L·mol-1)该计算式依据的是_____________守恒。
25.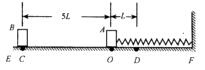 (20分)如图所示,EF为绝缘水平面,O点左侧是粗糙的,右侧是光滑的,一轻质绝缘弹簧右端固定在墙壁上,左端与静止在O点、质量为m的不带电小物块A连接,弹簧处于原长状态。质量为2 m,电荷量为q的带正电物块B,在水平向右、电场强度为E的匀强电场作用下由C处从静止开始向右运动,B运动到O点时与物块A相碰(设碰撞时间极短,碰撞过程中无电荷量损失,A、B不粘连),碰后它们一起向右运动,当它们运动到D点时撤去电场。已知物块B与地面.EO段间的滑动摩擦力大小为0.2 Eq,物块B和A均可视为质点,弹簧的形变始终在弹性限度内,且CO=5L,OD=L。求:
(20分)如图所示,EF为绝缘水平面,O点左侧是粗糙的,右侧是光滑的,一轻质绝缘弹簧右端固定在墙壁上,左端与静止在O点、质量为m的不带电小物块A连接,弹簧处于原长状态。质量为2 m,电荷量为q的带正电物块B,在水平向右、电场强度为E的匀强电场作用下由C处从静止开始向右运动,B运动到O点时与物块A相碰(设碰撞时间极短,碰撞过程中无电荷量损失,A、B不粘连),碰后它们一起向右运动,当它们运动到D点时撤去电场。已知物块B与地面.EO段间的滑动摩擦力大小为0.2 Eq,物块B和A均可视为质点,弹簧的形变始终在弹性限度内,且CO=5L,OD=L。求:
(1)撤去电场后弹簧的最大弹性势能;
(2)返回运动的过程中,物块B由O点向左运动直到静止所用的时间。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com