
题目列表(包括答案和解析)
6.下列有关比较中,大小顺序排列错误的是
A.物质的熔点:石英>食盐>冰>汞
B.热稳定性:PH3>H2S>HBr>NH3
C.结合质子的能力:CO32->CH3COO->SO42-
D.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液
5.物质世界中有很多变化是由物理变化造成的。以下变化或过程就属于物理变化的是
A.激光法蒸发石墨得C60 B.渗析法净化氢氧化铁胶体
C.鸡蛋白遇浓硝酸显黄色 D.直流电通过氯化钠水溶液
4.100℃时,将0.1molN2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) 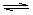 2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
①烧瓶内气体的颜色不再加深,②N2O4 的消耗速率与NO2的生成速率之比为1∶2,③NO2的生成速率与NO2消耗速率相等,④NO2的物质的量浓度不变,⑤烧瓶内气体的质量不再变化,⑥烧瓶内气体的压强不再变化,⑦烧瓶内气体的密度不再变化,⑧烧瓶内气体的平均相对分子质量不再变化
A.②⑤⑦ B.①③④⑥⑧ C.只有③ D.只有⑤
3.下列说法中,正确的是 ( )
A.离子晶体的组成中一定有金属元素
B.晶体中有阳离子就一定有阴离子 。
C.由原子组成的晶体可以是原子晶体,也可以是分子晶体
D.离子晶体不可能存在非极性共价键
2.旨在限制全球温室气体排放量的《京都都议定书》于2005年2月16日正式生效。为降低
我国二氧化碳气体排放量(居世界第二)的下列措施中,你认为不切合实际的是 ( )
A.停止使用产生二氧化碳气体的化学能
B.充分利用太阳能
C.合理、安全开发利用氢能、核能
D.因此制宜开发利用风能、水能、地热能、潮汐能
1.关于工业生产的下列叙述中,不正确的是
A.工业生产硫酸时,使用热交换器可以充分利用反应中所放出的热量
B.工业上合成氨没有采用更大的压强是从设备和动力要求方面考虑的
C.工业上用离子交换膜法电解饱和食盐水制烧碱
D.工业上采用电解熔融氯化铝的方法制取金属铝
37. 9.6g铜溶于足量的稀硝酸。请写出反应的化学方程式,并计算反应产生的气体在标准状况下的体积。
25(10分).有 A、B、C、D、E五种化合物,它们分别由Na+、Ba2+、
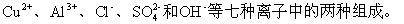
(1)白色固体A既不溶于水,也不溶于稀硝酸。
(2)白色固体B不溶于水,但加入焰色反应为黄色的E溶液时,B溶解且生成无色的溶液。
(3) C与E具有相同的阴离子,C与稀硫酸反应可以生成A。
(4)D是一种棕黄色固体,溶解于水后形成绿色的溶液。D溶液与E溶液反应可以得到蓝色的沉淀。
根据上述实验事实,推断A、B、C、D、E各为什么物质。
A 、B 、C 、D 、E 。
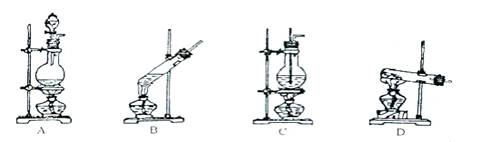
36(5分).实验室制取NH3选择下图所示气体发生装置中的 (填代号),反应的化学方程式: 。收集NH3通常使用 法。
21(6分).以下叙述错误的是:
A.随手丢弃废电池会导致土壤污染
B.浓硝酸久置变黄是因为硝酸被空气中的氧气氧化
C.氮族元素是位于周期表中第ⅤA族元素
D.氨气泄露可以用水吸收以消除对环境的污染
E.氮族元素都是非金属元素
F.王水是浓硝酸和浓盐酸(体积比3﹕1)的混合物
G.铜锌原电池中锌是负极
22(3分).在某一化学反应中,反应物B的浓度在5S内从2.0mol/L变成0.5mol/L,在这5S内B的化学反应速率为 。
23(4分).反应CO(g)+H2O(g) 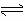 CO2(g)+H2(g)(正反应是放热反应)已达平衡。
CO2(g)+H2(g)(正反应是放热反应)已达平衡。
(1)通入过量的水蒸气,平衡 移动。
(2)减少CO的浓度,平衡 移动。
(3)增大平衡体系的压强,平衡 移动。
(4)使用催化剂,平衡 移动。
24.(5分)A是一种在磁场作用下自身能产生磁性的金属,B、C、D、E、F均含有A元 素,它们之间有如下变化关系:
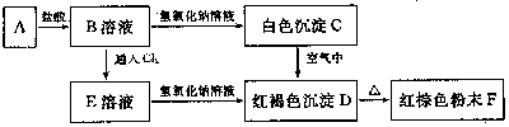
(1) B的名称是__________________________。
(2) F的化学式是_________________________。
(3) C→D反应的化学方程式是:___________________________________________。
20.取两份铝粉,第1份加入足量的盐酸,第2份加入足量的氢氧化钠,如果放出等体积气体,两份铝粉的质量之比为( )
A.1:2 B.1:3 C.3:2 D.1:1
第Ⅱ卷(非选择题共40分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com