
题目列表(包括答案和解析)
14.某恒温恒容的容器中,反应2A(g)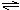 B(g)建立了平衡。若再向容器中通入一定量的A气体或B气体,重新达到平衡后,有关容器内A、B的体积分数说法正确的是
B(g)建立了平衡。若再向容器中通入一定量的A气体或B气体,重新达到平衡后,有关容器内A、B的体积分数说法正确的是
A.气体A的体积分数比原平衡时大,气体B的体积分数比原平衡时小
B.气体A的体积分数比原平衡时小,气体B的体积分数比原平衡时大
C.气体A、B的体积分数都比原平衡时小
D.气体A、B的体积分数都比原平衡时大
13.等体积的0.1mol/L的盐酸与0.06mol/L的Ba(OH)2溶液混合后,溶液的pH等于
A.2.0 B.12.3 C.1.7 D.12.0
12.T °C时A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图(1)所示;若保持其他条件不变,温度分别为T1和T2时,B的体积百分含量与时间的关系如图(2)所示。则下列结论正确的是
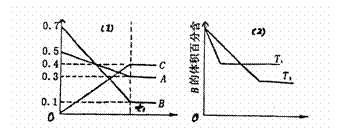
图(1) 图(2)
A.在(t1+10)min时,保持其它条件不变,增大压强,平衡向逆反应方向移动
B.其它条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大
C.T °C若由0.4mol/L A、0.4mol/L B、0.2mol/L C反应、达到平衡后,C的浓度仍为0.4mol/L
D.(t1+10)min保持压强不变,通入稀有气体,平衡向正反应方向移动
11.在0.1mol/L的CH3COOH溶液中,要促进醋酸电离,且氢离子浓度增大,应采取的措施是
A.升温 B.加水 C.加入NaOH溶液 D.加入稀HCl
10.下列反应中熵减少的是
A.食盐晶体溶于水 B.氢气在氧气中燃烧生成液态水
C.碳酸氢铵分解 D.水蒸气冷凝为水
9.把1mL0.1mol/LH2SO4加水稀释制成2L溶液,在此溶液中由水电离产生的H+接近于
A.1×10-4mol/L B.1×10-8mol/L C.1×10-11mol/L D.1×10-10mol/L
8.下列各组热化学方程式程中,化学反应的△H前者大于后者的是
①C(s)+O2(g)=CO2(g);△H1
C(s)+1/2O2 (g)=CO(g);△H2
②S(s)+O2 (g)=SO2(g);△H3
S(g)+O2 (g)=SO2(g);△H4
③H2(s)+1/2O2(g)=H2O(g);△H5
2H2 (g)+O2(g)=2H2O(l);△H6
④CaCO3(s)=CaO(s)+CO2(g);△H7
CaO(s)+H2O(l)=Ca(OH)2(s);△H8
A.① B.③④ C.②③④ D.①②③
7.常温常压下在可移动活塞的甲、乙容器(如图)里分别充有等体积的二氧化氮和空气,已知:2NO2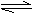
 N2O4;△H<0.现分别进行下列两个实验:①将两容器置于沸水中加热;②在活塞上都加2千克的砝码。在以上两情况下,甲和乙容器中气体体积大小的比较,正确的是
N2O4;△H<0.现分别进行下列两个实验:①将两容器置于沸水中加热;②在活塞上都加2千克的砝码。在以上两情况下,甲和乙容器中气体体积大小的比较,正确的是
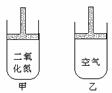 A.①甲>乙 ②甲>乙
A.①甲>乙 ②甲>乙
B.①甲>乙 ②甲<乙
C.①甲<乙 ②甲>乙
D.①甲>乙 ②甲=乙
6.在密闭容器中进行下列反应:M(气)+N(气) R(气)+2L(?),该反应中
R(气)+2L(?),该反应中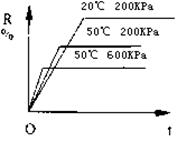 R的百分含量在不同条件下的变化如下图所示,请判断下列结论正确的是
R的百分含量在不同条件下的变化如下图所示,请判断下列结论正确的是
A.正反应为放热反应,L为气体
B.正反应为吸热反应,L为气体
C.正反应为吸热反应,L为固体或液体
D.正反应为放热反应,L为固体或液体
5.己知胆矾溶于水时温度降低,室温下,将1mol无水硫酸铜配成溶液时放出的热量为Q1kJ,又知胆矾分解的热化学方程式为∶ CuSO4•5H2O(s)=CuSO4(s)+5H2O(l) ΔH=+Q2kJ/mol 则Q1、Q2的关系为
A.Q1<Q2 B.Q1>Q2 C.Q1=Q2 D.无法确定
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com