
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
28.(1)ΔΌΓΓI2ΓΓ ΔΎ≤Μ «ΘΜ(2)ΔΌCΓΓ ΔΎ»ή“ΚΖ÷≤ψΓΔ…œ≤ψΈό…Ϊœ¬≤ψΉœ…ΪΘΜΔέCCl4”κΥ°ΜΞ≤Μœύ»ή«“I2‘ΎCCl4÷–»ήΫβΕ»±»‘ΎΥ°÷–ΒΡ¥σΓΓ (3)»Γ“ΜΝΘΜΣΥΊΤ§―–œΗΚσ»ή”ΎΥ°≈δ≥…»ή“Κ‘ΌΒΈΦ”ΒμΖέ»ή“Κ»γ»ή“Κ±δάΕ‘ρΥΒΟςΤδΚ§I2ΓΘ
27ΓΔ(1)DΓΓ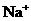 (2)ΒΎ»ΐ÷ήΤΎΓΔIIIΉε
(2)ΒΎ»ΐ÷ήΤΎΓΔIIIΉε
(3)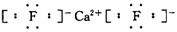 (ΟΩΩ’2Ζ÷Θ§Ι≤8Ζ÷)
(ΟΩΩ’2Ζ÷Θ§Ι≤8Ζ÷)
26ΓΔ(Δ≈ΔΎΓΓ ΔΤPCl3ΜρCCl4ΓΓ ΒΎ»ΐ÷ήΤΎΓΔΔωAΉεΓΓ 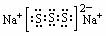 ΓΓΔ«KC8)
ΓΓΔ«KC8)
25ΓΔΔ≈ΓΓ ΘΨΓΓΓΓΘΦΓΓΓΓΔΤ »γœ¬ΆΦΓΓΓΓΓΓ Δ«ΓΓ +236(12Ηω)
24ΓΔΫβΈωΘΚ(1)Β»Έο÷ ΒΡΝΩΒΡNaNO3ΚΆKCl»ή”ΎΥ°ΚσΘ§Υυ–Έ≥…ΒΡΥΡ÷÷Έο÷ Ϋ‘“Ή»ή”ΎΥ°Θ§“ΣΖ÷άκΥϋΟ«÷ΜΡήΗυΨί≤ΜΆ§Έ¬Ε»œ¬»ήΫβΕ»ΒΡ≤ΜΆ§Ϋχ––Θ§“ρ¥Υ Β―ιΔΌΔέΒΡΙΊΦϋΧθΦΰ «Έ¬Ε»ΓΘ
(2)Ζ÷άκKNO3(NaCl)ΨßΧε”κ»ή“ΚΒΡ≤ΌΉςΈΣΙΐ¬ΥΓΘΗυΨίΧβΡΩΥυΗχ»ήΫβΕ» ΐΨίΘ§100Γφ ±’τΖΔH2OΚσΒΟΒΫNaClΨßΧε(NaCl»ήΫβΕ»Ήν–Γ)Θ§ά以ΚσΒΟΒΫΒΡ÷ς“Σ «KNO3(»ήΫβΕ»÷°≤νΉν¥σ)Θ§Ι C «KNO3ΓΘ
(3)‘Ύ100Γφ ±NaCl»ή“Κ“―±ΞΚΆΘ§Ι ΫΒΈ¬ά以Ιΐ≥Χ÷–Θ§‘ΎΒΟKNO3ΨßΧεΒΡΆ§ ±Θ§”–…ΌΝΩNaClΈω≥ωΘ§Φ¥ΨßΧε÷–Κ§Na+ΓΔClΘ≠Θ§Na+”Ο―φ…ΪΖ¥”ΠΦλ―ιΘ§ClΘ≠”ΟAgNO3»ή“ΚΚΆœΓHNO3Φλ―ιΓΘ
(4)Ε‘Κ§”–…ΌΝΩNaClΒΡKNO3Ω…”Ο÷ΊΫαΨßΒΡΖΫΖ®Χα¥ΩΓΘ
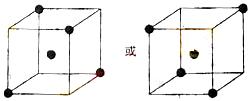 ¥πΑΗΘΚ(1)Έ¬Ε»ΓΓ (2)Ιΐ¬ΥΓΓ CΓΓ
(3)Na+ΓΔClΘ≠ΓΓ Na+”Ο―φ…ΪΖ¥”ΠΦλ―ιΘ§ClΘ≠”ΟAgNO3»ή“ΚΚΆœΓHNO3Φλ―ιΓΓ (4)÷ΊΫαΨß
¥πΑΗΘΚ(1)Έ¬Ε»ΓΓ (2)Ιΐ¬ΥΓΓ CΓΓ
(3)Na+ΓΔClΘ≠ΓΓ Na+”Ο―φ…ΪΖ¥”ΠΦλ―ιΘ§ClΘ≠”ΟAgNO3»ή“ΚΚΆœΓHNO3Φλ―ιΓΓ (4)÷ΊΫαΨß
23ΓΔ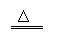 ¥πΑΗΘΚΚλΚ÷ΓΓ Fe(OH)3ΫΚΧεΓΓ
Fe3++3H2OΓΓΓΓΓΓΓΓ
Fe(OH)3(ΫΚΧε)+3H+
¥πΑΗΘΚΚλΚ÷ΓΓ Fe(OH)3ΫΚΧεΓΓ
Fe3++3H2OΓΓΓΓΓΓΓΓ
Fe(OH)3(ΫΚΧε)+3H+
(1)÷πΫΞ±δ…νΓΓ Fe(OH)3ΫΚΝΘ¥χ’ΐΒγΚ…ΓΓ Βγ”Ψ
(2)–Έ≥…ΚλΚ÷…Ϊ≥ΝΒμΓΓ ΒγΫβ÷ (NH4)2SO4Βγάκ≥ωΒΡSO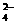 άκΉ”÷–ΚΆΝΥΫΚΧεΝΘΉ”Υυ¥χΒγΚ…Θ§ ΙFe(OH)3ΫΚΧεΨέ≥Ν
άκΉ”÷–ΚΆΝΥΫΚΧεΝΘΉ”Υυ¥χΒγΚ…Θ§ ΙFe(OH)3ΫΚΧεΨέ≥Ν
(3)œ»≥ωœ÷ΚλΚ÷…Ϊ≥ΝΒμΘ§Κσ≥ΝΒμ»ήΫβ–Έ≥…ΜΤ…Ϊ»ή“ΚΓΓ ΒγΫβ÷ H2SO4 ΙFe(OH)3ΫΚΧεΨέ≥ΝΘ§ΥφΉ≈H2SO4ΒΡΦ”»κΘ§H+”κFe(OH)3ΖΔ…ζΖ¥”ΠFe(OH)3+3H+=====Fe3++3H2OΘ§ Ι≥ΝΒμ»ήΫβΓΘ
(4)…χΈω
22ΓΔ(1)ΫΪΒΦΙήΒΡ≥ωΩΎΫΰ»κΥ°≤έΒΡΥ°÷–Θ§ ÷Έ’ΉΓ ‘ΙήΘ§”–Τχ≈ί¥”ΒΦΙήΩΎ“ί≥ωΘ§Ζ≈ΩΣ ÷ΚσΘ§”–…ΌΝΩΥ°Ϋχ»κΒΦΙήΘ§±μΟςΉΑ÷Ο≤Μ¬©ΤχΓΘ
ΓΓ (2)ΔΎΔΌΔέΓΓ (3)¬ΐ¬ΐΫΪΝΩΆ≤œ¬“Τ
ΓΓ (4)[22.4L.mol-1 ΓΝ298KΓΝ (a-b)g]/ 273K ΓΝ c L
21ΓΔ Σ»σ_Φ묩ΓΔ»σœ¥_Η…‘ο
28Θ°(11Ζ÷)œ¬Οφ «ΙΊ”Ύ“©ΈοΜΣΥΊΤ§(ΈςΒΊΒβΤ§) Ι”ΟΥΒΟς ιΒΡ≤ΩΖ÷ΡΎ»ίΓΘ

(1)ΗυΨί…œ ωΥΒΟςΚΆΥυ―ßΜ·―ß÷Σ ΕΜΊ¥πΘΚ
ΔΌΜΣΥΊΤ§÷–Κ§”–ΒΡΜν–‘≥…Ζ÷ «ΓΓΓΓΓΓΓΓΓΓ(–¥Ζ÷Ή” Ϋ)
ΔΎ«κΆΤΕœΜΣΥΊΤ§ΓΓΓΓΓΓΓΓ(ΓΑ «Γ±ΜρΓΑ≤Μ «Γ±)ΑΉ…ΪΓΘ
(2)Ρ≥―ß…ζΈΣ―ι÷ΛΜΣΥΊΤ§÷–»Ζ ΒΚ§”–…œ ω≥…Ζ÷Θ§Άξ≥… Β―ι»γœ¬Θ§«κΧνΩ’ΘΚ
ΔΌ»Γ“ΜΝΘ“©Τ§Ζ≈»κ―–≤ß÷–―–ΥιΘ§‘ΌΫΪ“©ΖέΉΑ»κ ‘Ιή≤ΔΦ”»κ‘Φ2mL’τΝσΥ°ΘΜœρΗΟ ‘Ιή÷–‘ΌΦ”»κ‘Φ2mLΓΓΓΓΓΓΓΓΓΓΓΓ (Χν―ΓœνΉ÷ΡΗ)Θ§≤Δ”ΟΝΠ’ώΒ¥ΘΜ
AΘ°ΨΤΨΪΓΓΓΓΓΓ BΘ°»»Ν―Τϊ”ΆΓΓΓΓΓΓΓΓΓΓ CΘ°ΥΡ¬»Μ·ΧΦΓΓΓΓΓΓΓΓ DΘ°Η ”Ά
ΔΎΟη ωΦ”»κΗΟ“ΚΧεΚσΩ…ΡήΙέ≤λΒΫΒΡœ÷œσΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓ
Δέ―Γ”ΟΗΟ“ΚΧεΉω Β―ιΒΡ‘≠“ρ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓ
(3)«κ‘Ό…ηΦΤΝμ“Μ÷÷ΖΫΖ®Θ§―ι÷ΛΜΣΥΊΤ§÷–ΒΡ≥…Ζ÷Θ§(ΉΔ“β–π ω Β―ι‘≠άμΓΔ≤ΌΉςΖΫΖ®ΚΆ Β―ιΫα¬έ)ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓ
(4)ΜΣΥΊΤ§÷–÷ς“Σ≥…Ζ÷‘Ύ “Έ¬ ± τΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΨßΧεΓΘ
27Θ°(11Ζ÷) AΓΔBΓΔCΓΔDΓΔEΕΦ «‘ΣΥΊ÷ήΤΎ±μ÷–«Α20Κ≈‘ΣΥΊΘ§‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§BΓΔCΓΔDΆ§÷ήΤΎΘ§AΓΔDΆ§÷ςΉεΘ§EΚΆΤδΥϊ‘ΣΥΊΦ»≤Μ‘ΎΆ§÷ήΤΎ“≤≤Μ‘ΎΆ§÷ςΉεΘ§BΓΔCΓΔDΒΡΉνΗΏΦέ―θΜ·ΈοΒΡΥ°Μ·ΈοΝΫΝΫΜλΚœΨυΡήΖΔ…ζΖ¥”Π…ζ≥…―ΈΚΆΥ°ΓΘ
ΓΓΗυΨί“‘…œ–≈œΔΘ§ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)AΚΆD«βΜ·Έο÷–Θ§Ζ–ΒψΫœΒΆΒΡ «________(―ΓΧνΓΑAΓ±ΜρΓΑDΓ±)ΘΜAΚΆBΒΡάκΉ”÷–Θ§ΑκΨΕΫœ–ΓΒΡ «________________(ΧνάκΉ”ΖϊΚ≈)ΓΘ
(2)‘ΣΥΊC‘Ύ‘ΣΥΊ÷ήΤΎ±μ÷–ΒΡΈΜ÷Ο «________ΓΘ
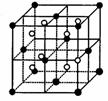
(3)AΚΆEΩ…Ήι≥…άκΉ”Μ·ΚœΈοΘ§ΤδΨßΑϊ(ΨßΑϊ «‘ΎΨßΧε÷–ΨΏ”–¥ζ±μ–‘ΒΡΉν–Γ÷ΊΗ¥ΒΞ‘Σ)ΫαΙΙ»γœ¬ΆΦΥυ ΨΘ§―τάκΉ”(”ΟΓΑΓώΓ±±μ Ψ)ΈΜ”ΎΗΟ’ΐΖΫΧεΒΡΕΞΒψΜρΟφ–ΡΘΜ“θάκΉ”(”ΟΓΑΓπΓ±±μ Ψ)ΨυΈΜ”Ύ–Γ’ΐΖΫΧε÷––ΡΓΘΗΟΜ·ΚœΈοΒΡΒγΉ” Ϋ «________ΓΘ
 ΓΓ ΓΓ
ΓΓ ΓΓ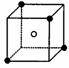
ΨßΑϊ ΓΓΓΓΓΓΓΓ ΨßΑϊΒΡ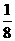
Δ»Ζ÷±π–¥≥ωAΓΔBΒΡΒγΉ”≈≈Ν– ΫΘ§CΒΡΙλΒά±μ Ψ ΫΘΚ
A.________ B._________C._______
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com