
题目列表(包括答案和解析)
27.(12分)一块未完全锈蚀的铜铁合金(铜未生锈)a g,加入1 mol·L-1的H2SO4溶液中(假设整个反应过程中无气体产生)。
(1)当消耗的硫酸体积为0.6 L时,合金片恰好溶解,且溶液中无Fe3+,则Fe2O3的质量是
g。
(2)a g合金片溶于1 L硫酸中,溶液中c(Fe3+)=0.1 mol·L-1、c(Cu2+)=0.05 mol·L-1,
则a的范围是 ,(假设反应后溶液的体积为1 L)。
26.(8分)将0.2 mol金属R的一种含氧酸盐在隔绝空气条件下加热,使之完全分解,生成0.2 mol R的氧化物RO以及CO、CO2混合气体,已知该混合气体对氢气的相对分子质量是18,体积为8.96 L(标准状况),金属R的原子核中质子数比中子数少4个。测得固体RO的质量比原含氧酸盐质量减轻一半。
(1)氧化物RO的质量是 g。
(2)该含氧酸盐的化学式为 。
25.(13分)醛可以发生分子间的反应,生成羟基醇。如:
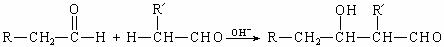
Ⅰ.根据上述信息,回答下列问题:
(1)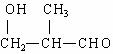 可由
与
两种醛合成。
可由
与
两种醛合成。
(2)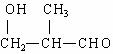 转化为
转化为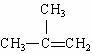 须依次经过 、
、
须依次经过 、
、
等较为合理的反应过程(填写反应类型名称)。
Ⅱ.已知烯烃在发生加成反应时,加成试剂中的氢总是加在含氢较多的不饱和碳上。
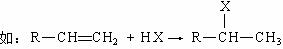
回答问题:
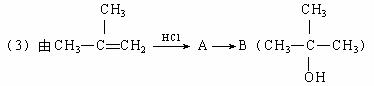
①写出A→B反应的化学方程式: (应注明反应条件)。
②A的同分异构体(不包括A)共有 种。
24.(8分)法国伊夫·肖万和美国罗伯特·格拉布及理查德·施罗克因在烯烃的复分解方法方面所取得的成就而获得2005年诺贝尔化学奖。金属卡宾是指一类有机分子,其中有一个碳原子与一个金属原子以双键连接,它们也可以看做一对拉着双手的舞伴,在与烯烃分子相遇后,两对舞伴会暂时组合起来;手拉手跳起四人舞蹈,随后它们“交换舞伴”,组合成两个新分子,其中一个是新的烯烃分子,另一个是金属原子和它的新舞伴;后者会继续寻找下一个烯烃分子,再次“交换舞伴”。
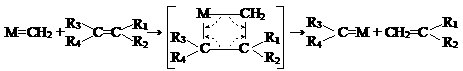
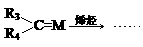
以下是利用烯烃复分解反应进行的合成,其中M==CH2为金属卡宾(Grubbs)。
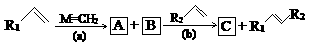
(1)写出(a)、(b)反应的化学方程式 ; 。
(2)从整个过程来看,金属卡宾的作用是 。
(3)写出卡宾在一定条件下可形成的CH2的电子式 。
23.(11分)下图表示各物质之间的转化关系。已知:A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1:1,但I晶体中阴、阳离子个数比是2:1,I常用做干燥剂。B还含非极性共价键。
请按要求填空:
(1)G的电子式是 。
(2)反应⑥的化学方程式是 ,反应⑤在空气中发生时的现 象是 ,已知C的燃烧热是1300 kJ·mol-1,则表示C 的燃烧热的热化学方程式是 。
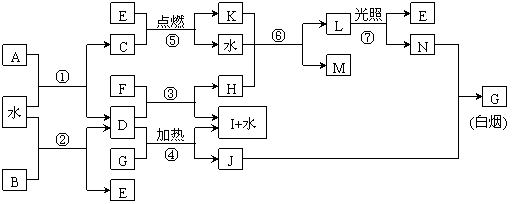 (3)根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是
。
(3)根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是
。
22.(10分)A、B、C、D、E五种短周期元素的原子序数依次增大,且知:
①其原子半径的大小关系是:D>E>B>C>A;
②A、D同主族,并可形成离子晶体DA;
③B、D、E三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素;
④B、E两种元素原子的最外层电子数之和等于A、C、D三种元素原子的最外层电子数之和。
请填写下列空白:
(1)DA与水反应后所得溶液的pH 7(填“>”、“<”或“=”)。
(2)化合物D2C2的电子式为 ,化合物BA5所属晶体类型为 。
(3)1mol E单质与足量的D的最高价氧化物的水化物溶液反应,能产生 mol A2气体。
(4)化合物BA3与BC在加热和有催化剂存在的条件下能发生反应,生成两种无毒物质,则该反应的化学方程式为 。
21.(13分)某兴趣小组的同学共同设置了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质。

(1)利用Ⅰ、Ⅱ装置制取气体(K2关闭,K1打开),甲同学认为:利用Ⅱ装置可以收集H2、NH3等气体,但不能收集O2和NO等气体,其理由是 。
乙同学认为:将Ⅱ装置作简单改进(不改变装置),也可收集O2和NO等气体,但不能收集NO2气体,则改进的方法是 ,将Ⅱ装置 再作简单改进(不改变装置),还可收集NO2气体,则改进方法是 。
(2)利用Ⅰ、Ⅲ装置验证物质的性质(K2打开,K1关闭),如证明氧化性:KMnO4>Cl2>Br2,则在A中加浓盐酸,B中加 ,C中加 ,观察到C中的现象是 。
(3)请利用Ⅰ、Ⅲ装置自行设计实验(K2打开,K1关闭),证明乙炔为不饱和的化合物,写出各仪器所加试剂:
A中加 ,B中加 ,C中加 ,证明乙炔为不饱和化合物的现象是 。
20.(8分)某学生往一支试管中按一定的顺序分别加入下列几种物质(一种物质只加一 次):A.KI溶液 B.淀粉溶液 C.NaOH溶液 D.稀H2SO4 E.氯水。发现溶液颜色按如下顺序变化:①无色→②棕黄→③蓝→④无色→⑤蓝。
依据溶液颜色的变化,回答下列问题:
(1)加入以上药品的顺序是(写序号) 。
(2)①→②反应的化学方程式为 。
(3)溶液由棕黄色变为蓝色的原因是 。
(4)③→④反应的化学方程式为 。
19.某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等)
|
|
50mL盐酸 |
50mL盐酸 |
50mL盐酸 |
|
m(混合物) |
9.2 g |
15.7 g |
27.6 g |
|
V(CO2)(标况) |
2.24 L |
3.36 L |
3.36 L |
则下列分析推理中不正确的是
A.盐酸的物质的量浓度为3.0 mol·L-1
B.根据表中数据不能计算出混合物中NaHCO3的质量分数
C.加入混合物9.2 g时盐酸过量
D.15.7 g混合物恰好与盐酸完全反应
第Ⅱ卷 (非选择题 共83分)
18.要求设计实验证明,某种盐的水解是吸热的,则下列回答中正确的是
A.将硝酸铵晶体溶于水,若水温下降,说明硝酸铵水解是吸热的
B.在盐酸中加入相同浓度的氨水,若混合液温度下降,说明盐类水解是吸热的
C.在醋酸钠溶液中加入醋酸钠晶体,若溶液温度下降,说明盐类水解是吸热的
D.在醋酸钠溶液中滴入酚酞试液,若加热后红色加深,说明盐类水解是吸热的
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com