
题目列表(包括答案和解析)
5.从下列事实所列出的相应结论正确的是
|
|
实 验 事 实 |
结 论 |
|
A |
Cl2的水溶液可以导电 |
Cl2是电解质 |
|
B |
SO2通入硝酸钡溶液出现白色沉淀 |
BaSO3不溶于强酸 |
|
C |
NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 |
酸性:HCO3->Al(OH)3 |
|
D |
常温下白磷可自燃而氮气须在放电时才与氧气反应 |
非金属性:P>N |
4.根据所学知识,下列有关胶体的说法中正确的是英才苑
A.将饱和的FeCl3溶液加热至沸,制得Fe(OH)3胶体
B.将磁性物质制成胶体离子作为药物的载体,可在磁场作用下送到病灶
C.化工生产上可利用丁达尔效应将油漆粒子均匀地沉积在镀件上
D.将蔗糖溶于溶解在酒精中,则可形成胶体
3.下列有关说法正确的是
A.CaCl2、聚苯乙烯、HD均为化合物
B.CH2O2、C3H6O2、C4H8O2互为同系物
C.明矾、冰醋酸、硫酸钡均为电解质
D.SiO2、NaCl、S8、Cu均能表示物质分子组成
2.广东北江曾发生严重的水体镉污染事件,专家确定用1200吨的聚合铁{简称PFS,化学式为:[Fe2(OH)n(SO4)(3-n)/2]m,n<5,m<10}分批加入,利用PFS在水体中形成絮状物,以吸附镉离子。结合题中信息,下列说法正确的是
A.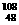 Cd核素原子中的电子数为48,中子数为60
Cd核素原子中的电子数为48,中子数为60
B.含镉废电池含镉量很少,无需进行回收处理
C.PFS是铁显十2价的一种碱式硫酸盐聚合物
D.实验室可通过FeSO4溶液水解和聚合制PFS
1. 下列化学用语表达正确的是
下列化学用语表达正确的是
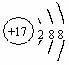
A.S2-的结构示意图: B.乙炔的结构简式CHCH
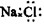 C.NaCl的电子式:
D.硝基苯的结构简式:
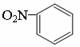
C.NaCl的电子式:
D.硝基苯的结构简式:
实验室用50ml浓盐酸跟足量的氯酸钾固体共热制取氯气,反应的化学方程式为(未配平):
KClO3 + HCl -- KCl + Cl2 ↑+ H2O
(1)配平上述反应化学方程式:
____ KClO3 +___ HCl ==__ KCl +__ Cl2 ↑+__ H2O
(2)浓盐酸在反应中显示出来的性质是 (填写编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)若产生0.1molCl2,则转移电子的物质的量为 mol.
(4)若反应中HCl的利用率只有50%,当氧化产物比还原产物多7.1g时,求浓盐酸的物质的量浓度。
20.(12分)为测定大理石中碳酸钙的纯度(设含杂质SiO2),某兴趣小组设计了如下方案:
①称取碳酸钙样品mg ②将样品充分高温煅烧,冷却后称量,剩余固体质量为m1g。
(1)该方案中高温煅烧应选用的仪器名称是 ;
判断碳酸钙样品完全分解的方法是 ;“冷却”应如何操作____ ;
理由是_____ _____ .
(2)有同学认为方案Ⅱ高温煅烧的过程中会发生CaCO3 + SiO2 CaSiO3
+ CO2↑,会导致测定结果有误,你认为这位同学的观点正确吗? ,(填“正确”或“错误”)
CaSiO3
+ CO2↑,会导致测定结果有误,你认为这位同学的观点正确吗? ,(填“正确”或“错误”)
请说明自己的理由: 。
19、(7分)(1)、实验室里化学试剂的保存方法是不相同的,下图中A、B、C、D、E是常见的一些保存药品的试剂瓶。请把下列常见试剂的序号填写在各试剂瓶下面的括号内。
①氢氧化钠溶液 ②浓硫酸 ③碳酸钠溶液 ④白磷 ⑤大理石 ⑥酒精 ⑦AgNO3溶液
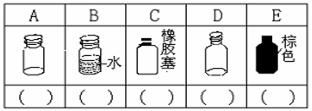
(2)皮肤溅上强碱液,急救时需要用到的物质及先后顺序是( )
A、水、稀醋酸 B、稀醋酸、水 C、水、稀盐酸 D、稀盐酸、水
18.(10分)根据下列框图关系填空。已知反应①、③是工业生产的重要反应,D为单质气体,E为无色刺激性气体,X由两种元素组成,常温下为无色液体,H为中学常见的强酸,H与E相对分子质量之间的关系为:Mr(H)-Mr(E)=34,又知C的焰色反应呈黄色,J为红褐色沉淀。
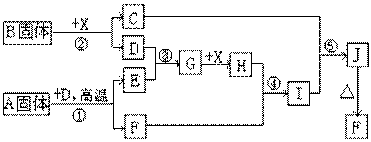
⑴ 写出下列物质的化学式B____________X____________
写出C的电子式______________。
⑵ 反应④的离子方程式为____________________________________;
反应③的化学方程式为____________________________________。
⑶ 已知每生成16g E,放出106.5kJ热量,则反应①的热化学方程式为_____________________________________________________________。
17.(10分)现有A、B、C、D四种短周期元素,A元素的原子半径是短周期元素中除稀有气体外半径最大的,B元素的原子最外层比次外层多3个电子,C元素是人体所含元素中质量分数最大的,D元素的一种同位素的质量数与质子数相等。请据此填空:
(1)A的原子结构示意图是 ;B2分子的电子式是 。
(2)C元素常见单质的化学式为 、 。
(3)C和D可形成电子数相同的两种粒子,该两种粒子反应后生成一种
中性分子,反应的离子方程式是 。
(4)A与B形成的一种化合物中,A元素的质量分数为35.4%,该化合物的摩尔质量不超过70g/mol,则该化合物的化学式是 ,其中可能有的化学键为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com