
题目列表(包括答案和解析)
23.(13分)工业上用铝土矿(主要成分是Al2O3,还有少量的Fe2O3、SiO2)提取冶炼铝的原料氧化铝。工艺流程如下图:
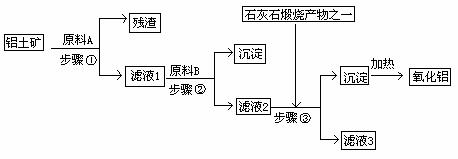
(1)原料A的名称是_____________,步骤①反应的离子方程式是_________________。
(2)滤液1中要加入稍过量原料B,原料B的化学式是________________,步骤②反应的离子方程式是:__________________________________________。
(3)步骤③的化学方程式是:_____________________________________________。
(4)如果省去步骤①,即溶解铝土矿是从加入原料B开始,则会对氧化铝的提取有什么影响___________________________________________________________________。
22.(9分)短周期的四种元素X、Y、Z、W,原子系数依次增大,Z原子最外层电子数是X、Y、W三种原子的最外层电子数之和,Z与X、Y、W三种元素形成原子个数之比为1:1的化合物分别是A.B.C,其中化合物C在空气中容易变白,请回答:
(1)写出Z的原子结构示意图_____________________________________________。
(2)写出化合物YZ2电子式:______________________________________________,
写出化合物C的电子式:______________________________________________。
(3)写出化合物C在空气中变白的化学方程式:_______________________________
_____________________________________________________________________。
20.(7分)为了测定某烷样品(丁烷,并含少量丙烷等气态烃)的平均相对分子质量,设计了下面的实验:
1取一个配有合适胶塞的洁净、干燥的锥形瓶,准确称量得到质量m1。
2往锥形瓶中通入干燥的该烷烃样品,塞好胶塞,准确称量;重复操作,直到前后2次称量结果基本相同,得到质量m2。
3往锥形瓶内加满水,塞好胶塞,称量得到质量m3。已知实验时的温度为T(k),压强p(kPa),水的密度ρ水(g/L),空气平均相对分子质量29.0,空气的密度ρ空气(g/L),回答下列问题:
(1)本实验的理论依据是(具体说明)__________________________________________
___________________________________________________________________________。
(2)步骤2中为什么要重复操作,直到后2次称量结果基本相同?答:______________
___________________________________________________________________________。
(3)具体说明本实验中怎样做到每次测量都是在相同体积下进行的?答:____________
___________________________________________________________________________。
(4)本实验收集气体样品的操作,可选用的方法是(填图中标号)__________。
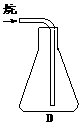
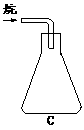


(5)锥形瓶内空气的质量m空气是_______________________________________。
(6)瓶中样品的质量m样品是___________________________________________。
(7)由实验测得该烷烃的平均相对分子质量是______________________________。
[(5)(6)(7)三空均列出算式]
19.(6分)“过氧乙酸”是抗“非典”中广泛用于医院、地面、门窗、汽车等方面的消毒液。下面是市售过氧乙酸商品标签:
|
过氧乙酸 甲、乙溶液各500mL 用法:把本品甲溶液1份,乙溶液 1份在玻璃或塑料容器内混合放24 小时,即可稀释使用 |
技术要求 含量不少于10%,一般可以用50倍纯水稀释使用(浓度为0.2%) |
(1)配制过氧乙酸消毒液的甲、乙溶液的主要成分各是什么?某校研究性学习小组为此进行以下研究,请你完成下列相关内容:
1查阅资料:过氧乙酸消毒液是由H2O2、H2O、CH3COOH及少量H2SO4混合后,反应生成过氧乙酸(CH3COOOH)为主要消毒成份的溶液。CH3COOOH容易放出原子氧,它与空气中微生物机体作用,达到灭菌目的。H2O2在酸性介质中稳定,是一种强氧化剂。
2提出假设:__________________________________________________________。
3实验验证:
|
实验主要步骤 |
实验主要现象 |
|
|
|
4得出结论:__________________________________________________________。
(2)该校根据“非典”消毒要求,急需配制0.2%过氧乙酸消毒液1m3,需要购进甲溶液_________瓶,乙溶液____________瓶。
18、氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有H2生成,下列叙述不正确的是:( BC )
A.NH4H是离子化合物 B.NH4H溶于水,所形成的溶液显酸性
C.NH4H与水反应时,NH4H是氧化剂
D.NH4H固体投入少量的水中,有两种气体生成
17、某K2CO3样品中含有Na2CO3、KNO3和Ba(NO3)2三种杂质中的一种或两种。现将13.8g样品放入足量水中,样品全部溶解。再加入过量的CaCl2溶液,得到9g沉淀。对样品所含杂质的正确判断是:( AB )
A.肯定有KNO3 B.肯定有KNO3,可能还含有Na2CO3
C.肯定没有Ba(NO3)2,可能有KNO3 D.肯定没有Na2CO3和Ba(NO3)2
16、将x molCO和y mol H2的混合气体充入盛有足量Na2O2的密闭容器中,再通入z molO2,并用电火花使其充分反应,有关容器内反应的下列叙述不正确的是:( B )
A.参加反应的Na2O2为:(x+y)mol
B.反应后容器中有O2:(x+y)/2mol
C.反应前后容器内压强之比(温度不变):(x+y)/z
D.反应后生成了x mol Na2CO3和2y mol NaOH
15、航天技术上使用一种氢氧燃料电池,它具有高能轻便、不污染环境等优点,该电池总反应方程式为:2H2+O2═2H2O,该电池的正极反应可表示为:( B )
A.4H++4e-═2H2↑ B.O2+2H2O+4e-═4OH―
C.4OH―-4e-═O2↑+2H2O D.2H2-4e-═4H+
14、在一定条件下,乳酸经一步反应能够生成的物质是:( A )
①CH2=CH-COOH
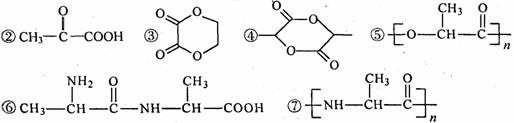
A.①②④⑤ B.①②③⑦ C.③⑤⑥ D.④⑥⑦
13、能正确表示下列反应的离子方程式是 ( B )
A.碳酸氢铵溶液中加入NaOH溶液共热 NH4++OH-  NH3
↑+H2O
NH3
↑+H2O
B.用碳酸钠溶液吸收少量二氧化硫 2CO32-+SO2+H2O ==2HCO3-+SO32-
C.FeBr2溶液中加入过量的氯水 2Fe2++2Br-+2Cl2 ==Br2+4Cl-+2Fe3+
D.硫酸镁溶液和氢氧化钡溶液反应 SO42-+Ba2+ ==BaSO4↓
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com