
题目列表(包括答案和解析)
23.(本小题共10分) 电解羧酸类金属盐的溶液,可得到脱去羧基后的有机物。例如,
|
2CH3COOK+2H2O == C2H6↑+2CO2↑+H2↑+2KOH。现将CH3COOK改为ClCH2COOK溶液,根据衍变关系, 回答有关问题。
|
|
|
|
|
|
 ClCH2COOK溶液 → A(混和物) → B溶液 → 纯净物B → C → D
E
ClCH2COOK溶液 → A(混和物) → B溶液 → 纯净物B → C → D
E
(1)ClCH2COOK水溶液的电极反应式(惰性电极)为:
阴极:__________________________, 阳极________________________________。
(2) A(混和物) 的主要成分___________________
(3)B的结构简式为________________________________
(4) 设B和C的氧化均很完全。D与B以物质的量之比为1:1反应生成E,在不同的反
应条件下, E的结构有能有多种。若E为一种含有六原子环状结构的有机物,则E的结构简式是_________________________。
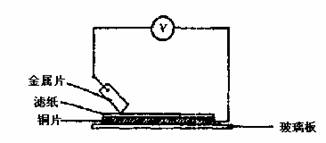
22. (本小题共10分) 将洁净的金属片A、B、C、D分别放置在浸有盐溶液的滤纸上面并压紧(如右图所示)。在每次实验时,记录电压表指针的移动方向和电压表的读数如下;
|
金属 |
电子流动方向 |
电压(V) |
|
A |
A→Cu |
+ 0. 78 |
|
B |
Cu→B |
-0.15 |
|
C |
C→Cu |
+ 1.35 |
|
D |
D→Cu |
+0.30 |
已知:构成两电极的金属其金属活泼性相差越大,电压表的读数越大。
请依据表中数据判断:
(1)____________金属可能是最强的还原剂;____________金属一定不能从硫酸铜溶液中置换出铜。
(2)若滤纸不用盐溶液浸润而改用NaOH溶液浸润,则在滤纸上能看到的蓝色沉淀析出的是_____________(填字母)金属。其对应的原电池的电极反应式为:
负极____________________,正极_____________________。
21. (本小题共8分) 已知在 0.lmol/L/的 NaHSO3溶液中有关微粒浓度由大到小的顺序为:
c(Na +)>c(HSO3-)>c(SO32-)>c(H2SO3)
①则该溶液中c(H+)______c(OH-)(填“>” “=”“<” =简述理由(并用离子方程式表示)__________________________________
②现向NH4HSO3溶液中,逐滴加入少量含有酚酞的NaOH溶液,可观察到的现象是______________________ ___;写出该反应的离子方程式______________________ _______。
③用铂电极电解NaHSO3溶液, 则总化学方程式是___________________________。
20.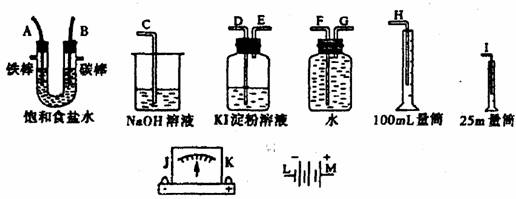 (本小题共12分) 请从下图中选出必要的装置进行电解饱和食盐水的实验,要求测定产生的氢气的体积(大于25mL),并检验氯气的氧化性。
(本小题共12分) 请从下图中选出必要的装置进行电解饱和食盐水的实验,要求测定产生的氢气的体积(大于25mL),并检验氯气的氧化性。
(1)A极发生的电极反应式是________,B极发生的电极反应式是____________。
(2)电源、电流表,与A、B两极的正确连接顺序为L→( )→( )→( )→( )→M。
(3)设计上述气体实验装置时,各接口的正确连接依序为
_______ 接________、_________接A、B接_________、_________接__________。
(4)已知饱和食盐水50mL,电流强度为IA,通电为 t min时,测得H2体积为 16.8mL(标况),此时溶液 pH约为___________,阿伏加德罗常数表达式NA为_______________(电子电量为l.6×10-19C, lg3=0.5)
19.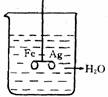 (本小题共8分) 如右图,(1)在银圈和铁圈(用细塑料棒连接)的连接处吊
(本小题共8分) 如右图,(1)在银圈和铁圈(用细塑料棒连接)的连接处吊
着一个绝缘的细丝,使之平衡,然后小心地从烧杯中央滴入CuSO4溶
液。①片刻后可观察到的现象是________________________。②产生上 述现象的原因是_________________________________。
(2) 将(1) 中细塑料棒取下, 使两环靠拢, 连接处吊着一个绝缘的细丝,调整圈的大小, 使 之平衡, 然后小心地从烧杯中央滴入CuSO4溶液。①片刻后可观察到的现象是_____________________ ___。②产生上述现象的原因是___________________________ ______。
18.下列关于实验现象的描述中不正确的是
A.把铜片和铝片紧靠在一起浸入稀硫酸中, 铜片表面出现气泡
B.用锌片作阳极, 铁片作阴极, 电解氯化锌溶液, 铁片表面出现一层锌
C.把铜片插入三氯化铁溶液中, 在铜片表面一层铁
D.实验室制H2, 把锌粒加入稀硫酸中, 再加几滴硫酸铜溶液, 气泡放出速率加快
第II卷 (非选择题 满分78分)
17.银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为: ( )
|
|
A.Ag B.Zn(OH)2
C.Ag2O D.Zn
16.用石墨电极电解饱和CuSO4溶液,一段时间后断开电路,要使溶液恢复到电解前浓度应向其中加入适量的 ( )
A.CuSO4 B.H2O
C.CuO D.Cu(OH)2
15.工业上①电解熔融Al2O3②电解熔融MgCl2③电解饱和NaCl溶液, 分别通过相同电子数时, 生成气体的物质的量大小是 ( )
A.①②③ B.③②①
C.③①② D.②③①
14.常温下镀锌铁片表面破损发生析氢腐蚀时,若有0.2mol电子发生转移,下列说法一定正确的是 ( )
A.有5.6g金属被腐蚀
B.有4.48L气体放出
C.有6.5g金属被腐蚀
D.有2.24L气体放出
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com